本试题 “有关乙炔分子中的化学键描述不正确的是[ ]A.两个碳原子采用sp杂化方式B.两个碳原子采用sp2杂化方式C.每个碳原子都有两个未杂化的2p轨道形成π键D.两个碳原...” 主要考查您对杂化轨道理论(中心原子杂化方式)
σ键、π键
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 杂化轨道理论(中心原子杂化方式)
- σ键、π键
杂化轨道理论:
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
分子的构型与杂化类型的关系:
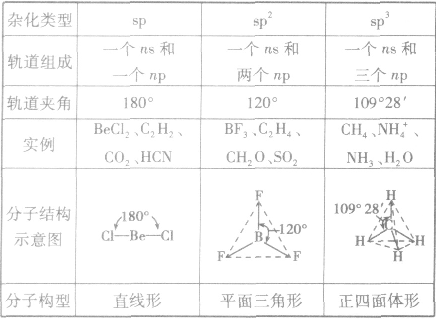
σ键:
成键原子的电子云以“头碰头”方式重叠形成的共价键,其特征是轴对称,即以形成化学键的两原子核的连线为轴作旋转,共价键的电子云图形不变。
π键:
成键原子的电子云以“肩并肩”方式形成的共价键,其特征是镜像对称,即:电子云由两块组成,若以包含原子核的平面为镜面,两块电子云互为镜像。
成键原子的电子云以“头碰头”方式重叠形成的共价键,其特征是轴对称,即以形成化学键的两原子核的连线为轴作旋转,共价键的电子云图形不变。
π键:
成键原子的电子云以“肩并肩”方式形成的共价键,其特征是镜像对称,即:电子云由两块组成,若以包含原子核的平面为镜面,两块电子云互为镜像。
共价键的分类:
(1)按成键原子是否相同或共用电子对是否偏移分 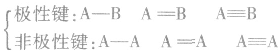
(2)按成键方式分

(3)按共用电子对数分
发现相似题
与“有关乙炔分子中的化学键描述不正确的是[ ]A.两个碳原子采用s...”考查相似的试题有:
- 甲烷、甲醇、肼(N2H4)、氨和氢气等都可作为燃料电池的燃料。(1)与甲醇互为等电子体的有机物分子式为__________,甲醇的熔、沸...
- 下列分子中的中心原子发生sp2杂化的是[ ]A.CH4B.NH3C.H2OD.BF3
- A、B、C、D、E、F六种元素位于短周期,原子序数依次增大,C基态原子核外有三个未成对电子,B与D形成的化合物BD与C的单质C2电...
- 已知a、b、x、y、z五种元素的原子序数依次增大,其中a原子的半径是所有原子中半径最小的,b原子中的电子有6种不同的运动状态...
- 下列分子或离子中,不存在sp3杂化类型的是( )A.SO42-B.NH3C.C2H6D.SO2
- 在乙烯分子中有5个σ键.一个π键,它们分别是[ ]A.sp2杂化轨道形成σ键.未杂化的2p轨道形成π键B.sp2杂化轨道形成π键.未杂化...
- (1)CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为___________;O22+中键数目和键数目之为________。(2)将乙炔通入[Cu(...
- 下列分子中的中心原子杂化轨道的类型相同的是( )A.SO3与SO2B.BF3与NH3C.BeCl2与SCl2D.C2H2与C2H4
- 氰气分子式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似。下列叙述正确的是[ ]A.在一定条件下可发生加成反应B.分子中的N≡C键...
- 下列关于σ键和π键的理解不正确的是[ ]A.σ键一般能单独形成,而π键一般不能单独形成B.σ键可以绕键轴旋转,π键一定不能绕键轴旋...