本试题 “(9分)某探究小组通过比较酸性KMnO4溶液与H2C2O4溶液反应过程中,溶液紫色消失时间长短的方法,研究浓度、温度对反应速率的影响。可供选择的实验条件:KMnO4...” 主要考查您对影响化学反应速率的因素
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 影响化学反应速率的因素
影响化学反应速率的因素:
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为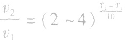
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
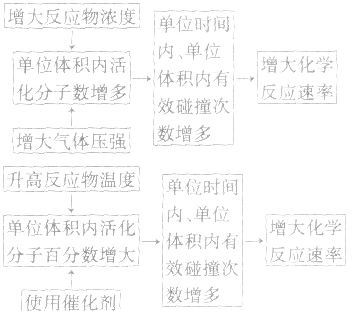
3.外因对化学反应速率影响的微观解释
1.内因:参加反应的物质的结构及性质。
2.外因:主要是指浓度、温度、压强和催化剂,另外还有光、超声波、激光、搅拌、固体表面积、形成原电池等。
(1)浓度:其他条件相同时,增大反应物浓度,化学反应速率增大;减小反应物浓度,化学反应速率减小。在一定温度下,同体、纯液体的浓度视为定值,如C与CO2的反应、Na与H2O的反应中,C的量和Na、H2O 的量减少并不意味着其“浓度”减小,即不冈其量的增减而影响反应速率,但会因固体表面积的变化而改变反应速率。
(2)温度:其他条件相同时,升高温度,可以加快反应速率,实验测得,温度每升高10℃,化学反应速率通常增大到原来的2~4倍。
经验公式为
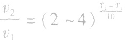
(3)压强:对于气体反应,当温度不变时,增大压强可以加快反应速率。对于气体反应体系,压强改变时有以下几种情况:

(4)催化剂:催化剂是能改变化学反应速率但在反应前后本身的质量和化学性质都不变的物质。对于某些化学反应,使用正催化剂能显著加快化学反应速率。
(5)其他因素:增大同体的表面积(如将块状改为粉末状),可增大反应速率;光照一般也可增大某些反应的速率;形成原电池可以加快反应速率;此外,超声波、放射线、电磁波等因素也能影响反应速率。
3.外因对化学反应速率影响的微观解释

发现相似题
与“(9分)某探究小组通过比较酸性KMnO4溶液与H2C2O4溶液反应过...”考查相似的试题有:
- 化学反应速率是通过实验测定的,下列化学反应速率的测量中,测量依据不可行的是( ) 选项化学反应测量依据(单位时间内)ACO(g...
- 下图曲线a表示放热反应X(g)+Y(g)Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线...
- 在容积可变的密闭容器中存在如下反应:2A(g)+2B(g)C(g)+3D(g) △H<0。如图为该可逆反应的反应速率一时间、转化率一时...
- 硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4==Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是[ ]反应温度...
- 下列说法错误的是( )A.在C(s)+H2O(g)CO(g)+H2(g)反应体系中,增加碳的量不能迅速提高正反应速率B.钾的金属性比钠...
- 加快化学反应速率可以采取的方法是( )A.升温B.减压C.降温D.减少反应物的浓度
- 下列说法中正确的是( )A.用完的干电池可以随意地丢弃B.增加炼铁高炉的高度不可以降低尾气中CO的含量C.使用催化剂一定能...
- 对于恒容密闭容器中一定条件下的反应:N2+3H2⇌2NH3,下列说法正确的是( )A.增加N2的量,可以加快反应速率B.当N2和H2全部...
- 下列做法,不能使的反应速率增大的是[ ]A.增大盐酸的浓度B.碾碎碳酸钙C.适当加热D.把2mol/L盐酸换成2mol/LH2SO4
- 下列关于催化剂的说法不正确的是( )A.温度越高,催化剂的催化效果越好B.汽车排气管上的“催化转化器”能减少有害气体排放C....