本试题 “向紫色石蕊溶液中通入二氧化碳,溶液变为______色,反应的方程式______,加热后溶液呈______色,反应的方程式______;盛装石灰水的瓶壁上常有一层白膜,这层...” 主要考查您对仪器的洗涤
化学反应方程式的书写
文字表达式
二氧化碳的性质
酸碱指示剂
物质的变质
物质的保存
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 仪器的洗涤
- 化学反应方程式的书写
- 文字表达式
- 二氧化碳的性质
- 酸碱指示剂
- 物质的变质
- 物质的保存
仪器的洗涤:
化学实验中干净的玻璃仪器有利于实验者观察到正确的实验现象,归纳、推理出正确的结论。因此,选择合适的洗涤剂,正确及时洗涤玻璃仪器,对于化学实验尤为重要。
洁净剂及其使用范围:
最常用的洁净剂有肥皂、合成洗涤剂(如洗衣粉)、洗液(清洁液)、有机溶剂等。
肥皂、合成洗涤剂等一般用于可以用毛刷直接刷洗的仪器,如烧瓶、烧杯、试剂瓶等非计量及非光学要求的玻璃仪器。
肥皂、合成洗涤剂也可用于滴定管、移液管、量瓶等计量玻璃仪器的洗涤,但不能用毛刷刷洗。
洗液多用于不能用毛刷刷洗的玻璃仪器,如滴定管、移液管、量瓶、比色管、玻璃垂熔漏斗、凯氏烧瓶等特殊要求与形状的玻璃仪器;也用于洗涤长久不用的玻璃仪器和毛刷刷不下的污垢。
洗涤玻璃仪器的方法与要求:
(1)一般的玻璃仪器(如烧瓶、烧杯等):先用自来水冲洗一下,然后用肥皂、洗衣粉用毛刷刷洗,再用自来水清洗,最后用纯化水冲洗3次(应顺壁冲洗并充分震荡,以提高冲洗效果)。计量玻璃仪器(如滴定管、移液管、量瓶等):也可用肥皂、洗衣粉的洗涤,但不能用毛刷刷洗。
(2)精密或难洗的玻璃仪器(滴定管、移液管、量瓶、比色管、玻璃垂熔漏斗等):先用自来水冲洗后,沥干,再用铬酸清洁液处理一段时间(一般放置过夜),然后用自来水清洗,最后用纯化水冲洗3次。
(3)洗刷仪器时,应首先将手用肥皂洗净,免得手上的油污物沾附在仪器壁上,增加洗刷的困难。
(4)一个洗净的玻璃仪器应该不挂水珠(洗净的仪器倒置时,水流出后器壁不挂水珠)。
玻璃仪器的干燥:
(1)晾干不急等用的仪器,可放在仪器架上在无尘处自然干燥。
(2)急等用的仪器可用玻璃仪器气流烘干器干燥(温度在60~70℃为宜)。
(3)计量玻璃仪器应自然沥干,不能在烘箱中烘烤。
玻璃仪器的保管:
要分门别类存放在试验柜中,要放置稳妥,高的、大的仪器放在里面。需长期保存的磨口仪器要在塞间垫一张纸片,以免日久粘住。
玻璃仪器洗涤干净的标准:
器壁内出现均匀水膜,既不聚成水滴,也不成股流下。
试管的洗涤:
倒掉时管内废液,注入半试管水,震荡后倒掉,这样连续洗几次;如果内部附有不易洗掉的物质,要用试管刷刷洗。刷洗时必须转动或上下移动试管刷,但用力不能过猛,以防试管损坏。
示意图如下:

一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2
 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
| 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。 ③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3
 CaO+ CO2↑
CaO+ CO2↑(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2
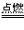 CO2
CO2 (3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2
 2CuO
2CuO ④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
二氧化碳是空气中常见的化合物,其分子式为CO?,由两个氧原子与一个碳原子通过共价键连接而成,常温下是一种无色无味气体,密度比空气略大,能溶于水,与水反应生成碳酸。固态二氧化碳俗称干冰。二氧化碳被认为是造成温室效应的主要来源。
物理性质:
常温下,二氧化碳是一种无色无味的气体,密度比空气大,能溶于水。
固态的二氧化碳叫做干冰。
化学性质:
(1)一般情况下,二氧化碳不能燃烧,也不支持燃烧,不供给呼吸,因此当我们进入
干枯的深井,深洞或久未开启的菜窖时,应先做一个灯火实验,以防止二氧化碳浓度
过高而造成危险
(2)二氧化碳和水反应生成碳酸,使紫色石蕊试液变红:CO2 + H2O===H2CO3,
碳酸不稳定,很容易分解成水和二氧化碳,所以红色石蕊试液又变回紫色:
H2CO3===H2O + CO2↑
(3)二氧化碳和石灰水反应:Ca(OH)2 + CO2====CaCO3↓+ H2O
(4)二氧化碳可促进植物的光合作用:6CO2+6H2O
 C6H12O6+6O2
C6H12O6+6O2 一氧化碳和二氧化碳性质的比较:
|
|
|
一氧化碳 |
二氧化碳 |
|
物理性质 |
状态 |
无色,无味气体 |
无色,无味气体 |
|
密度 |
1.250g/l(略小于空气) |
1.977g/l(大于空气) | |
|
溶解性 |
1体积水中约溶解0.02体积 |
1体积中约溶解1体积 | |
|
化学性质 |
可燃性 |
有可燃性 |
一般情况下,既不能燃烧,也不能支持燃烧 |
|
还原性 |
有还原性: |
没有还原性 | |
|
跟水反应 |
不能 |
能:CO2+H2O==H2CO3 | |
|
跟澄清石灰水反应 |
不能 |
CO2+Ca(OH)2==CaCO3↓+H2O | |
|
毒性 |
有毒 |
无毒 | |
|
主要用途 |
作气体燃料,用于高炉炼铁 |
灭火,人工降雨,干冰制冷剂等,作化工原料和温室肥料 | |
|
相互转化 |
C+O2 CO2 CO2C+CO2  2CO 2CO | ||
干冰:
一定条件下,二氧化碳气体会变成固体,固体二氧化碳叫“干冰”。干冰升华时,吸收大量的热,因此可作制冷剂。如果用飞机向云层中撤干冰,由于干冰升华吸热,空气中的水蒸气迅速冷凝变成水滴,就可以形成降雨。
二氧化碳不一定能灭火:
二氧化碳一般不支持燃烧,但在一定条件下,某些物质也可以在二氧化碳中燃烧,如将点燃的镁条伸入盛有二氧化碳的集气瓶中,镁条能继续燃烧,反应的化学方程式为:2Mg+CO2
 2MgO+C,所以活泼金属着火不能用二氧化碳来灭火
2MgO+C,所以活泼金属着火不能用二氧化碳来灭火 二氧化碳与一氧化碳的鉴别方法:
(1)澄清石灰水:将气体分别通入澄清石灰水中,能使澄清石灰水变浑浊的是二氧化碳,无明显现象的是一氧化碳。
(2)燃着的木条:将气体分别在空气中点燃,能燃烧的是一氧化碳,不能燃烧的是二氧化碳。
(3)紫色石蕊试液:将气体分别通入紫色石蕊试液中,能使石蕊试液变红的是二氧化碳,无明显现象的是一氧化碳。
(4)还原金属氧化物:将气体分别通过灼热的氧化铜,出现黑色粉末变红这一现象的是一氧化碳,没有明显现象的是二氧化碳。
二氧化碳与一氧化碳的除杂方法:
1.CO(CO2)(括号内的物质为杂质):通常将气体通人过量的碱溶液(一般用氢氧化钠溶液而不用澄清石灰水)中,二氧化碳与碱溶液反应,从而达到除杂的目的。
2.CO2(CO)(括号内的物质为杂质):通常将气体通过灼热的氧化铜,一氧化碳与氧化铜反应生成铜和二氧化碳,从而达到除杂的目的。不能用点燃的方法,因为CO2不支持燃烧,也不能燃烧。
二氧化碳与石灰石的应用:
二氧化碳与石灰水反应出现白色沉淀,反应的方程式为:CO2+Ca(OH)2==CaCO3↓+H2O。
该反应及现象有以下儿方面的应用:
(1)检验二氧化碳气体;
(2)鉴别NaOH溶液和澄清石灰水:将CO2气体通入待测溶液中,生成白色沉淀的溶液为澄清石灰水,无明显现象的为NaOH溶液;
(3)除去某些气体中的杂质:如除去CO中的CO2 气体,可将混合气体通过澄清石灰水;
(4)解释澄清石灰水为什么要密封保存:敞口放置的澄清石灰水会吸收空气中的CO2而使澄清石灰水表面生成一层白膜或变浑浊,其成分是CaCO3;
(5)用石灰砂浆砌砖抹墙不久后变白变硬:石灰砂浆的主要成分是Ca(OH)2,吸收空气中的CO2发生反应Ca(OH)2声称白色固体CaCO3固体。
(6)保存鸡蛋:将鸡蛋浸泡在澄清石灰水中,取出来后CO2与石灰水反应封闭鸡蛋壳上的小孔,可以延长鸡蛋的保存时间。
二氧化碳肥料:
二氧化碳是光合作用的原料之一,因而现在在温室大棚内种植蔬菜水果时,经常人为提高温室内CO2 浓度,以增加农作物产员,增大CO2浓度的方法通常有以下几种:
(1)在温室内放置干冰,干冰升华增大CO2浓度。
(2)在温室内放置通过化学反应产生CO2气体的物质,如在塑料大棚顶部的容器内放置石灰石和稀盐酸。
灯火实验:
(1)二氧化碳本身无毒,但它不供给呼吸,当空气中二氧化碳含量超过常量时,也会对人体健康产生不良影响。
| 空气中二氧化碳的体积分数/% | 对人体健康的影响 |
| 1 | 感到气闷,头昏,心悸 |
| 4—5 | 气喘,头痛,眩晕 |
| 10 | 神志不清,呼吸停止,死亡 |
跟酸或碱的溶液起作用而显示不同颜色的物质,叫酸碱指示剂,通常也简称指示剂。
紫色石蕊试液和无色酚酞试液的显色:
紫色石蕊试液和无色酚酞试液是两种常用的酸碱指示剂,它们与酸性、碱性溶液作用时显示的颜色见下表:
| 酸性溶液 | 碱性溶液 | 中性溶液 | |
| 石蕊试液 | 红 | 蓝 | 紫 |
| 酚酞试液 | 无 | 红 | 无 |
易错点:
①变色的是指示剂,而不是酸或碱的溶液。如盐酸使紫色石蕊试液变红,不能说成紫色石蕊试液使盐酸变红,但可以说紫色石蕊试液遇盐酸变红。
②酸或碱的溶液能使紫色石蕊试液或酚酞试液变色,但能使紫色石蕊试液或酚酞试液变色的不一定是酸或碱的溶液,还可能是酸性盐溶掖或碱性盐溶液。如碳酸钠溶液能使紫色石蕊试液变蓝,但碳酸钠不是碱,而是盐。
酸碱指示剂的代用品:
在自然界里,有许多植物色素在不同的酸碱性溶液中.都会发生特定的颜色变化。这些植物色素可以用作石蕊和酚酞等指示剂的代用品。一些植物的色素及其在酸碱性溶液中的颜色变化如下:
| 代用指示剂的颜色 | |||
| 在酸性溶液中 | 在中性溶液中 | 在碱性溶液中 | |
| 牵牛花 | 红色 | 紫色 | 蓝色 |
| 苏木 | 黄色 | 红棕色 | 玫瑰红色 |
| 紫萝卜皮 | 红色 | 紫色 | 黄绿色 |
| 月季花 | 浅红色 | 红色 | 黄色 |
| 美人蕉 | 淡红色 | 红色 | 绿色 |
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
1.钠保存在煤油中
2.NaOH溶液用橡胶塞
3.硝酸用玻璃塞棕色瓶
4.硝酸银用棕色瓶
5.白磷保存在水中
物质保存中需注意:
一、 防挥发:
1 .油封:氨水,浓盐酸,浓硝酸等易挥发无机液体,在液面上滴 10 ~ 20 滴矿物油,可以 防止挥发(不可用植物油)。
2 .水封:二硫化碳中加 5mL 水,便可长期保存。汞上加水,可防汞蒸气进入空气。汞旁放 些硫粉,一但失落,散布硫粉使遗汞消灭于化学反应中。
3 .腊封:乙醚、乙醇、甲酸等比水轻的或易溶性挥发液体,以及萘、碘等易挥发固体,紧 密瓶塞,瓶口涂腊。 溴除进行原瓶腊封外,应将原瓶置于具有活性炭的塑料筒内, 筒口进行 腊封。
二、防潮:
1 .漂白粉、过氧化钠应该进行腊封,防止吸水分解或吸水爆炸。氢氧化钠易吸水潮解,应 该进行腊封; 硝酸铵、 硫酸钠易吸水结状, 倒不出来, 以至导致试剂瓶破裂, 也应严密腊封。
2 .碳化钙、无水硫酸铜、五氧化二磷、硅胶极易吸水变质,红磷易被氧化,然后吸水生成 偏磷酸,以上各物均应存放在干燥器中。
3 .浓硫酸虽应密闭,防止吸水,但因常用,故宜放磨口瓶中,磨口瓶塞应该原配,切勿对调。
4 .“ 特殊药品 ” 的地下室,下层布块灰,中层布熟石灰上层布双层柏油纸,方可存放药物。
三、防变质:
1 .防氧化:亚硫酸钠、硫酸亚铁、硫代硫酸钠均易被氧化,瓶口应涂腊。
2 .防碳酸化:硅酸钠、过氧化钠、苛性碱均易吸收二氧化碳,应该涂腊。
3 .防风化:晶体碳酸钠、晶体硫酸铜应进行腊封,存放在地下室中。
4 .防分解:碳酸氢铵、浓硝酸受热易分解,涂腊后,存放在地下室中。
5 .活性炭能吸附多种气体而变质,(木炭亦同),应放在干燥器中。
6 .黄磷遇空气易自燃,永远保存水中,每 15 天查水一次:磷试剂瓶中加水、置于有水水 糟中,上加钟罩封闭。
7 .钾、钠保存在火油中。
8.硫酸亚铁溶液中滴几滴稀硫酸,加入过量细铁粉,进行腊封。
9 .葡萄糖溶液容易霉变,稍加几滴甲醛即可保存。
10 .甲醛易聚合,应开瓶后立即加少量甲醇;乙醛则加乙醇。
四、防光:
1 .硝酸银,浓硝酸及大部份有机药品应该放在棕色瓶中。
2 .硝酸盐存放在地下室中既防热,又防光、防火还能防震。
3 .有机试剂橱窗一律用黑漆涂染。
4 .实验室用色布窗帘,内红外黑双层。
五、防毒害:
1 .磷、硝酸银、氯酸钾、氯化汞等剧毒物放地下室内,双人双锁,建立档案,呈批取用, 使用记载,定期检查。
2 .磷化钙、磷化铝吸水后放出剧毒性磷化氢,应放在干燥器中保存,贴上红色标签。
3 .由于没有通风橱,经常在地面布石灰,吸附某些毒害气相物质。
4 .浓酸,浓碱、溴、酚等腐蚀的药物,使用红色标签,以示警戒。
六、防震:
1 .硝酸铵震动易爆炸,放地下室中。
2 .自制的大晶体明矾、大晶体硫酸铜,用软纸垫包放大口试剂瓶中,进行缓冲,并按 “ 四位 数字 ” 进行编号入厨。
与“向紫色石蕊溶液中通入二氧化碳,溶液变为______色,反应的方...”考查相似的试题有:
- 某科考小组在云南乌蒙山区发现了一种矿石,敲开表层发现里面有许多金黄发亮的晶体物质,酷似黄金,经检测其成分有黄铁矿(主要...
- 现有A、B、C、D、E、F、G、H、I九种常见物质,能发生如F反应:①A(溶液)+CuCl2(溶液)→B↓(蓝色)+C;②C(溶液)+D(溶液)...
- (1)图为2008年北京奥运会“金镶玉”等奖牌,6000枚奖牌所需黄金13.04吨、银1.34吨和电解铜6.93吨.据介绍,在金属奖牌内环和...
- 下列物质的用途与化学原理不相符合的是( )选项用途化学原理(用化学方程式表示)①红磷用于制烟幕弹4P+5O2 点燃 . 2P2O5②天...
- 完成下列反应的化学方程式,并注明反应类型(共15分)Cu-→CuO-→CuSO4-→Cu(OH)2-→CuSO4-→Cu①______;②______;③______;④__...
- 磷酸二氢铵[NH4H2PO4]是一种含有______、______两种营养元素的复合化肥,熟石灰常用来中和土壤的酸性,但是这两种物质不宜混...
- 下列有关二氧化碳的检验、制备和用途能达到目的是[ ]A.干冰用于人工降雨B.二氧化碳气体通入紫色石蕊试液中,溶液变蓝C.用...
- 把一张滤纸在某指示剂中浸泡后晾干,再用醮有氢氧化钠溶液的玻璃棒在上面画一朵花,花呈红色,再将该滤纸悬持挂于铁架台上,...
- 食醋、食盐、碱面、蔗糖、花生油、大米、矿泉水都是厨房常备物品.请选择物质填空:(1)市场上食盐的品种丰富,有碘盐、锌盐...
- 下列现象的出现只与空气中的水蒸气有关的是( )A.固体烧碱露置在空气中变质B.浓硫酸露置在空气中浓度会变稀C.铁制品在潮...
 2CO2
2CO2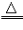 Cu+CO2
Cu+CO2