本试题 “下列实验描述正确的是[ ]A.在制备硝酸钾晶体实验中先常温减压过滤,后高温常压过滤B.在中和热测定的实验中,将氢氧化钠和盐酸混合反应后的最高温度作为末温...” 主要考查您对离子的检验
中和热的测定
原电池原理的探究实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 离子的检验
- 中和热的测定
- 原电池原理的探究实验
离子的检验:
(1)焰色反应:Na+:黄色;K+:紫色(透过蓝色钴玻璃观察);Ca2+:砖红色;
(2)H+:H+酸性。遇紫色石蕊试液变红,遇湿润蓝色石蕊试纸变红;
(3)NH4+:在试液中加强碱(NaOH)加热,产生使湿润红色石蕊试纸变蓝的气体;NH4++OH-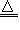 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O
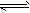 NH3?H2O
NH3?H2O NH4++OH-
NH4++OH-
(4)Fe3+:①通KSCN或NH4SCN溶液呈血红色:Fe3++SCN-==[Fe(SCN)]2+;②通NaOH溶液红褐色沉淀:Fe3++3OH-==
Fe(OH)3↓
(5)Fe2+:①遇NaOH溶液生成白色沉淀在空气中迅速转化成灰绿色最后变成红褐色沉淀:Fe3++2OH-=Fe(OH)2↓;
4Fe(OH)2+O2+2H2O==4Fe(OH)3;
②试液中加KSCN少量无明显变化再加氯水出现血红色: 2Fe2++Cl2==2Fe3++2Cl-;Fe3++SCN-==[Fe(SCN)]2+
(6)Mg2+:遇NaOH溶液有白色沉淀生成,NaOH过量沉淀不溶解:Mg2++2OH-==Mg(OH)2↓,但该沉淀能溶于NH4Cl溶液;
(7)Al3+:遇NaOH溶液(适量)有白色沉淀生成,NaOH溶液过量沉淀溶解:Al3++3OH-==Al(OH)3↓;Al(OH)3+OH-==
AlO2-+2H2O
(8)Cu2+:遇NaOH溶液有蓝色沉淀生成,加强热变黑色沉淀:Cu2++2OH-==Cu(OH)2↓;Cu(OH)2 CuO+H2O
CuO+H2O
(9)Ba2+:遇稀H2SO4或硫酸盐溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ba2++SO42-==BaSO4↓
(10)Ag+: ①加NaOH溶液生成白色沉淀,此沉淀迅速转变为棕色沉淀溶于氨水Ag++OH-==AgOH↓;2AgOH==Ag2O+H2O;AgOH+2NH3?H2O==[Ag(NO3)2]OH+2H2O
②加稀HCl或可溶性氧化物溶液再加稀HNO3生成白色沉淀:Ag++Cl-==AgCl↓
(11)OH-:OH-碱性:①遇紫色石蕊试液变蓝;②遇酚酞试液变红;③遇湿润红色石蕊试纸变蓝;
(12)Cl-:遇AgNO3溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ag++Cl-=AgCl↓
(13)Br-:加AgNO3溶液有浅黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++Br-=AgBr↓
(14)I-: ①加AgNO3溶液有黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++I-=AgI↓;②加少量新制氯水后再加淀粉溶液显蓝色:2I-+Cl2=I2+2Cl-;I2遇淀粉变蓝
(15)S2-:①加强酸(非强氧化性)生成无色臭鸡蛋气味气体:S2-+2H+=H2S↑;②遇Pb(NO3)2或(CH3COO)2Pb试液生成黑色沉淀,遇CuSO4试液产生黑色沉淀:Pb2++S2-=PbS↓;Cu2++S2-=CuS↓
(16)SO42-:加可溶性钡盐[BaCl2或Ba(NO3)2]溶液有白色沉淀生成后再加稀HCl或稀HNO3沉淀不溶解:Ba2++SO42-=BaSO4↓
(17)SO32-:加强酸(H2SO4或HCl)把产生气体通入品红溶液中,品红溶液褪色:SO32-+2H+=H2O+SO2↑ SO2使品红溶液褪色
(18)CO32-:加稀HCl产生气体通入澄清石灰水,石灰水变浑浊:CO32-+2H+=H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(19)HCO3-:取含HCO3-盐溶液煮沸,放出无色无味、使澄清石灰水变浑浊的气体;或向HCO3-溶液里加入稀MgSO4溶液,无现象,加热煮沸有白色沉淀MgCO3生成,同时放出CO2气体。
(20)NO3-:浓缩试液加稀硫酸和铜片加热有红棕色气体产生,溶液变成蓝色:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(21)PO43-:加AgNO3溶液产生黄色沉淀,再加稀HNO3沉淀溶解:3Ag++PO43-=Ag3PO4↓;Ag3PO4溶于稀HNO3酸。
(1)焰色反应:Na+:黄色;K+:紫色(透过蓝色钴玻璃观察);Ca2+:砖红色;
(2)H+:H+酸性。遇紫色石蕊试液变红,遇湿润蓝色石蕊试纸变红;
(3)NH4+:在试液中加强碱(NaOH)加热,产生使湿润红色石蕊试纸变蓝的气体;NH4++OH-
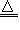 NH3↑+H2O;NH3+H2O
NH3↑+H2O;NH3+H2O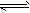 NH3?H2O
NH3?H2O NH4++OH-
NH4++OH- (4)Fe3+:①通KSCN或NH4SCN溶液呈血红色:Fe3++SCN-==[Fe(SCN)]2+;②通NaOH溶液红褐色沉淀:Fe3++3OH-==
Fe(OH)3↓
(5)Fe2+:①遇NaOH溶液生成白色沉淀在空气中迅速转化成灰绿色最后变成红褐色沉淀:Fe3++2OH-=Fe(OH)2↓;
4Fe(OH)2+O2+2H2O==4Fe(OH)3;
②试液中加KSCN少量无明显变化再加氯水出现血红色: 2Fe2++Cl2==2Fe3++2Cl-;Fe3++SCN-==[Fe(SCN)]2+
(6)Mg2+:遇NaOH溶液有白色沉淀生成,NaOH过量沉淀不溶解:Mg2++2OH-==Mg(OH)2↓,但该沉淀能溶于NH4Cl溶液;
(7)Al3+:遇NaOH溶液(适量)有白色沉淀生成,NaOH溶液过量沉淀溶解:Al3++3OH-==Al(OH)3↓;Al(OH)3+OH-==
AlO2-+2H2O
(8)Cu2+:遇NaOH溶液有蓝色沉淀生成,加强热变黑色沉淀:Cu2++2OH-==Cu(OH)2↓;Cu(OH)2
 CuO+H2O
CuO+H2O (9)Ba2+:遇稀H2SO4或硫酸盐溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ba2++SO42-==BaSO4↓
(10)Ag+: ①加NaOH溶液生成白色沉淀,此沉淀迅速转变为棕色沉淀溶于氨水Ag++OH-==AgOH↓;2AgOH==Ag2O+H2O;AgOH+2NH3?H2O==[Ag(NO3)2]OH+2H2O
②加稀HCl或可溶性氧化物溶液再加稀HNO3生成白色沉淀:Ag++Cl-==AgCl↓
(11)OH-:OH-碱性:①遇紫色石蕊试液变蓝;②遇酚酞试液变红;③遇湿润红色石蕊试纸变蓝;
(12)Cl-:遇AgNO3溶液有白色沉淀生成,加稀HNO3沉淀不溶解:Ag++Cl-=AgCl↓
(13)Br-:加AgNO3溶液有浅黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++Br-=AgBr↓
(14)I-: ①加AgNO3溶液有黄色沉淀生成,加稀HNO3沉淀不溶解:Ag++I-=AgI↓;②加少量新制氯水后再加淀粉溶液显蓝色:2I-+Cl2=I2+2Cl-;I2遇淀粉变蓝
(15)S2-:①加强酸(非强氧化性)生成无色臭鸡蛋气味气体:S2-+2H+=H2S↑;②遇Pb(NO3)2或(CH3COO)2Pb试液生成黑色沉淀,遇CuSO4试液产生黑色沉淀:Pb2++S2-=PbS↓;Cu2++S2-=CuS↓
(16)SO42-:加可溶性钡盐[BaCl2或Ba(NO3)2]溶液有白色沉淀生成后再加稀HCl或稀HNO3沉淀不溶解:Ba2++SO42-=BaSO4↓
(17)SO32-:加强酸(H2SO4或HCl)把产生气体通入品红溶液中,品红溶液褪色:SO32-+2H+=H2O+SO2↑ SO2使品红溶液褪色
(18)CO32-:加稀HCl产生气体通入澄清石灰水,石灰水变浑浊:CO32-+2H+=H2O+CO2↑;CO2+Ca(OH)2=CaCO3↓+H2O
(19)HCO3-:取含HCO3-盐溶液煮沸,放出无色无味、使澄清石灰水变浑浊的气体;或向HCO3-溶液里加入稀MgSO4溶液,无现象,加热煮沸有白色沉淀MgCO3生成,同时放出CO2气体。
(20)NO3-:浓缩试液加稀硫酸和铜片加热有红棕色气体产生,溶液变成蓝色:
Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
(21)PO43-:加AgNO3溶液产生黄色沉淀,再加稀HNO3沉淀溶解:3Ag++PO43-=Ag3PO4↓;Ag3PO4溶于稀HNO3酸。
中和热测定:
(1)目的:①用量热法测定HCl与NaOH的中和热。②了解化学标定法,并掌握其操作。
(2)原理:在298K、溶液足够稀的情况下,1molOH-与1molH+中和,可放出57.3.kJ的热量。即:H+(aq)+OH-(aq) =H2O(aq) △H=-57.3kJ/mol
(3)仪器和实验:大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50mL)两个、泡沫塑料或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。0.50 mol/L 盐酸、0.55 mol/L NaOH溶液。
(4)步骤:
①在大烧杯底垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如图所示。该实验也可在保温杯中进行。
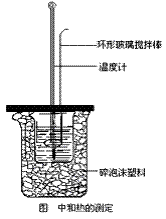
②用一个量筒量取50mL0.50mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
③用另一个量筒量取50mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
④把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
⑤重复实验两次,取测量所得数据的平均值作为计算依据。
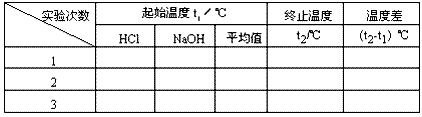
⑥根据实验数据计算中和热。
(1)目的:①用量热法测定HCl与NaOH的中和热。②了解化学标定法,并掌握其操作。
(2)原理:在298K、溶液足够稀的情况下,1molOH-与1molH+中和,可放出57.3.kJ的热量。即:H+(aq)+OH-(aq) =H2O(aq) △H=-57.3kJ/mol
(3)仪器和实验:大烧杯(500 mL)、小烧杯(100 mL)、温度计、量筒(50mL)两个、泡沫塑料或纸条、泡沫塑料板或硬纸板(中心有两个小孔)、环形玻璃搅拌棒。0.50 mol/L 盐酸、0.55 mol/L NaOH溶液。
(4)步骤:
①在大烧杯底垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平。然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过,以达到保温、隔热、减少实验过程中热量损失的目的,如图所示。该实验也可在保温杯中进行。

②用一个量筒量取50mL0.50mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记入下表。然后把温度计上的酸用水冲洗干净。
③用另一个量筒量取50mL 0.55 mol/L NaOH溶液,并用温度计测量NaOH溶液的温度,记入下表。
④把温度计和环形玻璃搅拌棒放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度,记为终止温度,记入下表。
⑤重复实验两次,取测量所得数据的平均值作为计算依据。

⑥根据实验数据计算中和热。
原电池原理的探究实验:
(1)通过设计实验的方式探究原电池的形成条件:①负极为较活泼金属;正极为较不活泼金属、石墨等②电极需要插入电解质溶液中③必需形成闭合回路
(2)工作原理:负极发生氧化反应;正极发生还原反应;电子流向:负极 正极
正极
探究过程:
(1)提出问题:化学反应伴随有能量的变化,化学能能否转变为电能呢?哪些反应能将化学能转变为电能?化学能是怎样转化为电能的呢?化学能转化为电能的基本原理是什么?
思考结果:电流形成原因:电子的定向移动(负极失电子,化合价升高,正极得电子,化合价降低)
(2)猜想与假设:原电池构成须有两个电极、导线、电解质溶液,氧化还原反应与电极和导线之间须构成闭合回路。
思考结果:电子由负极流向正极,电流由正极流向负极
(3)制定计划:用Zn片、Cu片、稀H2SO4和导线来做实验探究原电池的工作原理,具体步骤见进行实验一栏。
思考结果:1.连接导线前,锌片上有气泡,铜片上无气泡;连接导线后,锌片上气泡减少,铜片上出现比较多的气泡。 2.电流计的指针有一些偏转。
(4)进行实验
实验1.将Zn片插入稀H2SO4中,观察现象并解释原因。
实验2.将Cu片插入稀H2SO4中,观察现象并解释原因。
实验3.取锌片和铜片同时插入装有稀H2SO4的烧杯中,观察现象。
实验4.用导线将插入稀H2SO4中的锌片和铜片连接起来,观察现象。
思考结果:4个实验中实验1有气泡产生,实验2没有明显现象,实验3中铜片上没有明显现象,实验4中大量气泡在铜片上产生,锌片逐渐溶解。
(5)收集证据:在导线间接入一个电流计来验证猜想与假设是否正确。
思考结果:1.形成了以铜,锌为电极,稀硫酸为电解液的原电池。 2.锌是电子流出方,为负极;铜片为正极。
(6)解释与结论:可以从电流计上看到,电流的方向是由铜片流向锌片。电子带负电荷,其流向与电流流向相反,因此,电子的流向是由锌片经导线流向铜片的。把原电池失去电子一极叫负极,得到电子一极叫正极。电子流向是通过原电池的负极流向正极,较活泼金属失去电子,发生氧化反应,氧化剂从正极得到电子,发生还原反应。这两个反应均是在电极上进行的,我们称之为“电极反应”。
思考结果:原电池的构成条件:第一,必须有电极。电极材料可以是活泼性不同的金属或者是金属与非金属构成。较活泼的金属为负极,较不活泼的金属或非金属为正极。第二,必须有电解质溶液,第三,要有导线,形成闭合回路。
(7)反思与评价:原电池形成的条件:1.形成闭合回路;2.溶液中有自由移动的离子;3.不同活泼性的电极,能发生自发的氧化还原反应学习原电池的工作原理和构成条件,其有利于生活,比如利用原电池原理来制备各种各样的电池。还能利用所学知识来解释生活中常见的一些现象,例如钢铁的腐蚀。
(1)通过设计实验的方式探究原电池的形成条件:①负极为较活泼金属;正极为较不活泼金属、石墨等②电极需要插入电解质溶液中③必需形成闭合回路
(2)工作原理:负极发生氧化反应;正极发生还原反应;电子流向:负极
 正极
正极 探究过程:
(1)提出问题:化学反应伴随有能量的变化,化学能能否转变为电能呢?哪些反应能将化学能转变为电能?化学能是怎样转化为电能的呢?化学能转化为电能的基本原理是什么?
思考结果:电流形成原因:电子的定向移动(负极失电子,化合价升高,正极得电子,化合价降低)
(2)猜想与假设:原电池构成须有两个电极、导线、电解质溶液,氧化还原反应与电极和导线之间须构成闭合回路。
思考结果:电子由负极流向正极,电流由正极流向负极
(3)制定计划:用Zn片、Cu片、稀H2SO4和导线来做实验探究原电池的工作原理,具体步骤见进行实验一栏。
思考结果:1.连接导线前,锌片上有气泡,铜片上无气泡;连接导线后,锌片上气泡减少,铜片上出现比较多的气泡。 2.电流计的指针有一些偏转。
(4)进行实验
实验1.将Zn片插入稀H2SO4中,观察现象并解释原因。
实验2.将Cu片插入稀H2SO4中,观察现象并解释原因。
实验3.取锌片和铜片同时插入装有稀H2SO4的烧杯中,观察现象。
实验4.用导线将插入稀H2SO4中的锌片和铜片连接起来,观察现象。
思考结果:4个实验中实验1有气泡产生,实验2没有明显现象,实验3中铜片上没有明显现象,实验4中大量气泡在铜片上产生,锌片逐渐溶解。
(5)收集证据:在导线间接入一个电流计来验证猜想与假设是否正确。
思考结果:1.形成了以铜,锌为电极,稀硫酸为电解液的原电池。 2.锌是电子流出方,为负极;铜片为正极。
(6)解释与结论:可以从电流计上看到,电流的方向是由铜片流向锌片。电子带负电荷,其流向与电流流向相反,因此,电子的流向是由锌片经导线流向铜片的。把原电池失去电子一极叫负极,得到电子一极叫正极。电子流向是通过原电池的负极流向正极,较活泼金属失去电子,发生氧化反应,氧化剂从正极得到电子,发生还原反应。这两个反应均是在电极上进行的,我们称之为“电极反应”。
思考结果:原电池的构成条件:第一,必须有电极。电极材料可以是活泼性不同的金属或者是金属与非金属构成。较活泼的金属为负极,较不活泼的金属或非金属为正极。第二,必须有电解质溶液,第三,要有导线,形成闭合回路。
(7)反思与评价:原电池形成的条件:1.形成闭合回路;2.溶液中有自由移动的离子;3.不同活泼性的电极,能发生自发的氧化还原反应学习原电池的工作原理和构成条件,其有利于生活,比如利用原电池原理来制备各种各样的电池。还能利用所学知识来解释生活中常见的一些现象,例如钢铁的腐蚀。
发现相似题
与“下列实验描述正确的是[ ]A.在制备硝酸钾晶体实验中先常温减...”考查相似的试题有:
- 某待测溶液中可能含有Fe2+、Fe3+、Al3+、Ag+、Ba2+、、Ca2+等,进行以下实验(所加酸、碱、氨水、溴水都是过量的)。根据实验...
- 有一包白色固体粉末,其中可能含有Ba(NO3)2、CaCl2、K2CO3,现做以下实验:①将部分粉末加入水中,振荡,有白色沉淀生成。②向①...
- 某无色混合气体可能由CH4、NH3、H2、CO、CO2和HCl中的某几种气体组成。在恒温、恒压的条件下,将此混合气体通过浓硫酸时,总...
- 下图是部分被污损的某白色固体药品标签。为探究其成分,取样滴入适量盐酸,无气泡产生。则该固体A.一定是NaClB.一定是NaNO3...
- 下列对进行焰色反应实验操作注意事项的说明正确的是①要透过蓝色的钴玻璃观察钾的火焰颜色 ②先把铂丝烧到与原来火焰颜色相同,...
- 有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,为了确定溶液中所含离子及其...
- 对溶液中的离子进行鉴定,下列实验所得结论不合理的是[ ]A.溶液中加入稀硝酸后,再加入AgNO3溶液,有白色沉淀生成,则溶液中...
- 能用分液漏斗分离的混合物是( )A.液溴和四氯化碳B.乙醇和乙酸C.氯化钙和碳酸钠溶液D.苯和蒸馏水
- 某溶液中含有SO42-、CO32、OH-三种阴离子,如果只取一次该溶液,分别将三种离子检验出来,则检验顺序是:(1)先检验______离...
- Ⅰ、某小组同学将一定浓度NaHCO3溶液加入到CuSO4溶液中发现生成了沉淀。甲同学认为沉淀是CuCO3,乙同学认为沉淀是CuCO3和Cu(OH...