本试题 “某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如下的实验装置。(1)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:_...” 主要考查您对氯水
二氧化硫
设计实验方案及探究实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯水
- 二氧化硫
- 设计实验方案及探究实验
氯水的成分:
新制氯水中存在的分子有盐酸(HCl)、次氯酸(HClO),水(H2O)、还有氯气
氯水的性质:
新制氯水呈黄绿色、有刺激性气味,属于混合物,其所含的多种微粒使氯水的化学性质表现出多重性。
①氯水的Cl2氧化性,只表现氯水的氧化性
A. 在某些含非金属阴离子的溶液中加氯水。
| 氯水滴加溶液 | 反应方程式 | 实验现象 |
| KI溶液 | 2KI+Cl2==2KCl+I2 | 溶液由无色变橙黄色 |
| NaBr溶液 | 2NaBr+Cl2==NaCl+Br2 | 溶液由无色变橙色 |
| K2S溶液 | K2S+Cl2==2KCl+S↓ | 溶液变浑浊 |
| Na2SO3溶液 | Na2SO3+Cl2+H2O==Na2SO4+2HCl | 氯水颜色褪去 |
C. 某些强还原性的气体通入氯水中,氯气将其氧化。
| 通入的气体 | 化学方程式 | 实验现象 |
| H2S | H2S+Cl2==2HCl+S↓ | 溶液出现浑浊 |
| HBr | 2HBr+Cl2==2HCl+Br2 | 溶液由浅黄绿色变橙色 |
| HI | 2HI+Cl2==2HCl+I2 | 溶液由浅黄色变橙黄色 |
| SO2 | SO2+Cl2+2H2O==H2SO4+2HCl | 溶液浅黄色褪去 |
A. 新制氯水滴入NaOH溶液等强碱溶液中,氯水褪色:
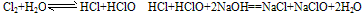
B. 新制氯水中滴加紫色石蕊试液时,溶液先变红色,后褪色,是盐酸的强酸性和次氯酸的强氧化性共同作用的结果。 ③氯水中次氯酸的强氧化性。
新制氯水起漂白作用时,是由于HClO的强氧化性将色素氧化使之褪色的结果,也是Cl2的漂白、杀菌、消毒作用必须有水存在的根本原因。
④氯水中盐酸的强酸性。
在AgNO3溶液中滴加适量的氯水,有白色沉淀生成。是氯水中的HCl与AgNO3作用的结果。
⑤氯水中盐酸的强酸性和氯气的强氧化性共同起作用。
向氯水中加镁粉、铝粉等活泼金属时,可观察到氯水颜色褪去且有气泡冒出,氯水中的Cl2和HCl与镁、铝共同作用的结果。
有关氯水问题的分析方法:
1.氯水性质的多样性
氯气溶于水形成的溶液叫氯水,新制的氯水呈浅黄绿色,有刺激性气味。氯水中存在三个平衡:
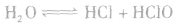 ,
,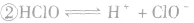 ,
,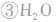
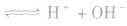 。所以,在氯水中存在三种分子:Cl2、 H2O、HClO;四种离子:H+、Cl-、ClO-及少量OH-。由于在光照条件下HClO可分解
。所以,在氯水中存在三种分子:Cl2、 H2O、HClO;四种离子:H+、Cl-、ClO-及少量OH-。由于在光照条件下HClO可分解
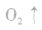 ,故久置的氯水为盐酸。
,故久置的氯水为盐酸。
(1)氯水的性质氯水在与不同物质发生反应时,表现出成分的复杂性和性质的多样性。
说明:
①氯水通常现用现制,可短时间密封保存于棕色试剂瓶中(见光或受热易分解的物质均保存在棕色试剂瓶中);
②Cl:使湿润的蓝色石蕊试纸先变红,后褪色。
(2)新制氯水、久置氯水、液氯的区别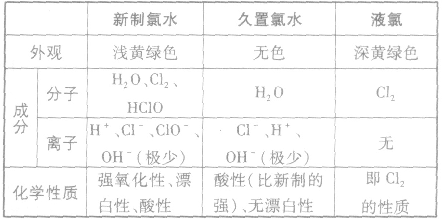
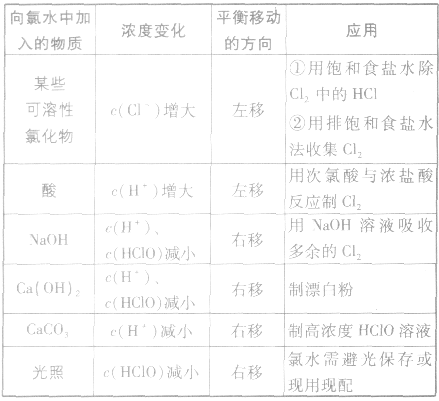
外界因素对平衡 的影响:
的影响:
卤离子的检验方法:
1.银盐法:
特别提醒:加入稀HNO3的目的是防止CO32-、 PO43-等离子的干扰。有关反应为: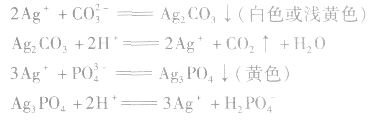
2.置换一萃取法
3.置换一淀粉法检验I-
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液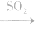 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


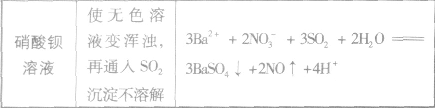
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表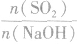 ,如下数轴所示:
,如下数轴所示: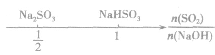
分析数轴可得:
(1)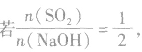 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)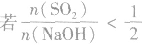 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)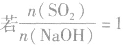 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)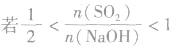 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)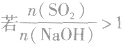 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
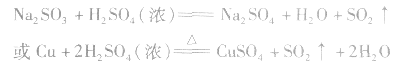
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

化学实验方案的设计:
1.概念:化学实验方案的设计是在实施化学实验之前.根据化学实验的目的和要求,运用相关的化学知识和技能,对实验的仪器、装置和方法所进行的一种规划。
2.实验方案设计的基本要求
(1)科学性:实验原理、实验操作程序和方法必须科学合理。
(2)安全性:尽量避免使用有毒药品和进行有一定危险性的实验操作,保护人身安全,保护仪器。
(3)可行性:实验所选用的药品、仪器、设备和方法等在中学现有条件下能满足要求。
(4)简约性:方案简单易行,尽可能采用简单的实验装置,较少的实验步骤和药品。还应遵循完成实验所用时间较短,副反应少,效果好等基本要求。
(5)经济性:综合考虑原料的用量和价格。
3.化学实验设计的基本内容一个相对完整的化学实验方案一般包括下述内容:
(1)实验名称;
(2)实验目的;
(3)实验原理;
(4)实验用品(药品、仪器、装置、设备)及规格;
(5)实验装置图、实验步骤和操作方法;
(6)实验注意事项;
(7)实验现象的记录及结果处理;
(8)问题与讨论。
4.化学实验方案设计的基本思路 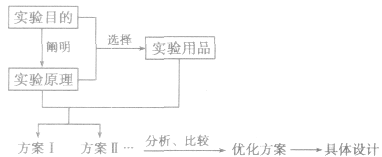
(1)明确目的、原理首先必须认真审题,明确实验的目的,弄清题目有哪些新的信息,结合已学过的知识,通过类比、迁移、分析,从而明确实验原理。
(2)选择仪器、药品根据实验的目的和原理,以及反应物和生成物的性质、反应条件(如反应物和生成物的状态、能否腐蚀仪器、反应是否需要加热及温度是否需要控制在一定的范围内等),合理选择化学仪器和药品。
(3)设汁装置、步骤根据实验目的和原理,以及所选用的仪器和药品,设计出合理的实验装置和实验操作步骤。学生应具备识别和绘制典型的实验仪器装置图的能力,实验步骤应既完整又简明。
(4)记录现象、数据根据观察,全面而准确地记录实验过程中的现象和数据。
(5)分析得出结论根据实验观察到的现象和记录的数据,通过分析、计算、图表、推理等,得出正确的结论。
化学实验方案设计的分类:
1.物质性质实验方案的设计研究物质性质的基本方法:观察法、实验法、分类法、比较法等。研究物质性质的基本程序:观察外观性质一预测物质性质一实验和观察一解释及结论。图示如下:
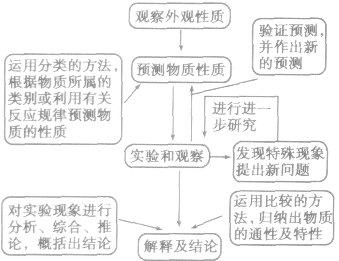
在进行性质实验方案的设计时,要充分了解物质的结构、性质、用途与制法之间的相互关系,要根据物质的结构特点,设计化学实验方案来探究或验证物质所具有的一些性质:
2.物质制备实验方案的设计
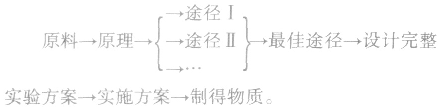
制备实验方案的设计,应遵循以下原则
(1)条件合适,操作简便;
(2)原理正确,步骤简单;
(3)原料丰富,价格低廉;
(4)产物纯净,污染物少。制备实验方案的设计,主要涉及原料、基本化学反应原理,实验程序和仪器、设备。核心是原料,由原料可确定反应原理,推导出实验步骤及所用仪器。
3.物质检验实验方案的设计

通过特定的反应现象,推断被检验物质是否存在。在对物质进行检验或鉴别时,一般的原则是:
①给出n 种物质进行鉴别,一般只需检验n一1种即可;
②物理和化学方法可并用,一般先用物理方法(如物质的颜色、气味、水溶性等),再用化学方法;
③设计的实验步骤越简单越好,实验现象越明显越好;
④有干扰离子存在时,应先排除干扰,以免得出错误的结论;
⑤进行检验的一般步骤为:观察外表一一加热固体(确定是否有结晶水)——配成溶液——观察外观一一加入试剂——观察现象——得出结论。
化学实验方案的评价:
对几个实验方案的正确与错误、严密与不严密、准确与不准确作出判断,要考虑是否合理、有无干扰现象、经济上是否合算和对环境有无污染等。
1.从可行性方面对实验方案作出评价科学性和可行性是设计实验方案的两条重要原则,在对实验方案进行评价时,要分析实验方案是否科学可行,实验方案是否遵循化学理论和实验方法的要求,在实际操作时能否做到可控易行。评价时,可从以下4个方面分析:
(1)实验原理是否正确、可行;
(2)实验操作是否安全、合理;
(3)实验步骤是否简单、方便;
(4)实验现象是否明显。
2.从“绿色化学”视角对实验方案作出评价 “绿色化学”要求设计安全的、对环境友好的合成线路,降低化学工业生产过程对人类健康和环境的危害,减少废弃物的产生和排放。据此,对化学实验过程或方案从以下4个方面进行综合评价:
(1)反应原料是否易得、安全、无毒;
(2)反应速率是否适巾;
(3)原料利用率以及合成物质的产率是否较高;
(4)合成过程中是否造成环境污染。
3.从安全性方面对实验方案作出评价从安全角度常考虑的主要因素如下:
(1)净化、吸收气体及熄灭酒精灯时要防止液体倒吸;
(2)使用某些易燃易爆品进行实验时要防爆炸(如 H2还原CuO应先通H2可燃性气体点燃前先验纯等);
(3)防氧化(如H2还原CuO后要“先灭灯再停氢”,白磷切割宜在水中进行等);
(4)防吸水(如实验取用、制取易吸水、潮解、水解的物质时宜采取必要措施,以保证达到实验目的);
(5)冷凝回流(有些反应中,为减少易挥发液体反应物的损耗和充分利用原料,需在反应装置上加装冷凝回流装置,如长玻璃管、竖装的干燥管及冷凝管等);
(6)易挥发液体产物(导出时可为蒸气)的及时冷却;
(7)仪器拆卸的科学性与安全性(可从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑);
(8)其他(如实验操作顺序、试剂加入顺序等)。
与“某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了...”考查相似的试题有:
- 在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质。下列实验现象和结论一致且正确的是[ ]A.向氯水中加入有色...
- 汽车已经成为重要的交通工具,但其排放的尾气是空气的主要污染物之一。已知汽车尾气中的主要污染物有:CmHn(烃)、SO2、NOx、C...
- 木炭与浓硫酸在加热条件下发生反应:C+2H2SO4(浓)CO2↑+2SO2↑+2H2O↑,下图虚线框中的装置可用来检验该反应产生的所有气体产物...
- 下列有关物质性质和用途的描述不符合事实的是A.有机物不导电 B.金刚石是自然界最硬的物质C.SO2可用作食品防腐剂D.NO可用...
- 酸雨形成的主要原因是( )A.汽车排放的大量尾气B.生产硫酸工厂排放的尾气C.工业上大量含硫燃料的燃烧D.乱砍滥伐,破坏了...
- 某研究性学习小组做铜与浓硫酸反应实验时,发现试管底部有白色固体并夹杂有少量黑色物质。倒去试管中的浓硫酸,将剩余固体(含...
- 下列说法正确的是 ( )A.浓硝酸和浓硫酸露置于空气中,容器内酸液的浓度都降低B.可用铁制容器储存稀硝酸C.SO2溶于水生成H...
- 关于浓H2SO4的性质说法错误的是( )A.浓H2SO4的脱水性属物理性质,相应的变化过程是物理变化B.蓝色石蕊试纸遇H2SO4先变红后...
- 重铬酸钾(K2Cr2O7)是工业生产和实验室的重要氧化剂.实验室模拟工业生产重铬酸钾时用铬铁矿(主要成份为FeO•Cr2O3)、纯碱...
- 为证明有关物质的性质,某学生设计了如图装置,当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛慢...