本试题 “下表中实验操作能达到实验目的是( )实验操作实验目的A向丙烯醛中滴加酸性高锰酸钾溶液,振荡后观察溶液是否褪色确定丙烯醛中是否含有碳碳双键B向混有少量苯...” 主要考查您对有机物的官能团
物质的除杂
实验操作达到的预期目的
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 有机物的官能团
- 物质的除杂
- 实验操作达到的预期目的
官能团:
定有机物化学特性的原子或原子团。常见的官能团:碳碳双键、碳碳三键、羟基、醛基、羧基、酯基、羰基、苯基、-X(卤素)、氨基。
定有机物化学特性的原子或原子团。常见的官能团:碳碳双键、碳碳三键、羟基、醛基、羧基、酯基、羰基、苯基、-X(卤素)、氨基。
根、基和官能团的区别:
1.根带电的原子团,如OH-电子式为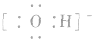 )、
)、  等。
等。
2.基电中性,不能单独存在,一般用“一R”表示烃基,其中的“一”表示一个电子,如甲基(一CH3),电子式为 常见的基有乙基(
常见的基有乙基(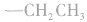 )、乙烯基 H (
)、乙烯基 H ( )、苯基(
)、苯基(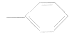 )、羟基(一OH)、硝基(
)、羟基(一OH)、硝基(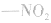 )等。
)等。
3. OH一与一OH、一COOH两种官能团的比较
除杂的原则:
(1)不增:不增加新的杂质
(2)不减:被提纯的物质不能减少
(3)易分:操作简便,易于分离
气体除杂的原则:
(1)不引入新的杂质
(2)不减少被净化气体的量注意的问题:
①需净化的气体中含有多种杂质时,除杂顺序:一般先除去酸性气体,如:氯化氢气体,CO2、SO2等,水蒸气要在最后除去。
②除杂选用方法时要保证杂质完全除掉,如:除CO2最好用NaOH不用Ca(OH)2溶液,因为Ca(OH)2是微溶物,石灰水中Ca(OH)2浓度小,吸收CO2不易完全。
方法:
A. 杂质转化法:欲除去苯中的苯酚,可加入氢氧化钠,使苯酚转化为苯酚钠,利用苯酚钠易溶于水,使之与苯分开
B. 吸收洗涤法;欲除去二氧化碳中混有的少量氯化氢和水,可使混合气体先通过饱和碳酸氢钠溶液,再通过浓硫酸即可除去
C. 沉淀过滤法:欲除去硫酸亚铁溶液中混有的少量硫酸铜,加入少量铁粉,待充分反应后,过滤除去不溶物即可
D. 加热升华法:欲除去碘中的沙子,即可用此法
E. 溶液萃取法:欲除去水中含有的少量溴,可采用此法
F. 结晶和重结晶:欲除去硝酸钠溶液中少量的氯化钠,可利用二者的溶解度不同,降低溶液温度,使硝酸钠结晶析出,可得到纯硝酸钠晶体
G. 分馏蒸馏法:欲除去乙醚中少量的酒精,可采用多次蒸馏的方法
H. 分液法:欲将密度不同且又互不相溶的液体混合物分离,可采用此法,如将苯和水分离
K. 渗析法:欲除去胶体中的离子,可采用此法。如除去氢氧化钠胶体中的氯离子
常见物质除杂总结:
原物所含杂质除杂质试剂除杂质的方法
(1)N2(O2)-------灼热的铜丝网洗气
(2)CO2(H2S)-------硫酸铜溶液洗气
(3)CO(CO2)-------石灰水或烧碱液洗气
(4)CO2(HCl)-------饱和小苏打溶液洗气
(5)H2S(HCl)-------饱和NaHS溶液洗气
(6)SO2(HCl)-------饱和NaHSO3溶液洗气
(7)Cl2(HCl)-------饱和NaCl溶液洗气
(8)CO2(SO2)-------饱和小苏打溶液洗气
(9)碳粉(MnO2)-------浓盐酸加热后过滤
(10)MnO2(碳粉)-------加热灼烧
(11)碳粉(CuO)-------盐酸或硫酸过滤
(12)Al2O3(Fe2O3)-------NaOH溶液(过量),再通CO2过滤、加热固体
(13)Fe2O3(Al2O3)-------NaOH溶液过滤
(14)Al2O3(SiO2)-------盐酸NH3·H2O过滤、加热固体
(15)SiO2(ZnO)-------盐酸过滤
(16)CuO(ZnO)-------NaOH溶液过滤
(17)BaSO4(BaCO3)-------稀硫酸过滤
(18)NaOH(Na2CO3)-------Ba(OH)2溶液(适量)过滤
(19)NaHCO3(Na2CO3)-------通入过量CO2
(20)Na2CO3(NaHCO3)-------加热
(21)NaCl(NaHCO3)-------盐酸蒸发结晶
(22)NH4Cl[(NH4)2SO4]-------BaCl2溶液(适量)过滤
(23)FeCl3(FeCl2)-------通入过量Cl2
(24)FeCl3(CuCl2)-------铁粉、Cl2过滤
(25)FeCl2(FeCl3)-------铁粉过滤
(26)Fe(OH)3胶体(FeCl3)-------(半透膜)渗析
(27)CuS(FeS)-------稀盐酸或稀硫酸过滤
(28)I2(NaCl)------升华
(29)NaCl(NH4Cl)-------加热
(30)KNO3(NaCl)-------蒸馏水重结晶
(31)乙烯(SO2、H2O)碱石灰洗气
(32)乙烷(乙烯)-------溴水洗气
(33)溴苯(溴)-------稀NaOH溶液分液
(34)硝基苯(NO2)-------稀NaOH溶液分液
(35)甲苯(苯酚)-------NaOH溶液分液
(36)乙醛(乙酸)-------饱和Na2CO3溶液蒸馏
(37)乙醇(水)-------新制生石灰蒸馏
(38)苯酚(苯)-------NaOH溶液、CO2分液
(39)乙酸乙酯(乙酸)-------饱和Na2CO3溶液分液
(40)溴乙烷(乙醇)-------蒸馏水分液
(41)肥皂(甘油)-------食盐过滤
(42)葡萄糖(淀粉)-------(半透膜)渗析
(1)不增:不增加新的杂质
(2)不减:被提纯的物质不能减少
(3)易分:操作简便,易于分离
气体除杂的原则:
(1)不引入新的杂质
(2)不减少被净化气体的量注意的问题:
①需净化的气体中含有多种杂质时,除杂顺序:一般先除去酸性气体,如:氯化氢气体,CO2、SO2等,水蒸气要在最后除去。
②除杂选用方法时要保证杂质完全除掉,如:除CO2最好用NaOH不用Ca(OH)2溶液,因为Ca(OH)2是微溶物,石灰水中Ca(OH)2浓度小,吸收CO2不易完全。
方法:
A. 杂质转化法:欲除去苯中的苯酚,可加入氢氧化钠,使苯酚转化为苯酚钠,利用苯酚钠易溶于水,使之与苯分开
B. 吸收洗涤法;欲除去二氧化碳中混有的少量氯化氢和水,可使混合气体先通过饱和碳酸氢钠溶液,再通过浓硫酸即可除去
C. 沉淀过滤法:欲除去硫酸亚铁溶液中混有的少量硫酸铜,加入少量铁粉,待充分反应后,过滤除去不溶物即可
D. 加热升华法:欲除去碘中的沙子,即可用此法
E. 溶液萃取法:欲除去水中含有的少量溴,可采用此法
F. 结晶和重结晶:欲除去硝酸钠溶液中少量的氯化钠,可利用二者的溶解度不同,降低溶液温度,使硝酸钠结晶析出,可得到纯硝酸钠晶体
G. 分馏蒸馏法:欲除去乙醚中少量的酒精,可采用多次蒸馏的方法
H. 分液法:欲将密度不同且又互不相溶的液体混合物分离,可采用此法,如将苯和水分离
K. 渗析法:欲除去胶体中的离子,可采用此法。如除去氢氧化钠胶体中的氯离子
常见物质除杂总结:
原物所含杂质除杂质试剂除杂质的方法
(1)N2(O2)-------灼热的铜丝网洗气
(2)CO2(H2S)-------硫酸铜溶液洗气
(3)CO(CO2)-------石灰水或烧碱液洗气
(4)CO2(HCl)-------饱和小苏打溶液洗气
(5)H2S(HCl)-------饱和NaHS溶液洗气
(6)SO2(HCl)-------饱和NaHSO3溶液洗气
(7)Cl2(HCl)-------饱和NaCl溶液洗气
(8)CO2(SO2)-------饱和小苏打溶液洗气
(9)碳粉(MnO2)-------浓盐酸加热后过滤
(10)MnO2(碳粉)-------加热灼烧
(11)碳粉(CuO)-------盐酸或硫酸过滤
(12)Al2O3(Fe2O3)-------NaOH溶液(过量),再通CO2过滤、加热固体
(13)Fe2O3(Al2O3)-------NaOH溶液过滤
(14)Al2O3(SiO2)-------盐酸NH3·H2O过滤、加热固体
(15)SiO2(ZnO)-------盐酸过滤
(16)CuO(ZnO)-------NaOH溶液过滤
(17)BaSO4(BaCO3)-------稀硫酸过滤
(18)NaOH(Na2CO3)-------Ba(OH)2溶液(适量)过滤
(19)NaHCO3(Na2CO3)-------通入过量CO2
(20)Na2CO3(NaHCO3)-------加热
(21)NaCl(NaHCO3)-------盐酸蒸发结晶
(22)NH4Cl[(NH4)2SO4]-------BaCl2溶液(适量)过滤
(23)FeCl3(FeCl2)-------通入过量Cl2
(24)FeCl3(CuCl2)-------铁粉、Cl2过滤
(25)FeCl2(FeCl3)-------铁粉过滤
(26)Fe(OH)3胶体(FeCl3)-------(半透膜)渗析
(27)CuS(FeS)-------稀盐酸或稀硫酸过滤
(28)I2(NaCl)------升华
(29)NaCl(NH4Cl)-------加热
(30)KNO3(NaCl)-------蒸馏水重结晶
(31)乙烯(SO2、H2O)碱石灰洗气
(32)乙烷(乙烯)-------溴水洗气
(33)溴苯(溴)-------稀NaOH溶液分液
(34)硝基苯(NO2)-------稀NaOH溶液分液
(35)甲苯(苯酚)-------NaOH溶液分液
(36)乙醛(乙酸)-------饱和Na2CO3溶液蒸馏
(37)乙醇(水)-------新制生石灰蒸馏
(38)苯酚(苯)-------NaOH溶液、CO2分液
(39)乙酸乙酯(乙酸)-------饱和Na2CO3溶液分液
(40)溴乙烷(乙醇)-------蒸馏水分液
(41)肥皂(甘油)-------食盐过滤
(42)葡萄糖(淀粉)-------(半透膜)渗析
实验操作达到的预期目的:
(1)①用托盘天平称取5.6g氧化铜粉末(托盘天平能准确到0.1克,所以用托盘天平称取5.6g氧化铜粉末是可以的)
②用10mL水和10mL酒精配制成20mL酒精溶液(由于分子间有间隔,10mL水和10mL静静混合后体积,不能配制成20mL酒精溶液)
③用排水集气法可收集到比较纯净的氧气(收集到的气体要比排空气法收集到的气体纯,由于空气的密度与氧气的密度相差不是很大,所以排空气法收集到的气体氧气不是很纯)
④用10mL量筒量取8.2mL水(10mL量筒精确到0.1mL,所以能量取8.2mL水)
(2) ①分别加入饱和碳酸钠溶液,鉴别乙酸乙酯和乙酸(观察到有气泡产生的是乙酸,能到到鉴别的目的)
②分别加入少量金属钠,比较水和乙醇中羟基氢的活泼性(通过观察与金属钠反应的剧烈程度可以判断羟基的活泼性,能达到目的)
③分别加入浓硝酸,比较铁和铜的金属活动性(铁和铜都能和浓硝酸反应,不能达到比较金属活动性的目的)
(1)①用托盘天平称取5.6g氧化铜粉末(托盘天平能准确到0.1克,所以用托盘天平称取5.6g氧化铜粉末是可以的)
②用10mL水和10mL酒精配制成20mL酒精溶液(由于分子间有间隔,10mL水和10mL静静混合后体积,不能配制成20mL酒精溶液)
③用排水集气法可收集到比较纯净的氧气(收集到的气体要比排空气法收集到的气体纯,由于空气的密度与氧气的密度相差不是很大,所以排空气法收集到的气体氧气不是很纯)
④用10mL量筒量取8.2mL水(10mL量筒精确到0.1mL,所以能量取8.2mL水)
(2) ①分别加入饱和碳酸钠溶液,鉴别乙酸乙酯和乙酸(观察到有气泡产生的是乙酸,能到到鉴别的目的)
②分别加入少量金属钠,比较水和乙醇中羟基氢的活泼性(通过观察与金属钠反应的剧烈程度可以判断羟基的活泼性,能达到目的)
③分别加入浓硝酸,比较铁和铜的金属活动性(铁和铜都能和浓硝酸反应,不能达到比较金属活动性的目的)
发现相似题
与“下表中实验操作能达到实验目的是( )实验操作实验目的A向丙...”考查相似的试题有:
- 下列有机化学反应方程式错误的是A.B.CH3COOH + CH3CH2OHCH3COOCH2CH3C.D.2CH3CH2OH + O22CH3CHO + 2H2O
- 下列关于有机化合物的说法正确的组合是 ①乙醛可发生银镜反应,说明其还原性较强②乙烯可以与氢气发生加成反应,苯不能与氢气加...
- 下列关于有机物的说法正确的是( )A.乙烯和苯都能使溴水褪色,褪色的原因相同B.淀粉、蛋白质完全水解的产物互为同分异构体C...
- 下列实验能达到预期目的是( )A.除去SO2气体中少量HCl2通过盛有饱和Na2SO3溶液的洗气瓶吸收后收集气体B.用溴水除去苯中的...
- 下列说法不正确的是[ ]A.铁管道与直流电源负极相连,防止铁管道腐蚀B.小苏打、氢氧化铝可用于治疗胃酸过多C.工业生产中,...
- NaCl固体中混有下列杂质时,可以利用加热的方法进行提纯的是[ ]A.KClO3B.K2SO4C.NH4ClD.NaHCO3
- 下列实验方案合理的是[ ]A.用通入酸性高锰酸钾溶液的方法除去乙烯中混有的二氧化硫B.用加入浓溴水的方法分离苯和苯酚的混合...
- 下列说法正确的是[ ]A.久置的浓HNO3呈黄色,为除去黄色可通入O2B.在常温下,将氯化铝溶液蒸发结晶,最后能得到氯化铝晶体C...
- 下列有关说法正确的是( )A.检验溶液中是否含SO42-时,在无其它阳离子干扰时,所加的BaCl2溶液用盐酸酸化B.为提高高锰酸钾...
- 下列实验或操作合理的是( )A.只有一个合理B.只有两个合理C.只有三个合理D.都不合理