本试题 “某混合溶液中含有0.2molNa+,0.25molMg2+,0.4Cl-,则SO42-的物质的量为( ) A.0.1mol B.0.3mol C.0.5mol D.0.15mol” 主要考查您对强电解质电离(氯化钠、硫酸氢钠等物质的电离)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 强电解质电离(氯化钠、硫酸氢钠等物质的电离)
强电解质电离:
强电解质在溶液中完全电离,且符号为“=”,如NaCl=Na++Cl-、NaHSO4==Na++H++SO42-
强电解质在溶液中完全电离,且符号为“=”,如NaCl=Na++Cl-、NaHSO4==Na++H++SO42-
酸与碱反应的几种情况:
1.等体积、等物质的量浓度的酸 混合
混合 
2.等体积的酸 混合
混合 
3.若酸 等体积混合溶液呈中性
等体积混合溶液呈中性 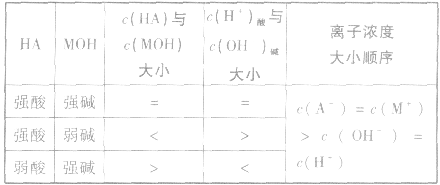
4.强酸溶液(pH=a)与强碱溶液(pH=b)完全中和时的体积比

发现相似题
与“某混合溶液中含有0.2molNa+,0.25molMg2+,0.4Cl-,则SO42-的...”考查相似的试题有:
- 下列物质中含有自由移动Cl-的是( )A.KClO3固体B.Cl2C.HCl气体D.KCl溶液
- 常温下,对下列四种溶液的叙述正确的是[ ]A.②、③两溶液相比,溶液中水的电离程度不同B.四种溶液分别加水稀释10倍,pH变化最...
- 某溶液由NaCl、MgCl2、Al2(SO4)3、Na2SO4组成,已知CNa+=0.4mol/L,CAl3+=0.2mol/LC Mg2+=0.1mol/L,CCl-=0.3mol/L则SO42-...
- 浓度均为0.1mol/L的8种溶液:①HNO3②H2SO4③CH3COOH ④Ba(OH)2⑤NaOH ⑥CH3COONa ⑦KCl ⑧NH4Cl其溶液的PH由小到大的顺序是_________...
- Ⅰ选择下列实验方法分离物质,将分离方法的序号填在横线上.A.萃取 B.分液 C.过滤 D.加热分解 E.蒸发 F.蒸馏(1)分离饱...
- 某学生用下列溶质配制一种混合溶液,已知溶液中c(Na+)=2c(SO42-)=2c(K+)=2c(Cl-),则溶质可能是( ) A.KCl、Na2SO4...
- 某盐的溶液中含有Na+、Mg2+、Cl-、SO42-四种离子,若Na+为0.2mol,Mg2+为0.4mol,Cl-为0.4mol,则SO42-物质的量为( )A.0.1...
- 醋酸和盐酸是高中化学中常见的两种酸,下列说法正确的是( )A.物质的量浓度相同的盐酸和醋酸溶液中的H+浓度也相同B.相同浓...
- 硼酸晶体呈片状,有滑腻感,可做润滑剂.硼酸对人体的受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面.试回答下...
- 下列图示及其解释错误的是[ ]A.图①表示NaCl在水中溶解和电离的示意图B.图②表示碳酸氢根离子水解示意图C.符合图③的电离方程...