本试题 “下列说法正确的是[ ]A.常温下0.4 mol/L HB溶液和0.2 mol/L NaOH溶液等体积混合后溶液的pH=3,则混合溶液中离子浓度的大小顺序为:c(Na+)>c(B-)>c(H+...” 主要考查您对水电离的影响因素
粒子浓度大小的比较
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水电离的影响因素
- 粒子浓度大小的比较
影响水电离平衡的因素:
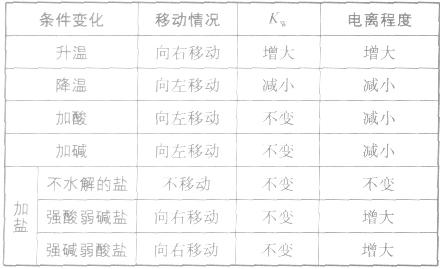
离子浓度大小比较方法:
(1)考虑水解因素:如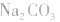 溶液
溶液 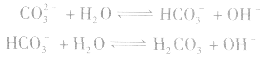
所以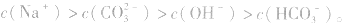
(2)不同溶液中同一离子浓度的比较要看溶液中其他离子对它的影响。如相同浓度的
 三种溶液中,
三种溶液中, 由大到小的顺序是c>a>b。
由大到小的顺序是c>a>b。
(3)混合液中各离子浓度的比较要综合分析水解因素、电离因素。如相同浓度的 的混合液中,离子浓度顺序为:
的混合液中,离子浓度顺序为: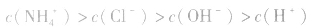
 的电离程度大于
的电离程度大于 的水解程度。
的水解程度。
盐溶液的“三大守恒”:
①电荷守恒:电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。如NaHCO3溶液中:
推出: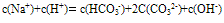
②物料守恒:电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。如NaHCO3溶液中nc(Na+):nc(C)=1:1,
推出: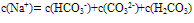
③质子守恒:电解质溶液中分子或离子得到或失去质子(H+)的物质的量应相等。例如在NH4HCO3溶液中H3O+、H2CO3为得到质子后的产物;NH3、OH-、CO32-为失去质子后的产物,故有以下关系: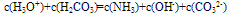
(2)粒子浓度大小比较的方法:
①单一溶液中离子浓度大小的比较
A. 一元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)>c(水电离出的另一离子)
如:在CH3COONa溶液中各离子浓度大小关系: 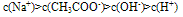
B. 二元弱酸盐溶液中离子浓度的关系是:
c(不水解离子)>c(水解离子)>c(显性离子)> c(二级水解离子)>c(水电离出的另一离子)
如:Na2CO3溶液中离子浓度的关系: 
②比较不同电解质溶液中同一种粒子浓度的大小。应注意弱酸、弱碱电离程度的大小以及影响电离度的因素,盐类水解及水解程度对该粒子浓度的影响。
③比较经过反应化学反应后离子浓度的大小:
A. 确定电解质溶液的成分
B. 确定溶液中含哪些粒子(分子、离子),此时要考虑物质的电离和水解情况
C. 确定各种粒子的浓度或物质的量的大小
D. 根据题目要求做出判断
注:要抓住“两小”。即弱电解质电离程度小,故未电离的弱电解质分子数远多于已电离出离子数目;盐的水解程度小,故未水解的粒子数目远多于水解生成的粒子数目
与“下列说法正确的是[ ]A.常温下0.4 mol/L HB溶液和0.2 mol/L...”考查相似的试题有:
- (8分)水的电离平衡曲线如下图所示。(1)若以A点表示25℃时水在电离平衡时的离子浓度,当温度升到100℃时,水的电离平衡状态...
- 若以w1和w2分别表示浓度为c1mol/L和c2mol/L硫酸的质量分数,已知2w1=w2,则下列推断正确的是(硫酸的密度比纯水的大)A.2c1...
- 下列叙述正确的是( )A.95℃纯水的pH
- 常温时,将pH为5的HCl溶液与pH为2的HCl溶液等体积混合后,溶液的氢氧根离子浓度最接近于 ( )A.2×10-12mol/LB.1/2(10-9+1...
- 常温下,若使pH=3的盐酸与pH=9的Ba(0H)2溶液混合使其成为pH=7的溶液,混合时两溶液的体积比为( )。A.1:60B.3:1C.100:lD...
- 关于浓度均为0.1mol•L-1的三种溶液:①CH3COOH、②NaOH、③CH3COONa溶液,下列说法不正确的是( )A.c(CH3COO-):③>①B.水电...
- 将PH = 1的盐酸平均分成2份,1份加适量水,另一份加入与盐酸物质的量浓度相等的NaOH溶液后,PH均变成了2,则加入的水与NaOH溶...
- (2009·重庆理综)物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )A.Ba(OH)2、Na2SO3、FeCl3、KClB.Na2SiO3、Na2CO3...
- (1)①pH= a的CH3COOH溶液稀释100倍后所得溶液pH a +2(填“>”或“<”)②0.01mol/LCH3COOH溶液的pH 2(填“>”或“<”);③0.1mo...
- 常温下,0.1mol/L的一元酸HA溶液其pH>1,而0.1mol/L的一元碱BOH的溶液中c(OH-)/c(H+)=1012,将此两种溶液等体积混合后,...