本试题 “(1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:①反应中观察到的现象是______.②该实验设计的特点有______.③待发生燃烧反应的试管冷却后,小明...” 主要考查您对验证物质燃烧的条件
物质组成元素的质量分数
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 验证物质燃烧的条件
- 物质组成元素的质量分数
定义:
燃烧是一种发光、发热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
燃烧条件的探究实验:
1. 实验方案
2. 实验结论:
燃烧必须同时具备:
①可燃物
②氧气(空气)
③达到燃烧所需的最低温度(着火点)
1. 着火点:可燃物燃烧所需的最低温度叫着火点,是物质固有的一种性质,与物质本身的性质有关,一般不随外界条件的改变而改变。
在通常状况下一些常见物质的着火点
2. 探究燃烧条件的实验设计方法
燃烧必须同时具备: ①可燃物 ②氧气(空气) ③达到燃烧所需的最低温度(着火点)。中考试题往往以实验设计题的形式来考查燃烧规律。燃烧条件的探究设计常常运用控制变量—对比法。
(1)分析对比实验设计

实验1:探究可燃物才能燃烧
实验2:探究可燃物接触氧气才能燃烧
实验3:探究达到着火点可燃物才能燃烧
(2)综合控制变量
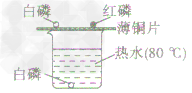
①把白磷和红磷都漏置在空气中(对比),用0℃的热水控制温度(这个温度高于白磷的着火点,低于红磷的着火点),白磷能燃烧,红磷不能燃烧,证明可燃物与氧气接触,且可燃物还必须达到着火点才能燃烧。
②烧杯底部放一块白磷,用水控制不让白磷与空气接触,温度仍然是80℃,与铜片上的白磷对比,证明可燃物即使温度达到着火点,如果不与氧气接触也不能燃烧。
燃烧是一种发光、发热的剧烈的化学反应。认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的。
燃烧条件的探究实验:
1. 实验方案
| 实验方案 | 实验现象 | 分析 |
分别将一小块白磷和一小块红磷放在薄铜片上,另取一小块白磷放入热水中,如下图: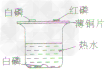 |
①薄铜片上:白磷燃烧,产生大量白烟,红磷没有变化 ②热水中,白磷没有燃烧 |
①白磷、红磷都是可燃物.薄铜片上的白磷与O2接触,同时温度达到白磷的着火点,故白磷能够燃烧 ②薄铜片上的红磷与O2 接触,但温度没有达到其着火点,热水中的白磷温度达到了其着火点.但没有与O2接触,所以红磷和水中的白磷都不能燃烧 |
2. 实验结论:
燃烧必须同时具备:
①可燃物
②氧气(空气)
③达到燃烧所需的最低温度(着火点)
1. 着火点:可燃物燃烧所需的最低温度叫着火点,是物质固有的一种性质,与物质本身的性质有关,一般不随外界条件的改变而改变。
在通常状况下一些常见物质的着火点
| 物质 | 白磷 | 红磷 | 木材 | 木炭 | 无烟煤 |
| 着火点/℃ | 40 | 240 | 250-330 | 320-370 | 700-750 |
燃烧必须同时具备: ①可燃物 ②氧气(空气) ③达到燃烧所需的最低温度(着火点)。中考试题往往以实验设计题的形式来考查燃烧规律。燃烧条件的探究设计常常运用控制变量—对比法。
(1)分析对比实验设计

实验1:探究可燃物才能燃烧
实验2:探究可燃物接触氧气才能燃烧
实验3:探究达到着火点可燃物才能燃烧
(2)综合控制变量

①把白磷和红磷都漏置在空气中(对比),用0℃的热水控制温度(这个温度高于白磷的着火点,低于红磷的着火点),白磷能燃烧,红磷不能燃烧,证明可燃物与氧气接触,且可燃物还必须达到着火点才能燃烧。
②烧杯底部放一块白磷,用水控制不让白磷与空气接触,温度仍然是80℃,与铜片上的白磷对比,证明可燃物即使温度达到着火点,如果不与氧气接触也不能燃烧。
定义:
物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=
如AmBn中A元素的质量分数=
若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=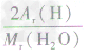 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成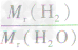 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%
化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例: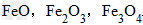 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
解析:三种含铁的氧化物的化学式可变形为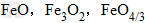 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: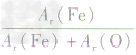 、
、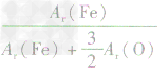 、
、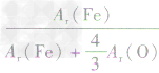 ,通过比较分母可知:
,通过比较分母可知: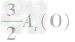 >
>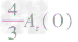 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。
物质中某元素的质量分数,就是该元素的质量与组成物质的各元素总质量之比。
公式:
某元素的质量分数=

如AmBn中A元素的质量分数=

若题目给出物质的化学式,又同时知道物质的实际质量,则可根据物质的质量×某元素的质量分数=该元素的质量,将其中所含元素的质量求出。同理,物质的质量=某元素质量÷该元素的质量分数。
公式的理解:
计算时应先列式计算,然后代入数据算出结果。如水中氢元素的质量分数=
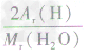 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%而不能写成
×100%=11.1%而不能写成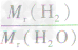 ×100%=
×100%= ×100%=
×100%= ×100%=11.1%
×100%=11.1%化学式中质量分数的应用:
①已知物质的质量求所含的某元素的质量
利用公式:元素的质量=物质的质量×该元素的质量分数
②已知元素的质量求物质的质量
利用公式:物质的质量=元素的质量÷该元素的质量分数
③根据元素的质量分数确定物质的化学式
利用化学式的变形比较元素质量分数的大小:
例:
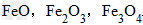 三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?
三种铁的氧化物按铁元素的质量分数由大到小排列的顺序为?解析:三种含铁的氧化物的化学式可变形为
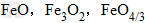 ,则三种含铁的氧化物中铁元素的质量分数分别为:
,则三种含铁的氧化物中铁元素的质量分数分别为: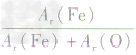 、
、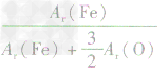 、
、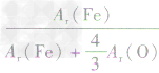 ,通过比较分母可知:
,通过比较分母可知: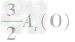 >
>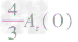 >Ar(O),故铁元素的质量分数由大到小排列的顺序为
>Ar(O),故铁元素的质量分数由大到小排列的顺序为 。
。 发现相似题
与“(1)如图为某学生设计的探究可燃物燃烧条件的实验,请回答:...”考查相似的试题有:
- 化学与生活紧密相连。下列做法不正确的是 A.生活中可用肥皂水鉴别硬水和软水B.夜间发现家中液化石油泄,立即开灯查明泄原因...
- 下列有关化学知识应用的叙述正确的是A.用催化剂可以将水变成汽油B.用过滤的方法把硬水变成软水C.用洗涤剂可以除去餐具上的...
- 联合国第63届大会确定2011年为“国际化学年”,以纪念化学学科对人类文明作出的巨大贡献,其主题是“化学--我们的生活,我们的未...
- 上海“11?15”特别重大火灾事故发生,震惊全中国,它警示人们要时刻注意安全。下列几种消防安全标志中属于易燃物的是 ( )
- 曾害得许多人家破人亡的海洛因是我国政府明令严禁的毒品,其组成可表示为C12H22O11.下列说法正确的是[ ]A.海洛因分子由碳、...
- 二氧化氯(ClO2)是一种重要的消毒剂。二氧化氯中氯元素、氧元素的质量比为 ,135g二氧化氯中氧元素的质量是 。
- “世界无烟日”的主题是“清洁空气、拒吸二手烟”.香烟燃烧产生的烟气中含有尼古丁(化学式为C10H14N2)、焦油、一氧化碳.下列...
- 已知尿素的化学式为CO(NH2)2,则:(1)尿素中碳元素的质量分数为______(2)人尿中氮元素的质量分数为0.91%,若假设人尿中...
- 2011年11月3日,“神舟八号”和“天宫一号”成功交会对接,被网友称为“太空之吻”,标志着 我国是世界上第三个完全独立掌握该交会...
- “瘦肉精” 学名盐酸克伦特罗, 化学式为C12H18Cl2N2O,食用含有“瘦肉精”的肉会对人体产生危害。下列关于瘦肉精说法正确的是[ ]A...