本试题 “〔1〕原子得到或失去电子后形成离子.某粒子的结构示意图为a= _________时该粒子是原子、当a=8时,该粒子符号为_________;〔2〕请用化学用语表示:空气中含...” 主要考查您对空气的成分
原子结构示意图
离子符号的意义及写法
离子结构示意图
化合价的写法和意义
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 空气的成分
- 原子结构示意图
- 离子符号的意义及写法
- 离子结构示意图
- 化合价的写法和意义
空气的成分:
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
概念:
原子结构示意图(如图)是表示原子核电荷数和电子层排布的图示形式。小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
原子结构示意图及各部分的含义:
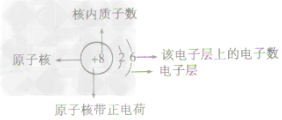
前20号元素的原子结构示意图:
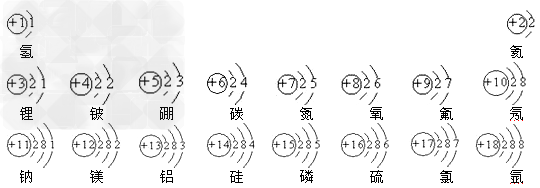
原子结构示意图(如图)是表示原子核电荷数和电子层排布的图示形式。小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。
原子结构示意图及各部分的含义:

前20号元素的原子结构示意图:

离子的定义:
带电的原子或原子团叫离子。
离子的分类:
阳离子:带正电荷的原子或原子团,如:K+、NH4+
阴离子:带负电荷的原子或原子团,如:Cl-、SO42-。
离子的形成(以Na+、Cl-的形成为例) :
①钠在氯气中燃烧生成氯化钠:2Na+Cl2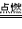 2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)

②从原子结构示意图分析Na+,Cl-的形成过程:

离子的表示方法——离子符号
在元素符号的右上角用“+”,“-”号表示离子的电性,数字表示离子所带的电荷,先写数字后写正负号,当数字为1 时,省略不谢。如Na+,Cl-,Mg2+,O2-。
原子团:
①有一些物质如Ca(OH)2,CaCO3等,它们中的一些原子集团如OH-、CO32-,常作为一个整体参加反应,这样的原子集团,叫做原子团,又叫做根。
②命名:原子团不能独立稳定地存在,它是物质 “分子”组成的一部分。
初中化学中的原子团除铵根 (NH4+)在化学式前面部分外,其他原子团在化学式的后一部分一般命名“xx根”,
如下面画线部分为原子团: NH4Cl(铵根)Na2CO3(碳酸根)K2SO4(硫酸根)NaOH(氢氧根)KNO3(硝酸根)KMnO4(高锰酸根)K2MnO4(锰酸根)KClO3(氯酸根) NH4NO3(铵根,硝酸根)
其他原子团有:SO32-(亚硫酸根)、NO2-(亚硝酸根),HSO3-(亚硫酸氢根),H2PO4-(磷酸二氢根)等。
关系式:
阳离子所带正电荷数=原子失去电子数=质子数-核外电子数
阴离子所带负电荷数=原子得到电子数=核外电子数-质子数
带电的原子或原子团叫离子。
离子的分类:
阳离子:带正电荷的原子或原子团,如:K+、NH4+
阴离子:带负电荷的原子或原子团,如:Cl-、SO42-。
离子的形成(以Na+、Cl-的形成为例) :
①钠在氯气中燃烧生成氯化钠:2Na+Cl2
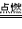 2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
2NaCl。钠与氯气反应时,每个钠原子失去1个电子形成钠离子(Na+),每个氯原子得到1个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成化合物氯化钠(NaCl)
②从原子结构示意图分析Na+,Cl-的形成过程:

离子的表示方法——离子符号
在元素符号的右上角用“+”,“-”号表示离子的电性,数字表示离子所带的电荷,先写数字后写正负号,当数字为1 时,省略不谢。如Na+,Cl-,Mg2+,O2-。
原子团:
①有一些物质如Ca(OH)2,CaCO3等,它们中的一些原子集团如OH-、CO32-,常作为一个整体参加反应,这样的原子集团,叫做原子团,又叫做根。
②命名:原子团不能独立稳定地存在,它是物质 “分子”组成的一部分。
初中化学中的原子团除铵根 (NH4+)在化学式前面部分外,其他原子团在化学式的后一部分一般命名“xx根”,
如下面画线部分为原子团: NH4Cl(铵根)Na2CO3(碳酸根)K2SO4(硫酸根)NaOH(氢氧根)KNO3(硝酸根)KMnO4(高锰酸根)K2MnO4(锰酸根)KClO3(氯酸根) NH4NO3(铵根,硝酸根)
其他原子团有:SO32-(亚硫酸根)、NO2-(亚硝酸根),HSO3-(亚硫酸氢根),H2PO4-(磷酸二氢根)等。
关系式:
阳离子所带正电荷数=原子失去电子数=质子数-核外电子数
阴离子所带负电荷数=原子得到电子数=核外电子数-质子数
概念:
离子结构示意图是用来表示离子核电荷数和电子排布的图示.同种元素的原子和离子其质子数相同.离子的核外电子数和质子数不同,阳离子的质子数大于核电荷数,阴离子的质子数小于核外电子数.主族元素的离子最外层一般为8个电子(最外层是K层为2个电子)。
阴阳离子的结构示意图与原子结构示意图的的区别:
1、结构示意图中,圆圈里的数字=半弧上的数字之和,它就是原子结构示意图。
2、结构示意图中,圆圈里的数字>半弧上的数字之和,它就是阳离子结构示意图。
3、结构示意图中,圆圈里的数字<半弧上的数字之和,它就是阴离子结构示意图。
离子结构示意图是用来表示离子核电荷数和电子排布的图示.同种元素的原子和离子其质子数相同.离子的核外电子数和质子数不同,阳离子的质子数大于核电荷数,阴离子的质子数小于核外电子数.主族元素的离子最外层一般为8个电子(最外层是K层为2个电子)。
阴阳离子的结构示意图与原子结构示意图的的区别:
1、结构示意图中,圆圈里的数字=半弧上的数字之和,它就是原子结构示意图。
2、结构示意图中,圆圈里的数字>半弧上的数字之和,它就是阳离子结构示意图。
3、结构示意图中,圆圈里的数字<半弧上的数字之和,它就是阴离子结构示意图。
化合价的定义:
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如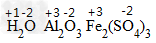 .
.
化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
一些常见元素和根的化合价:
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
一种元素一定数目的原子跟其他元素一定数目的原子相化合的性质,叫做这种元素的化合价。化合价有正价、负价之分,如在H2O中,氢原子与氧原子的个数比为2:1,H为+1价,0为-2价;在MgCl2中,镁原子与氯原子的个数比为1:2,Mg为+2价,Cl为-1价。
化合价的意义:
化合价反映元素的原子之间相互化合时的数日,是元素的一种性质。因此,强调化合价时,一定要指明元素。
化合价的表示方法:
通常在元素符一号或原子团的正上方用+n或-n表示,“+”“-”在前,数值在后。“1”不能省略。例如
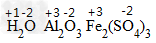 .
.化合价的一般规律:
(1)化合价有正价和负价;
(2)金属元素跟非金属元素化合时,金属元素显正价,非金属元素显负价,如MgCl2中Mg为+2价,Cl为-1价;非金属元素和氧元素形成化合物时,非金属元素通常显正价,氧元素通常显-2价,如SO2中S为+4价,O为-2价;
(3)一些元素在不同物质中可显不同的化合价,如KMnO4、K2MnO4中锰元素的化合价分别为+7,+6价;
(4)化合物中,各元素正、负化合价代数和为0;
(5)因为化合价是元素的原子在形成化合物时才表现出来的一种性质,所以单质中元素的化合价为0;
(6)原子团不能独立存在,只是化合物的一个组成部分,所以原子团的化合价由各元素的正、负化合价的代数和算出,原子团的化合价一定不为0。
化合价与最外层电子数的关系:
(1)金属元素的化合价数值一般等于它的最外层电子数。
(2)非金属元素的最高正价数值等于它的最外层电子数(O、F除外),最低负价数值等于8减去最外层电子数。
化合价符号与离子符号的比较
| 元素化合价的符号 | 离子符号 | |
| 概念不同 | 表示元素原子所显化合价的数值和正负的符号 | 表示带电原子(或原子团)所带电荷的电性核电荷量的符号 |
| 位置不同 | 化合价写在元素符号或原子团的正上方 | 所带电荷写在元素符合(或原子团)的右上角。 |
| 前后不同 | 正负号在前,数字在后 | 数字在前,正负号在后 |
| 省略不同 | 化合价为+1或-1价时,数字1不能省略 | 带一个单位正电荷或负电荷时,“1”不能省略不写 |
一些常见元素和根的化合价:
| 元素和根的名称 | 元素和根的符号 | 常见的化合价 | 元素和根的名称 | 元素和根的符号 | 常见的化合价 |
| 钾 | K | +1 | 氯 | Cl | -1、+1、+5、+7 |
| 钠 | Na | +1 | 溴 | Br | -1 |
| 银 | Ag | +1 | 氧 | O | -2 |
| 钙 | Ca | +2 | 硫 | S | -2、+4、+6 |
| 镁 | Mg | +2 | 碳 | C | +2、+4 |
| 钡 | Ba | +2 | 硅 | Si | +4 |
| 铜 | Cu | +1、+2 | 氮 | N | -3、+2、+3、+4、+5 |
| 铁 | Fe | +2、+3 | 磷 | P | -3、+3、+5 |
| 铝 | Al | +3 | 氢氧根 | OH- | -1 |
| 锰 | Mn | +2、+4、+6、+7 | 硝酸根 | NO3- | -1 |
| 锌 | Zn | +2 | 硫酸根 | SO42- | -2 |
| 氢 | H | +1 | 碳酸根 | CO32- | -2 |
| 氟 | F | -1 | 铵根 | NH4+ | +1 |
记忆口诀:
常见元素的化合价口诀
(1)一价钾、钠、银、氢、氟,二价钙、镁、钡和锌,铝价正三氧负二,以上价态要记真。铜一二来铁二三,碳硅二四要记全,硫显负二正四六,负三正五氮和磷,氯价最常显负一,还有正价一五七,锰显正价二四六,最高价数也是七。
(2)常见原子团的化合价口诀
一价铵根氢氧根,另有硝酸氯酸根。二价硫酸碳酸根,勿忘一个锰酸根。三价只有磷酸根。除了铵根皆为负,常写常用能记住。
发现相似题
与“〔1〕原子得到或失去电子后形成离子.某粒子的结构示意图为a=...”考查相似的试题有:
- 取两块干燥的玻璃片,对着其中一块呼气,观察玻璃片上水珠的情况,并与另一块放在空气中的玻璃片作对比,得出人体呼出的气体...
- 用物质的化学式填空:(1)最理想的气体燃料是______;(2)容易导致酸雨形成的气体是______;(3)能与人体中血红蛋白结合的...
- 空气中含量最多,化学性质又不活泼的气体是[ ]A. 氧气B. 氮气C. 水蒸气D. 二氧化碳
- M元素的一种微粒的结构示意图为(1)当M为原子时X=______,化学性质______(填稳定或不稳定),(2)M元素的单质是空气的重要...
- 某元素的原子结构示意图为,该元素原子核内有______个质子,其-2价阴离子最外层上有______个电子。该元素的单质在一定条件下...
- 下图是有关氧气的知识网络图(反应条件部分省略), 用化学用语回答:(1)物质①的化学式是 ;(2)物质②的阳离子是 ;(3)物质③带...
- 将元素、分子、原子、离子、质子、中子或电子填入下列有关空格内.(1)化学变化中的最小粒子是 ____.(2)Na和Na+属于同一...
- (1)某元素的原子结构示意图为 ,该元原子核内有_______个质子,最外电子层上有___________个电子。(2)用符号表示:2个氢气...
- “用微观的眼光看世界”是我们学习化学的重要思想方法。试根据以下材料,结合你所学过的知识,简要回答:材料一:一滴水里大约...
- 元素周期表是学习化学的重要工具,下表是元素周期表的一部分.请回答下列问题:1H2He3Li4Be5B6C7N8O9F10Ne11Na12Mg13Al14Si15...