本试题 “下列说法你认为不正确的是( )A.实验室从苯酚中分离出苯的过程中,可选用如图装置及操作B.化学反应中原子可重新组合、也可以破裂,爆炸过程中不一定伴随着...” 主要考查您对化学反应和物理变化
合成有机高分子化合物
物质的分离
合成氨(人工固氮)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应和物理变化
- 合成有机高分子化合物
- 物质的分离
- 合成氨(人工固氮)
化学变化:在化学反应中,分子破裂成原子,原子重新排列组合生成新物质的过程,称为化学反应。在反应中常伴有发光发热变色生成沉淀物等现象。
物理变化:在物理变化中没有新物质生成,一般只是物质的形状或状态发生变化。
物质变化对比:
| 物理变化 | 化学变化 | |
| 特征 | 没有新物质生成 | 有新物质生成 |
| 实质 | 构成物质的粒子间隔发生变化,物质的组成、结构没有变化,无新物质生成 | 物质的组成、结构发生变化,物质中原子重新组合,有新物质生成 |
| 关系 | 化学变化中一定有物理变化,但物理变化中一定没有化学变化 | |
(1)化学变化中常伴随着发光、发热和颜色变化,但有发光、发热或颜色变化的变化不一定是化学变化,如在常压下将氧气冷却到-184℃时,O2变成淡蓝色的液体。
(2)原子的裂变、聚变中虽有新物质形成,但它不属于中学化学变化研究的范畴。
化学反应的实质:
判断一个反应是否为化学反应的依据是反应是否生成新的物质。化学反应的实质是旧键的断裂和新键的形成。
合成有机高分子化合物:
由千百个原子彼此以共价键结合形成相对分子质量特别大、具有重复结构单元的有机化合物。是由一类相对分子质量很高的分子聚集而成的化合物,也称为高分子、大分子等。一般把相对分子质量高于10000的分子称为高分子。包括天然和合成有机高分子化合物。常见合成有机高分子化合物:聚乙烯、聚氯乙烯等
有机高分子化合物的合成:
高分子化合物大部分是由小分子通过聚合反应制得的。
(1)加聚反应:不饱和单体通过加聚反应生成高分子化合物。
①聚乙烯类(塑料、纤维)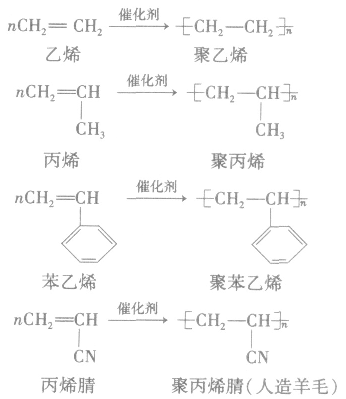
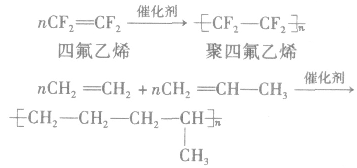
②聚二烯类(橡胶)
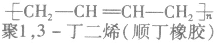
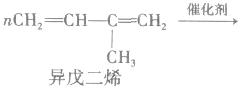
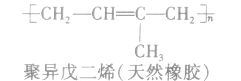
(2)缩聚反应:单体聚合成高分子的同时有小分子生成的聚合反应。
①聚酯类 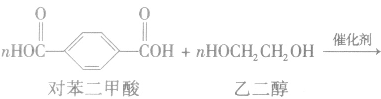
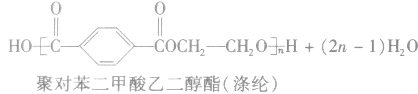
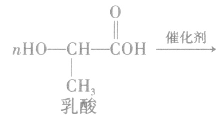
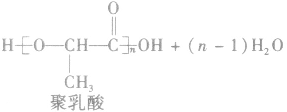
②聚氨基酯类
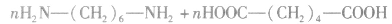
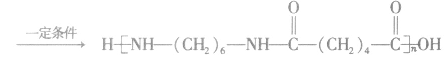
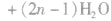

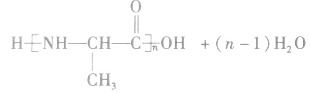
③酚醛树脂类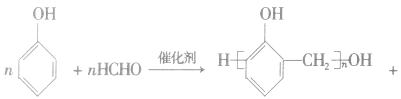
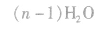
对高分子化合物的理解:
(1)通常把生成高分子化合物的低分子化合物(反应物)叫做单体(如乙烯是聚乙烯的单体),高分子化合物中化学组成相同、可重复的最小单位叫做链节(如一CH2一CH2一是聚乙烯的链节),高分子链中含有链节的数目叫做聚合度,通常用n表示。注意单体与链节是不同的,单体是反应前的低分子化合物;链节不是物质,不能独立存在,是反应后有机高分子化合物中的片段。 (2)低分子有机物的相对分子质量都有一个确定的数值,而高分子化合物的相对分子质量只是一个平均值。它是以低分子有机物作原料,经聚合反应得到各种相对分子质量不等的物质的混合物。
单体与高分子化合物的互推规律:
聚合时找准结合点,反推单体时找准分离处,“结合点必为分离处”。
1.由单体推断高聚物的方法
(1)单烯烃型单体加聚时,“断开双键,键分两端,添上括号,n写后面”。如

(2)二烯烃型单体加聚时,“单变双,双变单,破两头,移中间,添上括号.n写后面”。如
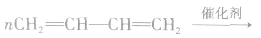
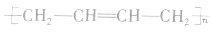
(3)分别含有一个双键的两种单体聚合时,“双键打开,中间相连,添上括号,n写后面”。如 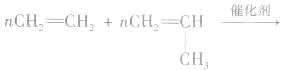
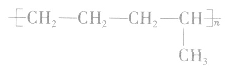
2.由高聚物推导单体的方法
(1)加聚产物单体的判断方法
①凡链节主链只有两个碳原子(无其他原子)的聚合物,其合成单体必为一种,将两个半键闭合即可。如
②凡链节主链有四个碳原子(无其他原子),且链节无双键的聚合物,其单体必为两种,在中央画线断开,然后两键闭合即可。如
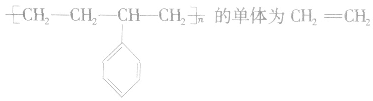
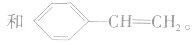
③凡链节主链上只有碳原子,斤存在碳碳双键结构的高聚物,其规律是“凡双键,四个碳;无双键,两个碳”画线断开。如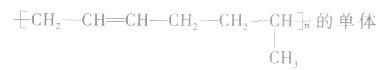
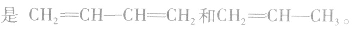
(2)缩聚产物单体的判断方法
①酯类高聚物中含有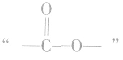 ,它的单体有两种,从
,它的单体有两种,从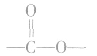 中间断开,
中间断开,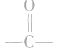 恢复为
恢复为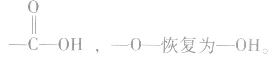
如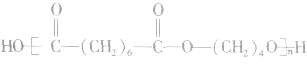 的单体为
的单体为
②酰胺类高聚物中含有"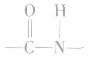 ",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如
",它的单体有两种,在亚氨基氮原子上加氢,羰基碳原子上加羟基,即得高聚物的单体。如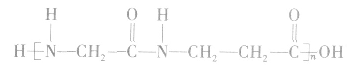 的单体为
的单体为
结构为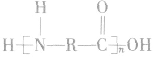 的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如
的高聚物,其合成单体必为一种,在亚氨基氮原子上加氢,在羰基碳原子上加羟基即得高聚物的单体。 如 的单体为
的单体为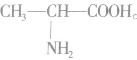
③酚醛树脂是由苯酚和甲醛缩聚而成的,链节中有酚羟基的结构。
如 和
和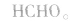
分离与提纯的原则和要求:
(1)选择分离与提纯方法应遵循的原则
①不增:指不能引入新的杂质。
②不减:指应尽可能减少被分离与提纯的物质的损失。
③易分离:指如果使用试剂除去杂质时,要求反应后的产物跟被提纯的物质容易分离。
④易复原:指分离物或被提纯的物质都要容易复原。
(2)分离与提纯操作过程应遵循“三必须”
①除杂质试剂必须过量;
②过量试剂必须除尽(因过量试剂会带人新的杂质);
③除杂途径必须选最佳。
常见的分离与提纯的方法:
(1)物质分离与提纯常用的物理方法
| 方法 | 适用范围或原理 | 装置 | 举例 | 注意事项 |
| 过滤 | 分离固体和液体混合物 | 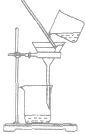 |
粗盐提纯时把粗盐溶于水,经过滤把不溶于水的杂质除去 | ①要“一贴二低三靠” 滤纸紧贴漏斗内壁;滤纸边缘低于漏斗口,漏斗里液面低于滤纸边缘;烧杯口紧靠玻璃棒,玻璃捧下端紧靠三层滤纸.漏斗下端紧靠烧杯内壁。 ②必要时洗涤沉淀物(在过滤器中加少量水),不可搅拌 |
| 结晶 重结晶 |
分离各组分在溶剂中的溶解度随温度变化不同的混合物 | 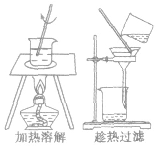 |
KNO3溶解度随温度变化大, NaCl溶解度随温度变化小,可用该法从二者的混合液中提纯KNO3 | ①一般先配较高温度下的浓溶液,然后降温结晶 ②结晶后过滤,分离出晶体 |
| 蒸发 | 溶解度随温度变化较小的物质 |  |
从食盐水溶液中提取食盐晶体 | ①溶质应不易分解、不易水解、不易被氧气氧化 ②蒸发过程应不断搅拌 ③近干时停止加热,余热蒸干 |
| 蒸馏 | 分离沸点不同的液体混合物 | 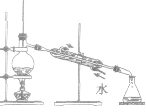 |
制无水乙醇(加生石灰)、硝酸的浓缩[加浓硫酸或 Mg(NO3)2] | ①温度计水银球在蒸馏烧瓶支管口处 ②加沸石(碎瓷片) ③注意冷凝管水流方向应下进上出 ④不可蒸干 |
| 分馏 | 分离多种液态混合物 | 同蒸馏 | 石油分馏 | 同蒸馏 |
| 萃取 | 分离两种互溶的液体 |  |
CCl4把溴水中的Br2萃取出来 |
①萃取后再进行分液操作 ②对萃取剂的要求:与原溶剂互不混溶,不反应;溶质在其中的溶解度比在原溶剂中大;溶质不与萃取剂反应 ③萃取后得到的仍是溶液,一般要通过分馏等方法进一步分离 |
| 分液 | 分离两种不相混溶的液体(密度不同) | 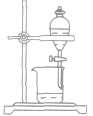 |
水、苯的分离 | 下层液体从下口放出,上层液体从上口倒出 |
| 液化 | 利用气体混合物中某组分易液化的特点来分离 | 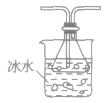 |
除去SO2中的SO3 | 可把锥形瓶换成硬质大试管 |
| 盐析 | 利用某些物质在加某些无机盐时,其溶解度降低而凝聚的性质来分离物质 | —— | 从皂化液中分离肥皂、甘油,蛋白质的盐析 | 盐析是物理变化。盐析之后一般要采取过滤的操作 |
| 洗气 | 杂质气体易溶于某液体 | 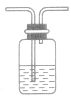 |
除去CO2中的HCl气体,可使混合气体通过盛有饱和NaHCO3 溶液的洗气瓶 | ①从洗气瓶的长导管一端进气 ②混合物中气体溶解度差别较大 |
| 升华 | 利用某些物质有升华的特性 |  |
粗碘中碘与钾、钠、钙、镁的碘化物混合,利用碘易升华的特点将碘与杂质分开 | 升华物质的集取方法不作要求 |
| 渗析 | 胶体提纯、精制 | 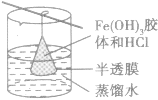 |
除去Fe(OH)3胶体中的HCl | 要不断更换烧杯中的水或改用流动水,以提高渗析效果 |
(2)物质分离与提纯常用的化学方法:
①加热法
混合物中混有某些热稳定性差的物质时,可直接加热,使热稳定性差的物质分解而分离出来。例如:食盐中混有氯化铵、纯碱中混有小苏打等均可直接加热除去杂质。
②沉淀法
在混合物中加入某试剂,使其中一种以沉淀形式分离出去的方法。使用该方法一定要注意不能引入新杂质,若使用多种试剂将溶液中不同粒子逐步沉淀时,应注意后加入试剂能将先加入的过量试剂除去,最后加入的试剂不引入新杂质。例如:加入适量BaCl2溶液可除去NaCl中混有的Na2SO4。
③转化法
利用化学反应将某种物质进行多次转化而分离。例如:分离Fe3+和Al3+时,可加入过量的NaOH溶液,生成Fe(OH)3和NaAlO2,过滤后,分别再加盐酸重新生成Fe3+和Al3+。注意转化过程中尽量减少被分离物质的损失.而且转化后的物质要易恢复为原物质。
④酸碱法
被提纯物质不与酸或碱反应,而杂质可与酸或碱发生反应,可用酸或碱作除杂试剂。例如:用盐酸除去 SiO2中的石灰石,用氢氧化钠除去铁粉中的铝粉。
⑤氧化还原法
a.对混合物中混有的还原性杂质,可加入适当的氧化剂将杂质氧化为被提纯物质。例如:将氯水滴入混有FeCl2的FeCl3溶液中,除去FeCl2杂质。
b.对混合物中混有的氧化性杂质,可加入适当还原剂将杂质还原为被提纯物质。例如:将过量铁粉加入混有FeCl3的FeCl2溶液中,振荡过滤,除去FeCl3 杂质。
⑥调节pH法
通过加入试剂来调节溶液的pH,使溶液中某组分沉淀而分离的方法。一般加入相应的难溶或微溶物来调节。例如:在CaCl2溶液中含有FeCl3杂质,由于 Fe3+水解,溶液呈酸性,可采用调节溶液pH的方法将 Fe3+沉淀除去,为此,可向溶液中加氧化钙或氢氧化钙或碳酸钙等。
⑦电解法
此法利用电解原理来分离、提纯物质。例如:电解精炼铜,将粗铜作阳极,精铜作阴极,电解液为含铜离子的溶液,通直流电,在阳极铜及比铜活泼的杂质金属失电子,在阴极只有铜离子得电子析出,从而提纯了铜。
1.定义:氮的固定是指将游离态的氮转化为化合态氮的方法。
2.方法:氮的固定主要方法有:
(1)人工合成氨 :化学固氨法。其条件要求高、成本高、转化率低、效率低。
(2)根瘤菌,生物固氨。常温常压下进行。成本低、转化率高、效率高。
3.工业应用:模拟生物的功能,把生物的功能原理用于化学工业生产,借以改善现有的并创造崭新的化学工艺过程。 二、合成氨的反应原理
1.加热试管中的铁丝绒至红热后注入氢气和氨气的混合气体,可以看到湿润的PH试纸变蓝色
2.用氢 气和氨气合成氨的反应式是
N2+3H2
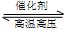 2NH3,属放热反应。
2NH3,属放热反应。 3.工业上,采用以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件下合成氨。
(1)催化剂的主要作用:成千上万倍地加快化学反应速率,缩短达平衡的时间,提高日产量。
(2)合成氨的适宜条件:以铁为主的催化剂,在400~500℃和10Mpa~30 Mpa的条件
(3)选择适宜生产条件的原则:有较高的反应速率和平衡转化率,能最大限度地提高利润。
(4)合成氨生产时,不采用尽可能高的压强,通常采用10MPa~30MPa 的压强,否则会增大设备的动力要求,增大成本。
(5)合成氨的反应为放热反应,降低温度促使平衡向有移动,有利于N2、H2转化为NH3;但降温必然减缓了反应速率,影响单位时间产率。生产中将二者综合考虑,既要保证N2、H2的转化率,又要保证较快的反应速率,只能选择适中的温度400~500℃左右。应注意该温度为催化剂活化温度,低于此温度,催化剂不起作用。
(6)催化剂是影响反应速率的几个因素中,对反应速率影响程度最大的。
催化剂的特点:
①选择性:不 同的反应选择不同的催化剂,如合成氨选择了铁触媒。每种催化剂都是对特定的反应有催化作用,并非能改变任何化学反应的速率。
②灵敏性:催化剂中混入杂质,常常会失去催化作 用,称催化剂“中毒”,因此 反应气体进入反应器前必须净化。 ③催化剂只有在活化温度以上才能起催化作用,如铁触媒活化温度为400~500℃,因此该温度为合成氨的适宜温度。
人工固氮技术——合成氨:
1.生产原理
2.合成氨的基本生产过程
(1)原料气的制备要实现合成氨的工业化生产,首先要解决氢气和氮气的来源问题。
①氮气的制备合成氨所需要的氮气都取自空气。从空气中制取氮气通常有两种方法:一是将空气液化后蒸发分离出氧气而获得氮气;二是将空气中的氧气与碳作用生成二氧化碳,再除去二氧化碳得到氮气。
②氢气的制备氢气主要来源于水和碳氢化合物。氢气的制取有下表中的几条途径。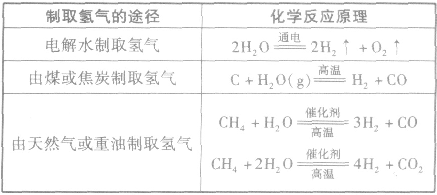
(2)原料气的净化
原料气的净化就是除去原料气中的杂质。在制取原料气的过程中,常混有一些杂质,其中的某些杂质会使合成氨所用的催化剂“中毒”(所谓“中毒”即是催化剂失去催化活性),所以必须除去。原料气净化的主要目的是防止催化剂“中毒”。
(3)氨的合成与分离
①氨的合成工业合成氨的主要设备是合成塔。将净化后的原料气经过压缩机压缩后输人合成塔,经过下列化学反应合成氨: 
②氨的分离从合成塔出来的混合气体,通常约含15%(体积分数)的氨。为了使氨从未反应的氮气和氢气里分离出来,要把混合气体通过冷凝器使氨液化,然后在气体分离器里把液态氨分离出来导入液氨贮罐。南气体分离器出来的气体,经过循环压缩机,再送到合成塔中进行反应。
3.合成氨适宜条件的选择
外加条件要尽可能加快反应速率,提高反应物的转化率.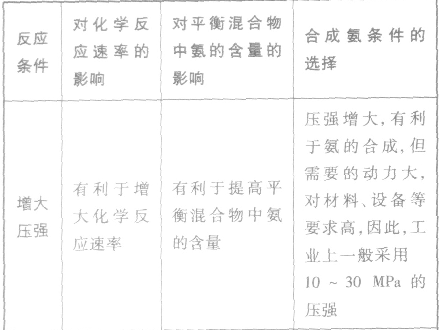
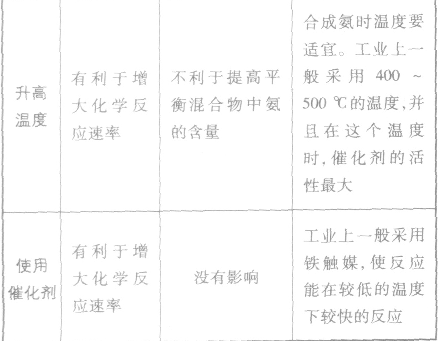
4.合成氨的环境保护
随着环境保护意识的增强,以及相关的法律、法规的严格实施,合成氨生产中可能产生的“三废”的处理越来越成为技术改造的重要问题。
(1)废渣
主要来自造气阶段,特别是以煤为原料而产生的煤渣,用重油为原料产生的炭黑等,现在大都将它们用作建材和肥料的原料。
(2)废气
主要是H2S和CO2等气体。对H2S气体的处理,先后采用了直接氧化法(选择性催化氧化)、循环法(使用溶剂将其吸收浓缩)等回收技术。对CO2 的处理,正在不断研究和改进将其作为尿素和碳铵生产原料的途径。
(3)废液
主要是含氰化物和含氨的污水。目前,处理含氰化物污水主要有生化、加压水解、氧化分解、化学沉淀、反吹回炉等方法;处理含氨废水多以蒸馏的方法回收氨达到综合利用的目的,对浓度过低的含氨废水,可用离子交换法治理。
与“下列说法你认为不正确的是( )A.实验室从苯酚中分离出苯的...”考查相似的试题有:
- 具有单双键交替长链(如:-CH=CH-CH=CH-CH=CH-)的高分子有可能成为导电塑料。2000年诺贝尔(Nobel)化学奖即授予开辟此领域的3...
- 下列实验操作正确的是( )A.做银镜反应实验后的试管内壁附有银,可用氨水清洗B.将饱和氯化铁溶液煮沸,可制得氢氧化铁胶体...
- 一集气瓶中气体呈红棕色,加入适量水后,盖上瓶盖振荡,得到橙色溶液,气体的红棕色消失,再打开瓶盖后,瓶中又呈红棕色,则...
- 为了达到下列表格中的实验要求,请从供选择的化学试剂及实验方法中选出合适的,将其标号填入对应的空格中。实验要求试剂及方...
- 请分别选用一种试剂除去下列物质中的杂质,并写出相应的离子方程式.物质杂质所选试剂离子方程式NaCl溶液Na2CO3____________M...
- (12分)某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度。(1)滴定:①用 式滴定管盛装camol/L盐酸标准液...
- 下列混合物的分离方法不可行的是 ( )。A.互溶的液态混合物可用分液方法分离B.互不相溶的液态混合物可用分液方法分离C.沸点...
- 下列分离和提纯的实验中,所选用的方法或仪器不正确的是( )序号ABCD实验目的制取蒸馏水分离水和植物油分离食盐水与泥沙从浓...
- 下列有关实验装置进行的相应实验,能达到实验目的的是A.用装置①除去Cl2中含有的少量HClB.用装置②从氯化铁溶液中直接蒸发结...
- 某KNO3溶液中,含杂质KBr,K2SO4和Ca(H2PO4)2,入试剂的顺序正确的是 A.Ba(NO3)2K2CO3KOH AgNO3HNO3B.AgNO3KOH K2CO3Ba...