本试题 “下列两组物质:甲--Fe、CuSO4、Na2CO3;乙--H2SO4、HC1、Ca(OH)2。(1)从物质分类的角度看,两组物质中均各有一种物质在类属上和其他物质不相同,它们是:甲__...” 主要考查您对化学反应方程式的书写
单质和化合物
酸、碱、盐
盐的性质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应方程式的书写
- 单质和化合物
- 酸、碱、盐
- 盐的性质
化学方程式的书写原则遵循两个原则:
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。
化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3 CaO+ CO2↑
CaO+ CO2↑
(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2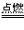 CO2
CO2
(3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2 2CuO
2CuO
④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2
 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
| 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。 ③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3
 CaO+ CO2↑
CaO+ CO2↑(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2
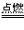 CO2
CO2 (3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2
 2CuO
2CuO ④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
单质:
(1)概念:由同种元素组成的纯净物。
(2)单质的分类:依据组成单质元素的性质把一单质分为三类。
金属单质:由金属元素组成的单质,如铁、铜、银等
非金属单质:由非金属元素组成的单质,如碳、磷、氧气等
稀有气体单质:由稀有气体元素组成的单质,如氦、氖、氛等单质
化合物:
(1)概念:由不同种元素组成的纯净物。
(2)化合物的分类:化合物分为有机化合物和无机化合物。
单质和化合物的区别和联系:
化合物与氧化物的区别和联系:
同种元素组成的物质一定是单质吗?
由同种元素组成的纯净物叫做单质。理解单质的概念必须抓住两点:①由同种元素组成;②必须是纯净物,如氧气是一单质。由同种元素组成的物质不一定是单质,也可能是混合物,但绝不可能是化合物,如氧气 (O2)、臭氧(O3)两种物质混在一起是一种混合物,但是只有一种氧元素;同样的例子还有红磷和白磷,金刚石和石墨等。
对单质和化合物概念的理解:
(1)单质的概念:
①理解一单质的概念不仅要关注它是由一种元素组成,还应注意它首先是一种纯净物。如:氧气、氮气、碳、硫、铁、铜、各种稀有气体等都属于单质。
②由同种元素组成的物质不一定是单质,还可能是混合物:如:氧气与臭氧的混合物、白磷与红磷的混合物、金刚石与石墨的混合物等都只含一种元素,但都属于混合物。
(2)化合物的概念:理解化合物的概念同样不仅要关注它是由两种或两种以上的元素组成,还应注意它首先是一种纯净物。如二氧化碳,氯化钠、高锰酸钾等都属于化合物。
(1)概念:由同种元素组成的纯净物。
(2)单质的分类:依据组成单质元素的性质把一单质分为三类。
金属单质:由金属元素组成的单质,如铁、铜、银等
非金属单质:由非金属元素组成的单质,如碳、磷、氧气等
稀有气体单质:由稀有气体元素组成的单质,如氦、氖、氛等单质
化合物:
(1)概念:由不同种元素组成的纯净物。
(2)化合物的分类:化合物分为有机化合物和无机化合物。
单质和化合物的区别和联系:
| 单质 | 化合物 | ||
| 区别 | 宏观组成 | 同种元素 | 不同种元素 |
| 微观构成 | 有同种原子构成 | 由不同种原子构成 | |
| 化学性质 | 不能发生分解反应 | 一定条件下发生分解反应 | |
| 联系 | 相互转变 | 它们均属于纯净物。单质发生化合反应可以生成化合物,化合物发生分解反应可以生成单质 | |
| 质子数 | 同一种元素的原子,不论在一单质里还是在化合物里,原子核内质子数保持不变 | ||
化合物与氧化物的区别和联系:
| 化合物 | 氧化物 | |
| 区别 | ①由不同种元素组成的纯净物叫化合物 ②由两种或两种以上元素组成 ③不一定含有氧元素 ④属于纯净物中的一类 |
①由两种元素组成的化合物中,如果有一种元素是氧元素,这种化合物叫氧化物 ②一定由两种元素组成 ③一定含有氧元素 ④属于化合物中的一类 |
| 联系 | 氧化物和化合物是个体与总体的关系,氧化物属于化合物中的一类 | |
同种元素组成的物质一定是单质吗?
由同种元素组成的纯净物叫做单质。理解单质的概念必须抓住两点:①由同种元素组成;②必须是纯净物,如氧气是一单质。由同种元素组成的物质不一定是单质,也可能是混合物,但绝不可能是化合物,如氧气 (O2)、臭氧(O3)两种物质混在一起是一种混合物,但是只有一种氧元素;同样的例子还有红磷和白磷,金刚石和石墨等。
对单质和化合物概念的理解:
(1)单质的概念:
①理解一单质的概念不仅要关注它是由一种元素组成,还应注意它首先是一种纯净物。如:氧气、氮气、碳、硫、铁、铜、各种稀有气体等都属于单质。
②由同种元素组成的物质不一定是单质,还可能是混合物:如:氧气与臭氧的混合物、白磷与红磷的混合物、金刚石与石墨的混合物等都只含一种元素,但都属于混合物。
(2)化合物的概念:理解化合物的概念同样不仅要关注它是由两种或两种以上的元素组成,还应注意它首先是一种纯净物。如二氧化碳,氯化钠、高锰酸钾等都属于化合物。
共价化合物与离子化合物的区别:
1. 共价化合物
(1)概念:像HCl、CO2这样以共用电子对结合在一起的化合物为共价化合物。
(2)共价化合物的类型:
①两种非金属原子结合成的化合物,如HCl、CO2等。
②非金属与酸根构成的化合物,如H2SO4、HNO3等。
2. 离子化合物与共价化合物的区别:
离子化合物是由阴、阳离子相互作用形成的化合物;共价化合物是原子间全部以共用电子对结合形成的化合物。离子化合物由离子构成,共价化合物大多数由分子构成。
酸:
1. 定义:电离时生成的阳离子全部是H+的化合物
2. 常见的酸:HCl,H2SO4,HNO3,H3PO4。
碱:
1. 定义:电离时生成的阴离子全部是OH-的化合物
2. 常见的碱:NaOH,KOH,Cu(OH)2,Fe(OH)3等
盐:
1. 定义:电离时生成金属离子(包括NH4+)和酸根离子的化合物
2. 常见的盐:NaCO3,NaCl,NaSO4等
酸、碱、盐的比较:
1. 定义:电离时生成的阳离子全部是H+的化合物
2. 常见的酸:HCl,H2SO4,HNO3,H3PO4。
碱:
1. 定义:电离时生成的阴离子全部是OH-的化合物
2. 常见的碱:NaOH,KOH,Cu(OH)2,Fe(OH)3等
盐:
1. 定义:电离时生成金属离子(包括NH4+)和酸根离子的化合物
2. 常见的盐:NaCO3,NaCl,NaSO4等
酸、碱、盐的比较:
| 从化学组成看 | 从电离观点看 | 组成特点 | |
| 酸 | 由氢元素和酸根组成 | 电离时生成的阳离子全都是氢离子(H+)的化合物 | 一定含氢元素 |
| 碱 | 由金属元素和氢氧根组成(氨水也是碱) | 电离时生成的阴离子全都是氢氧根离子(OH-)的化合物 | 一定含氢、氧 元素 |
| 盐 | 含有金属元素(或NH4+) 和酸根 | 电离时能生成金属离子(或NH4+)和酸根离子的化合物 | 酸式盐中一定含氢元素,碱式盐中一定含氢、氧元素 |
盐的定义:
盐是指由金属离子(或钱根离子)和酸根离子构成的化合物,盐在溶液里能解离成金属离子(或钱根离子)和酸根离子。根据阳离子不同,可将盐分为钠盐、钾盐、钙盐、钱盐等,根据阴离子不同,可将盆分为硫酸盐、碳酸盐,硝酸盐等。
生活中常见的盐有:
氯化钠(NaCl),碳酸钠 (Na2CO3)、碳酸氧钠(NaHCO3)、碳酸钙和农业生产上应用的硫酸铜(CuSO4)。
盐的物理性质:
(1)盐的水溶液的颜色常见的盐大多数为白色固体,其水溶液一般为无色。但是有些盐有颜色,其水溶液也有颜色。例如:胆矾(CuSO4·5H2O)为蓝色,高锰酸钾为紫黑色;含Cu2+的溶液一般为蓝色,含Fe2+的溶液一般为浅绿色,含Fe3+的溶液一般为黄色。
(2)盐的溶解性记忆如下钾钠硝钱溶水快(含K+,Na+,NH4+,NO3-的盐易溶于水);硫酸盐除钡银钙(含SO42-的盐中,Ag2SO4, CaSO4微溶,BaSO3难溶)都易溶;氯化物中银不溶(含 Cl-的盐中,AgCl不溶于水,其余一般易溶于水);碳酸盐溶钾钠钱[含CO32-的盐,Na2CO3、(NH4)2CO3、 K2CO3易溶,Na2CO3微溶,其余难溶〕。
盐的化学性质:
(1)盐+金属一另一种盐+另一种金属(置换反应),例如:Fe+CuSO4==FeSO4+Cu
规律:反应物中盐要可溶,金属活动性顺序表中前面的金属可将后面的金属从其盐溶液中置换出来(K, Ca,Na除外)。
应用:判断或验证金属活动性顺序和反应发生的先后顺序。
(2)盐+酸→另一种盐+另一种酸(复分解反应),例如;HCl+AgNO3==AgCl↓+HNO3。
规律:反应物中的酸在初中阶段一般指盐酸、硫酸、硝酸。盐是碳酸盐时可不溶,若是其他盐,则要求可溶。应用:实验室制取CO2,CO32-、Cl-,SO42-的检验。
(3)盐+碱→另一种盐+另一种碱(复分解反应)
规律:反应物都可溶,若反应物中盐不为按盐,生成物其中之一为沉淀或水。
应用:制取某种碱,例如:Ca(OH)2+Na2CO3== CaCO3↓+2NaOH。
(4)盐+盐→另外两种盐
规律:反应物都可溶,生成物至少有一种不溶于水。
应用:检验某种离子或物质。例如:NaCl+AgNO3 =AgCl↓+NaNO3(可用于鉴定Cl-);Na2SO4+BaCl2==BaSO4↓+2NaCl(可用与鉴定SO42-)
几种常见盐的性质及用途比较如下表:
易错点:
①“食盐是盐是对的,但“盐就是食盐”是错误的,化学中的“盐”指的是一类物质。
②石灰石和大理石的主要成分是碳酸钙,它们是混合物,而碳酸钙是纯净物。
③日常生活中还有一种盐叫亚硝酸钠,工业用盐中常含有亚硝酸钠,是一种自色粉末,有咸味,对人体有害,常用作防腐保鲜剂。
④CuSO4是一种白色固体,溶于水后形成蓝色的CuSO4溶液,从CuSO4溶液中结品析出的晶体不是硫酸铜,而是硫酸铜晶休,化学式为CuSO4·5H2O,俗称胆矾或蓝矾,是一种蓝色固体。硫酸铜与水结合也能形成胆矾,颜色由白色变为蓝色.利用这种特性常用硫酸铜固体在化学实验中作检验水的试剂。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
风化:
风化是指结晶水合物在室温和干燥的条件下失去结晶水的现象,这种变化属于化学反应。如 Na2CO3·10H2O==Na2CO3+10H2O;CaSO4·2H2O ==CaSO4+2H2O。
侯氏制碱法:
我国化工专家侯德榜于1938-1940年用了三年时间,成功研制出联合制碱法,后来命名为“侯氏联合制碱法”。其主要原理是:
NH3+CO2+H2O== NH4HCO3
NH4HCO3+NaCl ==NaHCO3↓+NH4CI
2NaHCO3==Na2CO3+H2O+CO2↑
(1)NH3与H2O,CO2反应生成NH4HCO3。
(2)NH4HCO3与NaCl反应生成NaHCO3沉淀。主要原因是NaHCO3的溶解度较小。
(3)在第(2)点中过滤后的滤液中加入NaCl,由于 NH4CI在低温时溶解度非常低,使NH4Cl结晶析出,可做氮肥。
(4)加热NaHCO3得到Na2CO3.
优点:保留了氨碱法的优点,消除了它的缺点,提高了食盐的利用率,NH4Cl可做氮肥,同时无氨碱法副产物CaCl2毁占耕田的问题。
盐是指由金属离子(或钱根离子)和酸根离子构成的化合物,盐在溶液里能解离成金属离子(或钱根离子)和酸根离子。根据阳离子不同,可将盐分为钠盐、钾盐、钙盐、钱盐等,根据阴离子不同,可将盆分为硫酸盐、碳酸盐,硝酸盐等。
生活中常见的盐有:
氯化钠(NaCl),碳酸钠 (Na2CO3)、碳酸氧钠(NaHCO3)、碳酸钙和农业生产上应用的硫酸铜(CuSO4)。
盐的物理性质:
(1)盐的水溶液的颜色常见的盐大多数为白色固体,其水溶液一般为无色。但是有些盐有颜色,其水溶液也有颜色。例如:胆矾(CuSO4·5H2O)为蓝色,高锰酸钾为紫黑色;含Cu2+的溶液一般为蓝色,含Fe2+的溶液一般为浅绿色,含Fe3+的溶液一般为黄色。
(2)盐的溶解性记忆如下钾钠硝钱溶水快(含K+,Na+,NH4+,NO3-的盐易溶于水);硫酸盐除钡银钙(含SO42-的盐中,Ag2SO4, CaSO4微溶,BaSO3难溶)都易溶;氯化物中银不溶(含 Cl-的盐中,AgCl不溶于水,其余一般易溶于水);碳酸盐溶钾钠钱[含CO32-的盐,Na2CO3、(NH4)2CO3、 K2CO3易溶,Na2CO3微溶,其余难溶〕。
盐的化学性质:
(1)盐+金属一另一种盐+另一种金属(置换反应),例如:Fe+CuSO4==FeSO4+Cu
规律:反应物中盐要可溶,金属活动性顺序表中前面的金属可将后面的金属从其盐溶液中置换出来(K, Ca,Na除外)。
应用:判断或验证金属活动性顺序和反应发生的先后顺序。
(2)盐+酸→另一种盐+另一种酸(复分解反应),例如;HCl+AgNO3==AgCl↓+HNO3。
规律:反应物中的酸在初中阶段一般指盐酸、硫酸、硝酸。盐是碳酸盐时可不溶,若是其他盐,则要求可溶。应用:实验室制取CO2,CO32-、Cl-,SO42-的检验。
(3)盐+碱→另一种盐+另一种碱(复分解反应)
规律:反应物都可溶,若反应物中盐不为按盐,生成物其中之一为沉淀或水。
应用:制取某种碱,例如:Ca(OH)2+Na2CO3== CaCO3↓+2NaOH。
(4)盐+盐→另外两种盐
规律:反应物都可溶,生成物至少有一种不溶于水。
应用:检验某种离子或物质。例如:NaCl+AgNO3 =AgCl↓+NaNO3(可用于鉴定Cl-);Na2SO4+BaCl2==BaSO4↓+2NaCl(可用与鉴定SO42-)
几种常见盐的性质及用途比较如下表:
| 氯化钠 | 碳酸钠 | 碳酸氢钠 | 碳酸钙 | 硫酸铜 | |
| 化学式 | NaCl | Na2CO3 | NaHCO3 | CaCO3 | CuSO4 |
| 俗称 | 食盐 | 纯碱、苏打 | 小苏打 | —— | —— |
| 物理性质 | 白色固体,易溶于水。水溶液有咸味,溶解度受温度影响小 | 白色固体,易溶于水 | 白色固体,易溶于水 | 白色固体,不溶于水 | 白色固体,易溶于水,溶液为蓝色,有毒 |
| 化学性质 | 水溶液显中性 AgNO3+NaCl==AgCl↓+NaNO3 |
水溶液显碱性 Na2CO3+2HCl==2NaCl+H2O+CO2↑ Na2CO3+Ca(OH)2==CaCO3↓+2NaOH |
水溶液显碱性 NaHCO3+HCl==NaCl+H2O+CO2↑ |
CaCO3+2HCl==CaCl2+H2O+CO2↑ | CuSO4+5H2O==CuSO4·5H2O CuSO4+Fe==FeSO4+Cu CuSO4+2NaOH==Cu(OH)2↓+Na2SO4 |
| 用途 | 作调味品和防腐剂,医疗上配置生理盐水。重要的化工原料 | 制烧碱,广泛用于玻璃、纺织、造纸等工业 | 焙制糕点的发酵粉的主要成分,医疗上治疗胃酸过多 | 实验室制取CO2,重要的建筑材料,制补钙剂 | 农业上配制波尔多液,实验室中用作水的检验试剂,精炼铜 |
易错点:
①“食盐是盐是对的,但“盐就是食盐”是错误的,化学中的“盐”指的是一类物质。
②石灰石和大理石的主要成分是碳酸钙,它们是混合物,而碳酸钙是纯净物。
③日常生活中还有一种盐叫亚硝酸钠,工业用盐中常含有亚硝酸钠,是一种自色粉末,有咸味,对人体有害,常用作防腐保鲜剂。
④CuSO4是一种白色固体,溶于水后形成蓝色的CuSO4溶液,从CuSO4溶液中结品析出的晶体不是硫酸铜,而是硫酸铜晶休,化学式为CuSO4·5H2O,俗称胆矾或蓝矾,是一种蓝色固体。硫酸铜与水结合也能形成胆矾,颜色由白色变为蓝色.利用这种特性常用硫酸铜固体在化学实验中作检验水的试剂。
盐的命名:
(1)只有两种元素组成的盐,读作“某化某”,如 NaCl读作氯化钠,AgI读作碘化银。
(2)构成中含有酸根的,读作“某酸某”。如Na2CO3、ZnSO4、AgNO3、KMnO4、KClO3分别读作:碳酸钠、硫酸锌、硝酸银、高锰酸钾、氯酸钾。
(3)含铵根的化合物,读作“某化铵”或“某酸铵”。如NH4Cl、(NH4)2SO4读作:氯化铵、硫酸铵。
(4)其他:Cu2(OH)2CO3读作“碱式碳酸铜”, NaHSO4读作“硫酸氢钠”, NaHCO3读作“碳酸氢钠”。
风化:
风化是指结晶水合物在室温和干燥的条件下失去结晶水的现象,这种变化属于化学反应。如 Na2CO3·10H2O==Na2CO3+10H2O;CaSO4·2H2O ==CaSO4+2H2O。
侯氏制碱法:
我国化工专家侯德榜于1938-1940年用了三年时间,成功研制出联合制碱法,后来命名为“侯氏联合制碱法”。其主要原理是:
NH3+CO2+H2O== NH4HCO3
NH4HCO3+NaCl ==NaHCO3↓+NH4CI
2NaHCO3==Na2CO3+H2O+CO2↑
(1)NH3与H2O,CO2反应生成NH4HCO3。
(2)NH4HCO3与NaCl反应生成NaHCO3沉淀。主要原因是NaHCO3的溶解度较小。
(3)在第(2)点中过滤后的滤液中加入NaCl,由于 NH4CI在低温时溶解度非常低,使NH4Cl结晶析出,可做氮肥。
(4)加热NaHCO3得到Na2CO3.
优点:保留了氨碱法的优点,消除了它的缺点,提高了食盐的利用率,NH4Cl可做氮肥,同时无氨碱法副产物CaCl2毁占耕田的问题。
发现相似题
与“下列两组物质:甲--Fe、CuSO4、Na2CO3;乙--H2SO4、HC1、Ca(O...”考查相似的试题有:
- 写出下列化学方程式.(1)水电解生成氢气和氧气:______.(2)二氧化碳通人澄清石灰水,使其变浑浊:______.(3)铁在氧气...
- 过氧化氢(化学式为H2O2)2以氧化锰为催化剂可迅速分解产生水和氧气.现欲制得于燥而纯净的氧气,可采用下图装置.装置A中,...
- 判断下列关于化学反应的说法是否正确,在正确说法下的横线上划“√”,在错误说法下的横线上用化学方程式举出一个否定的例子:(...
- “从生活走向化学,从化学走向社会”,体现了化学学习的新理念.化学对于生产、生活及社会发展具有重要的意义.(1)电动自行车...
- 小明发烧去医院打吊针时,看到一个小朋友不小心将体温计打碎了,护士在散落的汞上撒了一些硫粉,使之变成硫化汞(HgS)固体,...
- 下图是化学实验中常用的几种装置.(1)写出标有序号的仪器名称:①______;②______.(2)在实验室中用过氧化氢溶液和二氧化...
- 下列化学方程式书写完全正确的是( )A.2Fe+O2 点燃 . 2FeOB.CO+O2 点燃 . CO2C.CO2↑+H2O=H2CO3D.2Mg+O2 点燃 . 2MgO
- 在①C,Fe,S,P;②MgO,CuO,CaO,SO2;③NO2,CO,HCl,H2O三组物质中,各有一种物质在分类上与组内其它物质不同,这三种物质...
- 分类是一种重要的学习方法(1)在下表的空格内写出相应的物质名称或化学式(分子式),并指出物质的类别(单质、氧化物、酸、...
- 为除去下表样品中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是[ ]样品成分所选试剂操作方法A.KCl(MnO2)水溶...