本试题 “溴被称为“海洋元素”。已知Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性。实验室模拟从海水中提取溴的主要步骤为:步骤1:将海水蒸发浓缩除去粗盐步骤2:将除...” 主要考查您对海水资源的综合利用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 海水资源的综合利用
海水资源的综合利用:
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
浩瀚的海洋是个巨大的资源宝库,它不仅孕育着无数的生命,还孕育着丰富的矿产,而海水本身含有大量的化学物质,又是宝贵的化学资源。可从海水中提取大量的食盐、镁、溴、碘、钾等有用物质,海水素有“液体工业原料”之美誉。
海水制盐:
(1)海水制盐的方法:从海水中得到食盐的方法有蒸发法(盐田法)、电渗析法等。目前,以蒸发法(盐田法)为主。
(2)海水晒盐的基本原理:水分不断蒸发,氯化钠等盐结晶析出。
(3)海水晒盐的流程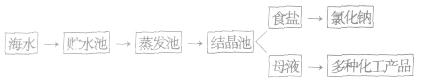
氯碱工业:
(1)食盐水的精制
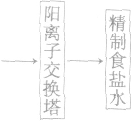
(2)电极反应
阴极: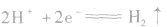
阳极:
总反应: :
:
(3)主要设备
离子交换膜电解槽一一阳极用金属钛(表面涂有钛、钉氧化物层)制成,阴极用碳钢(覆有镍镀层)制成。阳离子膜具有选择透过性,只允许Na+透过,而Cl-、 OH一和气体不能透过。 
(4)产品及用途
烧碱:可用于造纸、玻璃、肥皂等工业
氯气:可用于制农药、有机合成、氯化物的合成
氢气:可用于金属冶炼、有机合成、盐酸的制取
海水提溴:
(1)氯化
氯化氧化溴离子,在pH=3.5的酸性条件下效果最好,所以在氯化之前要将海水酸化。
(2)吹出
当海水中的Br一被氧化成Br2以后,用空气将其吹出。另外,也可以用水蒸气,使溴和水蒸气一起蒸出。
(3)吸收
目前比较多的是用二氧化硫作还原剂,使溴单质转化为HBr,再用氯气将其氧化得到溴产品。化学方程式如下: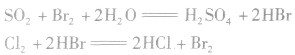
海水提镁:
(1)工艺流程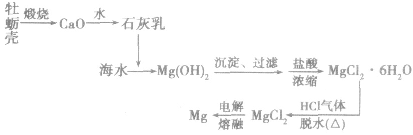
(2)主要化学反应
①制备石灰乳: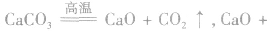
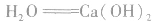
②沉淀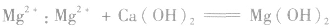
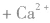
③制备
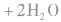
从海水中提取重水:
提取重水的方法:蒸馏法、电解法、化学交换法、吸附法等。常用方法:化学交换法(硫化氢一水双温交换法)
铀和重水目前是核能开发中的重要原料,从海水中提取铀和重水对一个国家来说具有战略意义,化学在开发海洋药物方面也将发挥越来越大的作用。潮汐能、波浪能也是越来越受到重视的新型能源。
发现相似题
与“溴被称为“海洋元素”。已知Br2的沸点为59℃,微溶于水,有毒性...”考查相似的试题有:
- 下列关于工业生产的说法中,不正确的是A.工业上,用焦炭在电炉中还原二氧化硅得到含杂质的粗硅B.生产普通水泥的主要原料有...
- 海水中有取之不尽的化学资源,从海水中可提取多种化工原料。下图是某工厂对海水资源的综合利用的示意图。试回答下列问题:(1)...
- 工业上从海水中提取单质溴可采用如下方法:(1)向海水中通入Cl2,将海水中的溴化物氧化,其离子方程式为_____________________...
- I.目前,我国采用“接触法”制硫酸,设备如图所示:(1)图中设备A的名称是_____________,该设备中主要反应的化学方程式为 。...
- 被誉为春果第一枝的大樱桃已经成为烟台农业经济的一个亮点。为了预防大樱桃在成熟期发生裂果现象,果农常施用一种钾肥。这种...
- 下列有关工业生产的叙述中错误的是A.电解氯化钠溶液制金属钠B.石灰石是炼铁和制玻璃的原料之一C.氯气通入石灰乳中制漂白粉...
- 在硫酸的工业制法中,下列生产操作及说明生产操作的主要原因二者都正确的是 A.从沸腾炉出来的炉气需净化,因为炉气中SO3会与...
- 2011年7月16日14时25分,中国石油大连石化公司厂区内1000万吨常减压蒸馏装置换热器发生泄漏,引发大火,所幸的是无人员伤亡。...
- 从海水中提取镁是世界各国获得镁的主要来源,以下是制取镁的过程中涉及的几种物质的溶度积,根据你所学的知识回答下列几个问...
- (16分)碳酸锂广泛应用于陶瓷和医药等领域。已-锂辉石(主要成分为Li2OAl2O34SiO2)为原材料制备Li2CO3的工艺流程如下:已知...