本试题 “下列说法正确的是[ ]A.多肽、油脂、纤维素、淀粉、蔗糖和葡萄糖在一定条件都能发生水解反应B.福尔马林、葡萄糖溶液与新制氢氧化铜悬浊液共热,都会有砖红色...” 主要考查您对溶液
浊液
胶体
葡萄糖
蔗糖
淀粉
纤维素
油脂
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 溶液
- 浊液
- 胶体
- 葡萄糖
- 蔗糖
- 淀粉
- 纤维素
- 油脂
一种或几种物质分散到另一种物质中,形成均一、稳定的混合物,分散质粒子的直径d<10-9m
电中性原理:
溶液对外是不显电性的,所以,在电解质的溶液中,阳离子所带正电荷总数=阴离子所带负电荷总数。
如含K+、Al3+、H+、Cl-、SO42-的溶液中,必然存在c(K+)+3c(Al3+)+c(H+)=c(Cl-)+2c(SO42-)。
溶液的稀释定律:
- 稀释前后溶液中溶质的物质的量不变: c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液)
- 稀释前后溶液中溶质的质量不变: ρ(浓溶液)V(浓溶液)w%(浓溶液)=ρ(稀溶液)V(稀溶液)w%(稀溶液)
容量瓶的使用:
1.容量瓶的使用及注意事项
(1)在使用前首先要检查是否漏水。
具体操作如下:
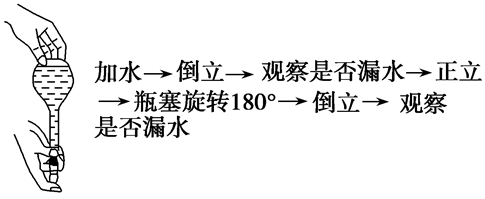
(2)检查合格后,用蒸馏水洗涤干净。
(3)四个“不能”
①不能将固体或浓溶液直接在容量瓶中溶解或稀释。
②不能作为反应容器或长期贮存溶液。
③容量瓶的容积是在瓶身所标温度下确定的,因而不能将过冷或过热的溶液转移到容量瓶中。
④只能配制容量瓶上规定容积的溶液,即不能配制任意体积的溶液。
2. 误差分析
分析依据 ,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
,以配置NaOH溶液为例,在进行误差分析时,根据实验操作弄清是“m”还是“V”引起的误差,再具体分析,具体情况如下:
| 能引起误差的一些操作 | 因变量 | c(mol/L) | |
| m | V | ||
| 砝码与物品颠倒(使用游码) | 减小 | —— | 偏低 |
| 称量时间过长 | 减小 | —— | |
| 用滤纸称NaOH | 减小 | —— | |
| 向容量瓶注液时少量溅出 | 减小 | —— | |
| 未洗涤烧杯和玻璃棒 | 减小 | —— | |
| 定容时,水多用滴管吸出 | 减小 | —— | |
| 定容摇匀后液面下降再加水 | —— | 增大 | |
| 定容时仰视刻度线 | —— | 增大 | |
| 砝码沾有其他物质或已生锈 | 增大 | —— | 偏高 |
| 未冷却至室温就注入容量瓶定容 | —— | 减小 | |
| 定容时俯视读数 | —— | 减小 | |
| 称量前小烧杯内有水 | —— | —— | 不变 |
| 定容后经振荡、摇匀,静置液面下降 | —— | —— | |
特别提醒:
(1)定容、摇匀后液面下降也不要补加蒸馏水,否则结果会偏低。
(2)定容时俯视、仰视对结果的影响。
①仰视刻度线(图1),导致溶液体积偏大。
②俯视刻度线(图2),导致溶液体积偏小。

为减小误差务必按:眼睛视线→刻度线→凹液面最低处的次序,做到“三点一线”。
一定物质的量浓度的溶液的配置:
1.主要仪器 (1)托盘天平:可精确至0.1g,称量前先调零,称量时物品放在左盘,砝码放在右盘。
(2)容量瓶:配制溶液的专用精确容器,瓶上标有温度、容积和刻度线。
(3)其他仪器:量筒、烧杯、玻璃棒、胶头滴管等。
2.配制过程
配制过程如下:

以配制480mL1mol·L-1NaCl溶液为例:
(1)所需容量瓶规格:500mL容量瓶。
(2)若用托盘天平应称量NaCl粉末29.3g。
(3)溶解过程中玻璃棒的作用为:搅拌加速溶解。
(4)移液
①移液前需要将溶液冷却至室温。
②移液中玻璃棒的作用为:引流。
③移液时需要进行的操作为:将烧杯中溶液注入容量瓶中,用少量蒸馏水洗涤烧杯内壁2~3次并将洗涤液也转入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀。
(5)定容
①当液面距瓶颈刻度线1~2cm时改用胶头滴管滴加蒸馏水。
②定容时要平视刻度线,直到凹液面最低点与刻度线相切。
(6)摇匀,转入试剂瓶保存
假如其他操作均准确无误,分析下列情况对配制浓度的影响。
①定容时俯视观察刻度线:偏高;
②移液时,对用于溶解NaCl的烧杯没有洗涤:偏低;
③定容后,将容量瓶振荡摇匀,静置后发现液面低于刻度线,又补水至刻度线:偏低。
溶液配制过程中的“四个数据”:
(1)选择容量瓶的规格时应该与所配溶液体积相等或稍大
数据
要求或解释
药品的质量
实验室中一般用托盘天平称量药品,而托盘天平只能称准0.1g,所以记录数据时只能保留小数点后一位数字。如题中NaOH的质量为10.0,不能写为10.00g
容量瓶的规格
(2)回答补充仪器的问题时应该注明容量瓶的规格,如应该回答“500ml容量瓶”,不能只回答“容量瓶”。
洗涤烧瓶2-3次
移液时洗涤烧瓶2-3次是为了确保溶质全部转移入容量瓶中,否则会导致溶液浓度偏低
液面离容量瓶颈刻度线下1-2cm
定容时,当液面离容量瓶颈刻度线下1-2cm时,应该改用胶头滴管滴加,否则溶液导致液体体积超过刻度线,导致溶液浓度偏低
浊液:
粒子直径大于100nm的分散系,若分散质为固体小颗粒的称为悬浊液,若分散质为小液滴的称为乳浊液。
悬浊液是固体的小颗粒分散在溶剂中所形成的混合物;
乳浊液是液体的小液滴分散在溶剂中所形成的混合物。
浊液的特性:
浊液里的固体小颗粒或小液滴都是由巨大数量的分子(或原子等)集合而成的。浊液静置后,其中的固体小颗粒或小液滴会逐渐下沉或上浮。所以浊液中物质的分散是不均一、不稳定的。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体:分散质粒子直径在10-9m~10-7m之间的分散系胶粒直径的大小是胶体的本质特征
胶体可分为固溶胶、液溶胶、气溶胶
①常见的液溶胶:Fe(OH)3、AgI、牛奶、豆浆、粥等
②常见的气溶胶:雾、云、烟等;
③常见的固溶胶:有色玻璃、烟水晶等胶体的性质:
丁达尔效应:
①当光束通过氢氧化铁胶体时,可以看到一条光亮的通路,这条光亮的通路是由于胶体粒子对光线散射(光波偏离原来方向而分散传播)形成的,即为丁达尔效应。
②布朗运动:粒子在不停地、无秩序的运动
③电泳:胶体粒子带有电荷,在电场的作用下,胶体粒子在分散剂里定向移动。一般来讲:金属氢氧化物,金属氧化物的胶粒吸附阳离子,胶体微粒带正电荷;非金属氧化物,金属硫化物的胶体胶粒吸附阴离子,胶体微粒带负电荷。
④胶体聚沉:向胶体中加入少量电解质溶液时,由于加入的阳离子(或阴离子)中和了胶体粒子所带的电荷,使胶体粒子聚集成为较大的颗粒,从而形成沉淀从分散剂里析出。该过程不可逆。
胶体的特性:
(1)丁达尔效应当一束光通过胶体时,胶体内会出现一条光亮的通路,这是由胶体粒子对光线散射而形成的,利用丁达尔效应可区分胶体和浊液。
(2)介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,但改变条件就有可能发生聚沉。
(3)聚沉:给胶体加热、加入电解质或加入带相反电荷的胶体颗粒等均能使胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出。聚沉常用来解释生活常识,如长江三角洲的形成、明矾净水等。
(4)电泳现象:在电场作用下,胶体粒子在分散剂中作定向移动。电泳现象说明胶体粒子带电。电泳常用来分离提纯胶体,如工业上静电除尘。
分散系比较:
| 分散系 | 溶液 | 胶体 | 悬浊液 | 乳浊液 |
| 分散质粒子大小 | <1nm | 1~100nm | >100nm | >100nm |
| 分散质粒子结构 | 分子、离子 | 少量分子的结合体或大分子 | 大量分子聚集成的固体小颗粒 | 大量分子聚集成的液体小液滴 |
| 特点 | 均一、透明、稳定 | 多数均一、透明、较稳定 | 不均一、不透明、久置沉淀 | 不均一、不透明、久置分层 |
| 能否透过滤纸 | 能 | 能 | 不能 | —— |
| 实例 | 食盐水、蔗糖溶液 | Fe(OH)3(胶体)、淀粉胶体 | 泥水、石灰乳 | 牛奶、油漆 |
胶体发生聚沉的条件:
因胶粒带电,故在一定条件下可以发生聚沉:
- 向胶体中滴加电解质
- 向胶体中加入带相反电荷胶粒的胶体
- 加热
常见的胶体的带电情况:
- 胶粒带正电荷的胶体有:金属氧化物、金属氢氧化物。例如Fe(OH)3、Al(OH)3等。
- 胶粒带负电荷的胶体有:非金属氧化物、金属硫化物、硅酸胶体、土壤胶体。
- 胶粒不带电的胶体有:淀粉胶体。
- 特殊的,AgI胶粒随着AgNO3和KI相对量不同,而带正电或负电。若KI过量,则AgI胶粒吸附较多I-而带负电;若AgNO3过量,则因吸附较多Ag+而带正电。
注意:胶体不带电,而胶粒可以带电。
Fe(OH)3胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
点拨:(1)淀粉溶液、蛋白质溶液虽叫做溶液,但属于胶体。
(2)胶体可以是液体,也可以是固体、气体,如烟、云、雾、有色玻璃等。
葡萄糖的结构:
分子式: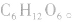
结构式: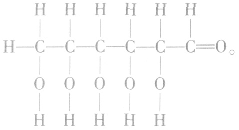
结构简式: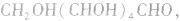 葡萄糖为多羟基醛(五羟基己醛)
葡萄糖为多羟基醛(五羟基己醛)
葡萄糖的性质:
1.葡萄糖的物理性质
葡萄糖是无色晶体,易溶于水,有甜味。
2.葡萄糖的化学性质
①氧化反应(显还原性)
a.燃烧

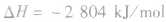
b.葡萄糖在人体组织中的缓慢氧化反应

c.与新制Cu(OH)2反应(用于检验糖尿病)
实验操作:在试管里加入2mL10%(质量分数) NaOH溶液,滴加2%(质量分数)CuSO4溶液4—6滴,得到新制Cu(OH)2,振荡后加入2mL10%葡萄糖溶液,在酒精灯上加热,观察现象。
实验现象:溶液中有红色沉淀产生。反应原理:葡萄糖分子中含有醛基,具有还原性,能把新生成的氢氧化铜还原成红色的氧化亚铜沉淀。发生的反应为

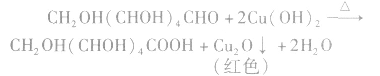
d.银镜反应(用于制镜或在保温瓶胆上镀银)
葡萄糖在热水浴中能被银氨溶液氧化,洁净的试管壁上会产生光亮的银镜,此反应称为银镜反应。可用于葡萄糖的检验。
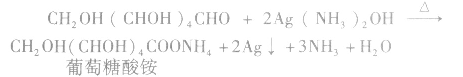
e.使溴水或酸性KMnO4溶液褪色
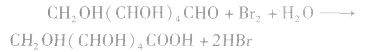
②加成反应

③酯化反应
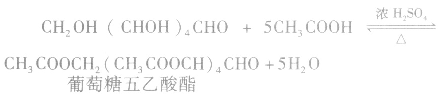
④与活泼金属钠反应
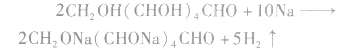
⑤在酒化酶作用下发酵
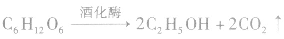
分子是为C12H22O11,与麦芽糖互为同分异构体。蔗糖水解生成一份子葡萄糖和一份子果糖。蔗糖存在甘蔗和甜菜中。蔗糖分子中没有醛基,不能与银氨溶液和新制氢氧化铜悬浊液反应,为非还原性糖。
蔗糖和麦芽糖:
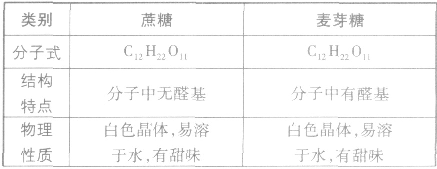

淀粉的结构:
分子组成:
结构特点:由几百个到几千个单糖单元构成的高分子化合物。有直链及支链结构
淀粉的性质:
1、物理性质:无气味、无味道的粉末状物质,它不溶于冷水,在热水里淀粉颗粒会膨胀破裂,有一部分淀粉溶解在水里。另一部分淀粉悬浮在水里,形成胶状淀粉糊(即糊化作用)
2、化学性质:
①不与银氨溶液发生银镜反应,是一种非还原性糖
②在酸或酶的作用下发生水解,最终产物是葡萄糖,反应方程式为: 

③淀粉遇碘后显蓝色
淀粉水解程度的判断:
淀粉在酸或酶的作用下水解,最终生成葡萄糖。淀粉遇碘变蓝色,不能发生银镜反应;而产物葡萄糖遇碘不变蓝色,能发生银镜反应。依据这两种物质的性质,可用银氨溶液和碘水来检验淀粉是否水解或水解的程度。
实验步骤如下: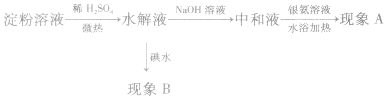
实验现象与结论见下表:
纤维素:
分子组成:(C6H10O5)n(n与淀粉分子式中的n是不同的值,故二者不是同分异构体)
结构特点:由几千个葡萄糖单元构成的高分子化合物
纤维素的性质:
1、物理性质:白色、无嗅、无味的具有纤维状结构的物质,一般不溶于水和有机溶剂
2、化学性质:
①不与银氨溶液发生银镜反应,是一种非还原性糖
②在酸作用下水解,最终产物是葡萄糖。比淀粉水解困难,反应方程式为: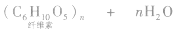

油脂:
1.概念:
油和脂肪统称为油脂,在化学成分上都是高级脂肪酸甘油酯,属于酯类。
2.油脂的组成和结构:
油脂在化学组成上都是由三分子高级脂肪酸和一分子丙三醇(甘油)脱水形成的酯,称为甘油三酯。
油脂的结构可表示为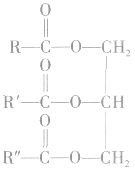
在油脂结构中,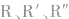 代表高级脂肪酸的烃基,
代表高级脂肪酸的烃基,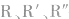 可以相同,也可以不相同。
可以相同,也可以不相同。
油脂的性质:
1、物理性质:纯净的油脂无色、无味,密度比水小,难溶于水,易溶于汽油、乙醚和氯仿等有机溶剂,它的黏度较大,没有恒定的熔沸点。
2、化学性质:
①水解反应
a.在有酸(酶)存在时,油脂水解生成甘油和相应的高级脂肪酸。

b.在有碱存在时,油脂水解生成甘油和相应的高级脂肪酸盐。油脂在碱性溶液中的水解反应又称为皂化反应。
②油脂的氢化
不饱和程度较高、熔点较低的液态油,通过催化加氢,可提高饱和度,转变成半固态的脂肪。由液态的油转变为半周态的脂肪的过程称为油脂的氢化,也称油脂的硬化,如油酸甘油酯通过氢化反应转变为硬脂酸甘油酯: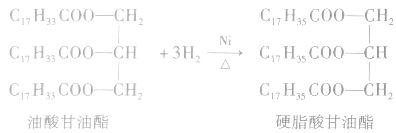
与“下列说法正确的是[ ]A.多肽、油脂、纤维素、淀粉、蔗糖和葡...”考查相似的试题有:
- 对于氯化铁溶液和氢氧化铁胶体,以下说法正确的是 ( )A.分散质粒子直径都在1nm~100nm之间B.分散质微粒都能透过半透膜C....
- 在T℃时,将a gNH3完全溶于水,得到VmL溶液,假设该溶液的密度为ρ g·cm-3,溶质的质量分数为w,其中含NH4+的物质的量为b mol...
- 下列物质中①蔗糖 ②淀粉 ③纤维素 ④蛋白质 ⑤油脂等物质,在稀酸存在的条件下分别进行水解,最后只生成一种产物的是( )A.①②...
- 下列说法错误的是 ( )A.乙醇可以由玉米制取B.鸡蛋清中加入CuSO4溶液产生盐析C.煤的气化可以得到水煤气D.石油分馏可获得...
- 下列说法,不正确的是( )A.糖类摄入不足,人易患低血糖;而摄入过多,则可能引发动脉硬化、冠心病等疾病B.某些植物油和鱼...
- 下列关于蛋白质的说法错误的是( ) A.蛋白质是生命的基础,没有蛋白质就没有生命B.任何一种蛋白质只含有碳、氢、氧、氮四种元...
- 若液氨相当于地球上的水,它可满足木星上生物生存的需要,那么木星上生物体内与地球上生物体内葡萄糖的分子结构相当的化合物...
- A.淀粉属于天然有机高分子化合物B.遇I-能变蓝色C.淀粉不溶于冷水D.淀粉在人体内能够水解生成葡萄糖,经肠壁吸收进入血液
- 中华民族有着有别于其他民族的饮食方式,以五谷杂粮为主,水果菜蔬必不可少。下列说法不正确的是( )A.糖类摄入不足,人易患...
- 科学家发现某药物M能治疗心血管疾病是因为它在人体内能释放出一种“信使分子”D,并阐明了D在人体内的作用原理,为此他们荣获了...