本试题 “在一个固定的反应器中,有一可以自由滑动的密封隔板,两侧分别进行如图所示的化学反应(均加有适量的新型固体催化剂,体积忽略).2SO2(g)+O2(g)⇌2SO3(g...” 主要考查您对化学平衡的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学平衡的有关计算
化学平衡计算的一般思路和方法:
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g) pC(g)+ qD(g)
pC(g)+ qD(g)
(1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
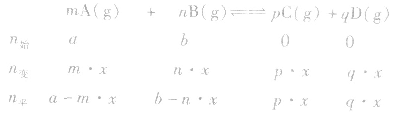
则有:

(2)对于反应物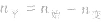 ,对于生成物
,对于生成物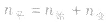
(3)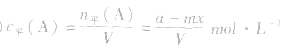
(4)A的转化率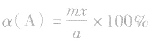
(5)平衡时A的体积(物质的量)分数
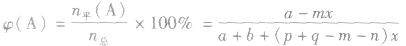
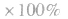
(6)
(7)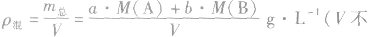
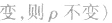
(8)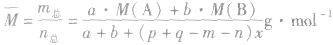
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g)
 pC(g)+ qD(g)
pC(g)+ qD(g) (1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
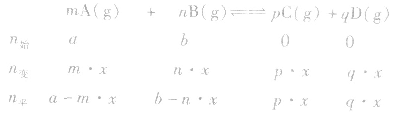
则有:

(2)对于反应物
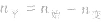 ,对于生成物
,对于生成物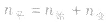
(3)
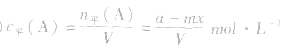
(4)A的转化率
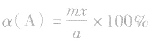
(5)平衡时A的体积(物质的量)分数
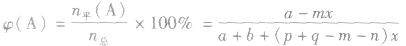
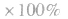
(6)

(7)
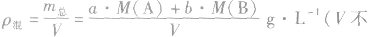
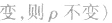
(8)
发现相似题
与“在一个固定的反应器中,有一可以自由滑动的密封隔板,两侧分...”考查相似的试题有:
- 相同温度下,在体积相等的三个恒容密闭容器中发生可逆反应:N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1。实验测得起始、平...
- 下列说法中正确的是A.从平衡常数的大小可以推断任意反应进行的程度B.对同一反应,K值越大,反应的转化率越大C.K值越大,反...
- (6分)在温度为830°K时,下列可逆反应具有某些特殊性质:CO+H2OH2+CO2若起始浓度[CO]为2mol/L、[H2O]=3mol/L,反应达到平衡...
- 在一密闭容器中反应mA(g)⇌nB(g)+nC(g)达到平衡.保持温度不变,将容器体积压缩到原来的一半,当达到新的平衡时,B和C的...
- 在体积不变的密闭容器中发生的反应是CO(g)+H2O(g)CO2(g)+H2(g)下列情况中,能说明反应达到化学平衡状态的是A.混合气体的密度...
- (6分)1 000 ℃时,在密闭容器中加入一定量的Na2SO4固体使其发生以下反应达到平衡:Na2SO4(s)+4H2(g)Na2S(s)+4H2O(g)...
- 质的量随时间变化的关系如图1,达平衡后在t1、t2、t3、t4时都只改变了一种条件,逆反应速率随时间变化的关系如图2。下列有关...
- (8分) 一定温度下,将2mol SO2气体和1mol O2气体通过一密闭容器中,发生如下反应:2SO2(g)+O2 (g)2SO3(g)。请填写下列空白...
- 对于可逆反应,当平衡向正反应方向移动时,下列说法一定正确的是A.反应物的转化率提高B.生成物的产量增加C.生成物的浓度增大...
- 为了探索外界条件对反应:aX(g)+bY(g)cZ(g)的影响,将X和Y以物质的量之比为a:b开始反应,通过实验得到不同条件下达到平衡时Z...