本试题 “下列有关说法错误的是( )A.H2O、NH3、CH4分子的中心原子均为SP3杂化轨道类型B.P、S、Cl元素的最高化合价依次升高C.N、O、F电负性依次增大D.Na、K、Rb第...” 主要考查您对杂化轨道理论(中心原子杂化方式)
元素周期表
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 杂化轨道理论(中心原子杂化方式)
- 元素周期表
杂化轨道理论:
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
是鲍林为了解释分子的立体结构提出的。中心原子杂化轨道、孤电子对数及与之相连的原子数间的关系是:杂化轨道数=孤电子对数+与之相连的原子数。杂化前后轨道总数比变,杂化轨道用来形成σ键或容纳孤对电子,未杂化的轨道与杂化轨道所在平面垂直,可用来形成π键。
常见杂化方式:
(1)sp杂化:直线型 如:CO2、CS2
(2)sp2杂化:平面三角形(等性杂化为平面正三角形) 如:BCl3 C2H4
不等性杂化为V字型 如:H2O H2S OF2
(3)sp3杂化:空间四面体(等性杂化为正四面体) 如:CH4、CCl4
不等性杂化为三角锥 如:NH3 PCl3 H3O+
sp3d杂化:三角双锥
sp3d2杂化:八面体(等性杂化为正八面体)
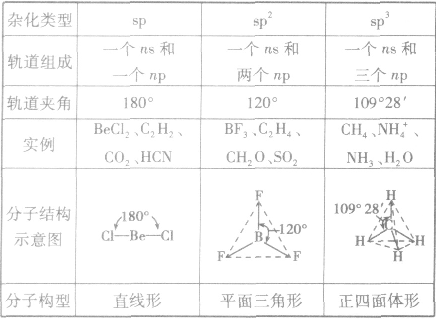
分子的构型与杂化类型的关系:
元素周期表编排原则:
(1)把电子层数相同的各种元素按原子序数递增的顺序从左至右排成横行。
(2)把最外层电子数相同的元素按电子层数递增的顺序由上到下排列成纵行。
注意:①元素周期表是元素周期律的具体表现形式,它反映了元素之间相互联系的规律。
②历史上第一个元素周期表是1869年俄国化学家门捷列夫在前人探索的基础上排成的,他将元素按相对原子质量由小到大依次排列,并将化学性质相似的元素放在一个纵行。
元素周期表的结构:
(1)周期
①周期的含义在元素周期表中,把电子层数相同的元素,按原子序数递增的顺序从左到右排成横行,这样每个横行为一个周期。现在使用的元素周期表有7个横行,即7 个周期。
②周期的划分
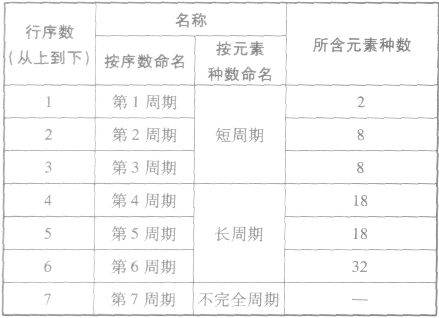
(2)族
①族的含义在周期表中,把不同横行(即周期)中最外层电子数相同的元素,按电子层数递增的顺序由上到下排成纵行,除第8、9、10三个纵行叫做第Ⅷ族外,其余15个纵行,每个纵行为一族。现在使用的元素周期表有18 个纵行,它们被划分为16个族。
②族的划分
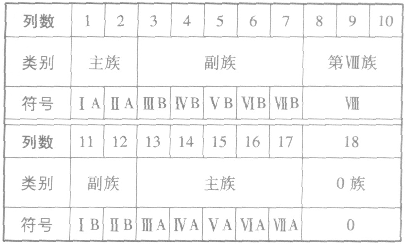
(3)元素周期表中主族元素金属性和非金属性的递变
发现相似题
与“下列有关说法错误的是( )A.H2O、NH3、CH4分子的中心原子均...”考查相似的试题有:
- A.乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。(1) CaC2中C22-与O22+互为等电子体,O22+的电子式可表...
- A、B两元素为某周期ⅡA族和ⅢA族元素,若A元素的原子序数为m,则B元素的原子序数可能为①m+1 ②m+10 ③m+11 ④m+18 ⑤m+25 ⑥m+32( ...
- 历史上第一个绘制出元素周期表的人是谁?( )A.戴维B.门捷列夫C.阿伏加德罗D.候德榜
- 有A、B、C、D四种元素,其中A为第四周期元素,与D可形成原子个数比为1:1和1:2的化合物。B为第四周期d区元素,最高化合价为+...
- 下列关于金属元素的特征的叙述:①金属元素在化合物中显正价,②金属元素只有金属性,没有非金属性,③金属元素的原子只有还原性...
- 下列不能证明氯的非金属性比硫强的实验是( )A.HCl比H2S稳定B.HCl溶液(盐酸)的酸性比H2S溶液(氢硫酸)的酸性强C.氯水...
- 下表是元素周期表的一部分,回答下列有关问题:族周期ⅠAⅡAⅢAⅣAⅤAⅥAⅦAⅧ2①②3③④⑤⑥⑦⑧⑨(1)写出下列元素符号:①______;②______(...
- 下列元素中,属于第三周期IIA族元素的是( )A.镁B.铝C.氧D.硫
- 下列有关现在的长式元素周期表的判断中正确的是( )A.从左向右数第七纵行是ⅦA族B.从左向右数第十一纵行是ⅠB族C.ⅠA族全部...
- 短周期元素W、X、Y、Z在元素周期表中的位置关系如图所示.下列说法正确的是( )A.元素Y的最高价氧化物对应水化物的酸性比Z...