本试题 “某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度,设计了如下活动过程,请完成表中空格:(已知CaSO4在水中微溶,CaCO3在水中难溶)实验步骤向3-...” 主要考查您对化学反应进行的方向
可逆反应与不可逆反应
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应进行的方向
- 可逆反应与不可逆反应
化学反应的方向与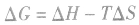 :
:
1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如 ,稳定性
,稳定性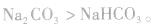
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如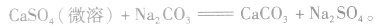
②由相对强酸(碱)向相对弱酸(碱)转变,如 ,
,  所以酸性强弱:
所以酸性强弱: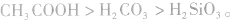
(3)由难挥发性物质向易挥发性物质转变
如 所以沸点:
所以沸点: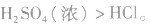
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如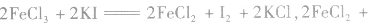
 ,则氧化性:
,则氧化性: 。
。
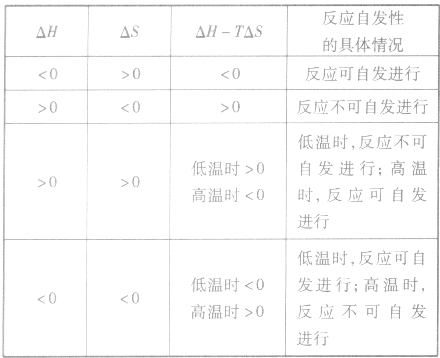
2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向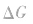
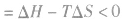 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;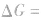
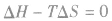 表明反应已达到平衡状态;
表明反应已达到平衡状态;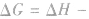
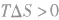 表明反应不能自发进行。
表明反应不能自发进行。
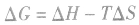 :
:1.化学反应进行方向的判据
(1)由稳定性弱的物质向稳定性强的物质转变
如
 ,稳定性
,稳定性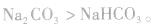
(2)离子反应总是向着使反应体系中某些离子浓度减小的方向进行
①溶解度大的物质向溶解度小的物质转变,如
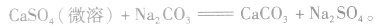
②由相对强酸(碱)向相对弱酸(碱)转变,如
 ,
,  所以酸性强弱:
所以酸性强弱: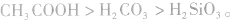
(3)由难挥发性物质向易挥发性物质转变
如
 所以沸点:
所以沸点: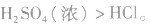
(4)由氧化性(还原性)强的物质向氧化性(还原性)弱的物质转变
如
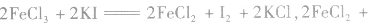
 ,则氧化性:
,则氧化性: 。
。 2.焓变和熵变共同判断反应的方向:
在温度、压强一定的条件下,自发反应总是向
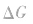
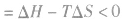 的方向进行,直至达到平衡状态;
的方向进行,直至达到平衡状态;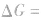
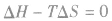 表明反应已达到平衡状态;
表明反应已达到平衡状态;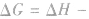
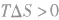 表明反应不能自发进行。
表明反应不能自发进行。
可逆反应与不可逆反应:
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
(1)可逆反应:在同一条件下,既能向正反应方向进行,同时又能向逆反应方向进行的反应。
注:①在可逆反应中,由反应物到生成物的反应叫正反应;由生成物到反应物的反应叫逆反应。
②可逆反应必须是“同一条件”。
(2)不可逆反应:在不同条件下能向两个方向进行的反应为不可逆反应。如:点燃情况下,氢气和氧气能生成水;在通电条件下,水电解能生成氢气和氧气。
可逆反应的特点:
①可逆反应必须是同一条件下既能向正反应方向又能向逆反应方向进行的反应,对于在不同条件下向正、逆反直方向进行的反应则不能认为是可逆反应。
②可逆反应是不能进行到底的,不能实现完全转化
发现相似题
与“某化学课外小组为了探究CaCl2溶液和Na2SO4溶液反应有没有限度...”考查相似的试题有:
- 下列对于化学反应方向说法正确的是 ( )A.反应2A(g)+B(g) =" 3C" (s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0B.常...
- 下列反应中,在高温下不能自发进行的是( )A.CO(g)C(s)+O2(g)B.NH4Cl(s)NH3(g)↑+HCl(g)↑C.(NH4)2CO3(s)NH4HCO3(s)+NH3(g)D....
- 物质(t-BuNO)2在正庚烷溶剂中发生如下反应:(t-BuNO)22(t-BuNO) 。(1)当(t-BuNO)2的起始浓度(c0)为0.50 mol·L-1时,实验...
- Ⅰ、某温度时,在2L密闭容器中将1molNO2分解:2NO22NO+O2,达到平衡时,NO的物质的量为0.5mol。平衡时O2的浓度是_______,NO的...
- 高温下14CO2与碳发生反应:14CO2+C2CO达到平衡后,平衡混合物中含14C的粒子有 A.14CO214CO14CB.14CO214COC.14CO2D.14CO
- 下列叙述中,不正确的是A.在相同条件下,焓变小于0而熵变大于0的反应肯定能自发进行B.升高温度会加快化学反应速率,其原因...
- 下列有关描述错误的是[ ]A.铝既能与盐酸反应,又能与氢氧化钠溶液反应,说明铝既有氧化性又有还原性B.在所有氧化还原反应中...
- 现用18O作为示踪原子进行如下反应:2SO2(g)+18O2(g)2 SO3(g),则当反应达到平衡后18O原子存在于哪种物质中[ ]A.O2B.S...
- 下图是可逆反应X2+ 3Y22Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是[ ]A.t1时,只有正方向反应B...
- 已知298时,2SO2(g)+O2(g)2SO3(g);△H = -197kJ·mol-1。在相同温度和压强下,向密闭容器中通入2molSO2和1molO2,达到平衡时放...