本试题 “2010上海世博会,来自全球的189个国家和57个国际组织实际参展,“绿色、低碳、可持续”等环保元素及多种节能技术在世博会这个大舞台上得到充分的体现.请回答:...” 主要考查您对氢气的用途
化学反应方程式的书写
文字表达式
自然界中的碳循环
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氢气的用途
- 化学反应方程式的书写
- 文字表达式
- 自然界中的碳循环
氢气的用途:
| 氢气的性质 | 氢气的用途 |
| 密度最小的气体 | 填充气球 |
| 燃烧放出大量的热 | 做高能燃料;作为新能源 |
| 还原性 | 冶炼金属;做保护气;制高纯硅 |
| 和多种物质反应 | 做化工原料,如制HCl,NH3等 |
化学方程式的书写原则遵循两个原则:
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。
化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。
③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3 CaO+ CO2↑
CaO+ CO2↑
(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2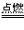 CO2
CO2
(3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2 2CuO
2CuO
④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2
 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
| 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。 ③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3
 CaO+ CO2↑
CaO+ CO2↑(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2
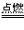 CO2
CO2 (3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2
 2CuO
2CuO ④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
概念:用文字表示化学反应的式子
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
文字表达式的书写步骤:
(1)写:根据反应事实写出反应物和生成物
(2)注:注明反应条件:[点燃,加热,光照,通电等]
碳循环:
生物圈中的碳循环主要表现在绿色植物从空气中吸收二氧化碳,经光合作用转化为葡萄糖,并放出氧气(O2)。
碳循环的描述:
碳循环是维持地球表层生命活动的主要物质循环。地球表层系统中的碳,绝大部分
以沉积物的形式储存在岩石圈中的储存库里。储存库中的碳,以碳水化合物的形式
存在于有机物质中(如岩石中的石油、天然气、煤),或以无机物的形式存在于矿
物碳酸盐中(如碳酸钙)。储存库里的碳,一般情况下是不参加碳循环的,除非岩
石被风化,化石燃料被利用,或火山活动将其以CO2和CO的形式带到大气中。大气
活性库中的碳,不到全部碳的2%。它主要是通过生物的呼吸作用来补充的,火山喷
发、人类燃烧化石燃料也是重要的来源。植物光合作用吸收大气中的CO2,生产有机
化合物,然后通过食物链传递。海洋中的浮游植物还可以直接生成碳酸盐骨骼。生物
死亡后,生物体沉降到海底形成沉积层。海洋浮游植物生成的有机质,同样也沉降到
海底,最终转变成石油和天然气。在适宜的地质条件下,陆地上的植物积累形成泥炭,
这种泥炭可以转变成煤、石油、天然气和煤被称为化石燃料,是碳的巨大储藏库。当
这些化石燃料被发掘、利用,燃烧生成的CO2和CO又会释放到大气中,参与碳循环。
碳的循环示意图:
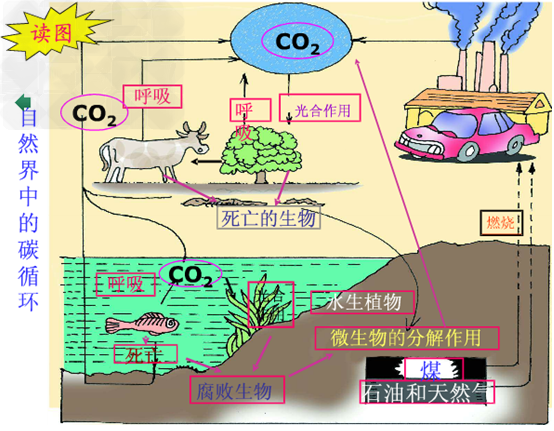
产生及消耗二氧化碳的途径:
(1)自然界消耗二氧化碳的途径:光合作用
(2)自然界产生二氧化碳的途径:
①主要途径:化石燃料的燃烧
②次要途径:呼吸作用,微生物的分解作用
生物圈中的碳循环主要表现在绿色植物从空气中吸收二氧化碳,经光合作用转化为葡萄糖,并放出氧气(O2)。
碳循环的描述:
碳循环是维持地球表层生命活动的主要物质循环。地球表层系统中的碳,绝大部分
以沉积物的形式储存在岩石圈中的储存库里。储存库中的碳,以碳水化合物的形式
存在于有机物质中(如岩石中的石油、天然气、煤),或以无机物的形式存在于矿
物碳酸盐中(如碳酸钙)。储存库里的碳,一般情况下是不参加碳循环的,除非岩
石被风化,化石燃料被利用,或火山活动将其以CO2和CO的形式带到大气中。大气
活性库中的碳,不到全部碳的2%。它主要是通过生物的呼吸作用来补充的,火山喷
发、人类燃烧化石燃料也是重要的来源。植物光合作用吸收大气中的CO2,生产有机
化合物,然后通过食物链传递。海洋中的浮游植物还可以直接生成碳酸盐骨骼。生物
死亡后,生物体沉降到海底形成沉积层。海洋浮游植物生成的有机质,同样也沉降到
海底,最终转变成石油和天然气。在适宜的地质条件下,陆地上的植物积累形成泥炭,
这种泥炭可以转变成煤、石油、天然气和煤被称为化石燃料,是碳的巨大储藏库。当
这些化石燃料被发掘、利用,燃烧生成的CO2和CO又会释放到大气中,参与碳循环。
碳的循环示意图:

产生及消耗二氧化碳的途径:
(1)自然界消耗二氧化碳的途径:光合作用
(2)自然界产生二氧化碳的途径:
①主要途径:化石燃料的燃烧
②次要途径:呼吸作用,微生物的分解作用
发现相似题
与“2010上海世博会,来自全球的189个国家和57个国际组织实际参展...”考查相似的试题有:
- (3分)按要求写出下列名称或符号。(1) 3个氮分子 ; (2) 2H ; (3) 4个硫酸根离子 。
- 某校化学兴趣小组学生对“金属活动性顺序”从内容、规律以及应用等方面进行了总结。请你认真填写下列空白:(1)金属活动性顺序...
- ______叫化合反应,如______(写文字表达式)属于化合反应;______叫分解反应,如______(写文字表达式)属于分解反应.
- (10天津市17).化学是一门实用性很强的科学,应用所学的化学知识能帮助我们解释许多问题。例如:(1)用适量的稀硫酸可以除...
- 根据下列要求,写出有关反应的化学方程式,并回答有关问题。(1)有黑色固体生成的化合反应 _________, 该反应是__________ (...
- (1)25℃时,将a g碳酸钠(化学式为Na2CO3)溶解于100g水中恰好形成饱和溶液。所得溶液的溶质质量分数为 ,此温度下碳酸钠的...
- 河南中牟县是全国闻名的大蒜生产基地。大蒜具有一定的抗病功能和食疗价值。每100克含挥发油约0.2%,油中主要成分为大蒜辣素(C...
- 完成下列化学反应方程式,并简答有关问题:化学反应化学反应方程式简答实验室制取氧气______反应类型:______一氧化碳在空气...
- 春天去郊游野炊是件快乐之事.然而,在野炊中,如果遇到下面一些问题,你是如何处理的?(1)在引燃细枯枝后,小丽迅速往“灶”...
- 碳酸钠与盐酸反应生成氯化钠、水和二氧化碳:______.