本试题 “下列说法中正确的是[ ]A.常温下,某溶液中由水电离的c(OH-)=1×10-13mol/L,则该溶液为NH4Cl溶液或NaOH溶液B.25℃时,浓度均为1 mol/L的KHCO3和K2CO3溶液中,...” 主要考查您对水的电离平衡
溶液的酸碱性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 水的电离平衡
- 溶液的酸碱性
水的电离:
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
水是一种极弱的电解质,可以发生微弱电离,电离方程式为:H2O
 H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L
H++OH-。25℃时,水电离出来的c(H+)=c(OH-)=10-7mol/L 注:水的电离是永恒存在的,不研究水溶液的体系中均存在水的电离平衡,不要忽略H+和OH-共同存在。
溶液的酸碱性:
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
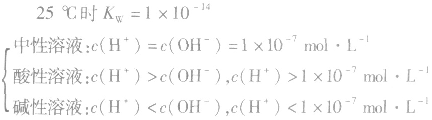
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
(1)pH=-lg[c(H+)],在溶液的c(H+)很小时,用pH来表示溶液的酸度。
(2)pH越大,c(H+)越小,c(OH-)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
(3)pH的范围:0~14
(4)溶液酸碱性判断:
当c(H+)>c(OH-)时,溶液呈酸性;
当c(H+)>=c(OH-)时,溶液呈键性;
当c(H+)<c(OH-)时,溶液呈中性。
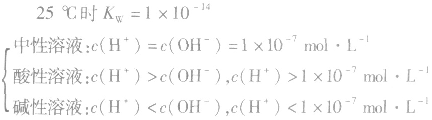
(5)关于pH相同的酸(含强酸和弱酸)
①溶液中c(H+)相等(填“相等”或“不等”)。
②溶液中溶质的物质的量的浓度:强酸<弱酸(填“>”或“<”)。
③耗碱规律:pH和溶液体积均相同的HCl、H2SO4、CH3COOH与碱完全反应时,消耗碱物质的量最多的是CH3COOH。
④稀释规律:分别加水稀释m倍时,溶液的物质的量的浓度均变为原来的1/m,强酸中c(H+)变为原来的1/m,但弱酸中c(H+)减小小于(填“大于”或“小于”)m倍,故稀释后弱酸酸性强于强酸。
溶液的pH:
1.定义:溶液里H+的物质的量浓度的负对数叫做pH。
2.表达式:
3.含义: pH越大,c(H+)越小,c(O-一)越大,酸性越弱,碱性越强。pH越小,c(H+)越大,c(OH-)越小,酸性越强,碱性越弱。
4.适用范围:
c(H+)很小时,用pH来表示溶液的酸碱度更方便。所以,pH适用于酸、碱的稀溶液
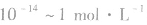 之间],pH取值范刚为0~14。
之间],pH取值范刚为0~14。
5.溶液的酸碱性和pH: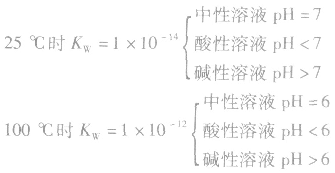
发现相似题
与“下列说法中正确的是[ ]A.常温下,某溶液中由水电离的c(OH-)=...”考查相似的试题有:
- 下列说法中正确的是A.同时含有分子和离子的电解质溶液,一定是弱电解质溶液B.pH=3的盐酸中,其c(H+)是pH=1的盐酸中的3倍C....
- 欲测定某NaOH溶液的物质的量浓度,可用0.1000mol·L-1HCl标准溶液进行中和滴定(用甲基橙作指示剂)。请回答下列问题:(1)滴...
- 下列叙述正确的是[ ]A.常温下pH=12的烧碱和pH=2的盐酸溶液等体积混合,混合液的pH =7B.pH相同氨水和烧碱溶液稀释相同倍数时...
- ㈠(2分)用pH试纸测定溶液pH的正确操作是______________________________________㈡(7分)某校学生用中和滴定法测定某NaOH...
- 常温下,将v1mL c1mol·L-1的氨水逐滴滴加到v2mL c2mol·L-1的盐酸中,下列结论中正确的是( )。A.若v1=v2 c1=c2,则混...
- 能使电离平衡H2OH++OH-向右移动,且使溶液呈酸性的是( )A.向水中加入少量硫酸氢钠固体B.向水中加入少量硫酸铝固体C.向...
- 现用pH=3的CH3COOH溶液和pH=11的NaOH溶液各VmL,进行中和滴定,当滴定到pH=7时,锥形瓶内溶液的体积为(滴定前后溶液未稀释...
- pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH-浓度分别为amol·L-1与bmol·L-1,则a和b的关系为A.a>bB.a=10...
- A.①④B.①③C.②④D.②③
- 250 mL pH=12的某一元强碱(MOH)溶液与250 mL 0.025 mol·L-1的硫酸溶液相混合,假设混合后液体体积为500 mL。试求:(1)混合...