本试题 “为保证鱼苗长距离顺利运输,必须满足三个条件:①保持适量的氧气;②及时排出鱼苗呼出的二氧化碳;③水溶液应显弱碱性,防止细菌大量繁殖。在储运鱼苗的水中,最...” 主要考查您对过氧化钠
氨水
过氧化氢
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 过氧化钠
- 氨水
- 过氧化氢
过氧化钠(Na2O2)的基本性质:
淡黄色固体,较稳定,可用作供氧剂、漂白剂
(1)与水反应:2Na2O2+2H2O==4NaOH+O2↑
(2)与CO2反应:2Na2O2+2CO2==2Na2CO3+ O2
(3)与HCl反应:2Na2O2+4HCl==4NaCl+2H2O+ O2↑
过氧化钠的特性及计算:
1.过氧化钠的强氧化性
2.Na2O2与CO2、H2O(g)反应的重要关系
(1)气体体积差的关系
2Na2O2+2CO2===2Na2CO3+O2 气体体积差 ①
2 1 ΔV=1
2Na2O2+2H2O(g)===4NaOH+O2 气体体积差 ②
2 1 ΔV=1
由此可见,若CO2和水蒸气的混合气体(或单一气体)通过足量Na2O2,气体体积的减少量是原气体体积的1/2,即为生成氧气的量。
(2)先后顺序关系
一定量的Na2O2与一定量的CO2和H2O(g)的混合物反应,可视为Na2O2首先与CO2反应,剩余的Na2O2再与H2O(g)反应。
(3)电子转移关系
当Na2O2与CO2或H2O反应时,每产生1molO2就转移2mol电子。
(4)固体质量变化关系
①足量过氧化钠与水、CO2反应的计算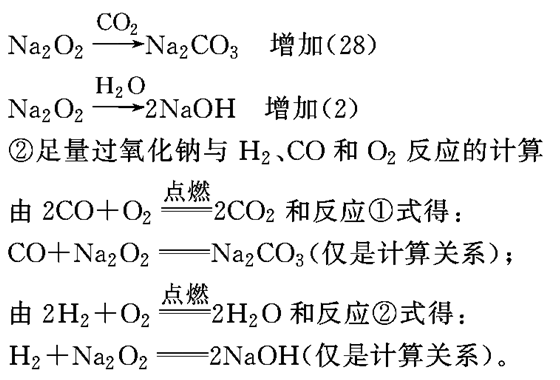
所以,有ag通式符合(CO)m(H2)n(m=0,1,2,3…,n=0,1,2,3…)的物质(包括纯净物和混合物)在氧气中燃烧,将其通过足量过氧化钠,反应完毕后,固体增重ag。
氧化钠与过氧化钠的比较:
| 物质 | 氧化钠 | 过氧化钠 |
| 色态 | 白色固体 | 淡黄色固体 |
| 类别 | 碱性氧化物 |
过氧化物(不属于碱性氧化物) |
| 化学键类型 | 仅含离子键 | 离子键和非极性键 |
| 电子式 | 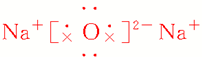 |
 |
| 生成条件 | 常温 | 点燃或加热 |
| 氧的化合价 | -2 | -1 |
| 阴阳离子个数比 | 1:2 | 1:2 |
| 稳定性 | 不稳定 | 稳定 |
| 转化关系 | 2Na2O+O2=2Na2O2 | |
| 用途 | 用于制取少量过氧化钠 | 供氧剂、漂白剂、氧化剂 |
| 与水反应方程式 | 2Na2O+2H2O=2NaOH | 2Na2O2+2H2O=4NaOH+O2↑ |
| 与CO2反应 | Na2O+CO2=NaCO3 | 2Na2O2+2CO2=2Na2CO3+O2↑ |
| 与HCl反应 | Na2O+2HCl=2NaCl+H2O | 2Na2O2+4HCl=4NaCl+2H2O+O2↑ |
| 保存 | 隔绝空气、密封保存 | 隔绝空气、远离易燃物、密封保存 |
特别提醒:
(1)用脱脂棉包裹住过氧化钠,滴加少量水时脱脂棉可以燃烧,不仅可以说明Na2O2与H2O反应生成O2,还可以说明该反应放热。
(2)Na2O2与H2O反应时H2O既不是氧化剂也不是还原剂。
方法技巧:Na2O与Na2O2的结构与性质
(1)Na2O中只含离子键,Na2O2中既含离子键,又含非极性键。
(2)等物质的量的Na2O与Na2O2分别于等量且足量的H2O反应,所得溶液的成分浓度相同
氨水:
(1) 浓氨水:易挥发,密度小于水,浓度越大,密度越小,无色,有刺激性气味的液体,熔沸点较低,能导电
(2)氨水是混合物(液氨是纯净物),其中含有3种分子(NH3、NH3·H2O、H2O)和3种离子(NH4+和OH-、极少量的H+)。
氨水的性质:
①刺激性:因水溶液中存在着游离的氨分子。
②挥发性:氨水中的氨易挥发。
③不稳定性:—水合氨不稳定,见光受热易分解而生成氨和水。
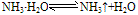
④弱碱性:氨水中一水合氨能电离出OH-,所以氨水显弱碱性,具有碱的通性:
A. 能使无色酚酞试液变红色,能使紫色石蕊试液变蓝色,能使湿润红色石蕊试纸变蓝。实验室中常见此法检验NH3的存在。
B. 能与酸反应,生成铵盐。浓氨水与挥发性酸(如浓盐酸和浓硝酸)相遇会产生白烟。

而遇不挥发性酸(如硫酸、磷酸)无此现象。实验室中可用此法检验NH3或氨水的存在。
工业上,利用氨水的弱碱性来吸收硫酸工业尾气,防止污染环境。
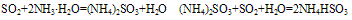
C. 沉淀性:氨水是很好的沉淀剂,它能与多种金属离子反应,生成难溶性弱碱或两性氢氧化物。例如:
生成的Al(OH)3沉淀不溶于过量氨水。
生成的白色沉淀易被氧化生成红褐色沉淀

利用此性质,实验中可制取Al(OH)3、Fe(OH)3等。
D. 络合性:氨水与Ag+、Cu2+、Zn2+三种离子能发生络合反应,当氨水少量时,产生不溶性弱碱或两性氢氧化物,当氨水过量时,不溶性物质又转化成络离子而溶解。
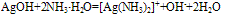
实验室中用此反应配制银氨溶液。
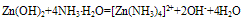
可用此反应来鉴别两性氢氧化物氢氧化铝和氢氧化锌。

现出弱的还原性,可被强氧化剂氧化。如氨水可与Cl2发生反应:
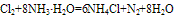
(4)氨水的保存方法:氨水对许多金属有腐蚀作用,所以不能用金属容器盛装氨水.通常把氨水盛装在玻璃容器、橡皮袋、陶瓷坛或内涂沥青的铁桶里。
氨水,液氨和一水合氨的比较:
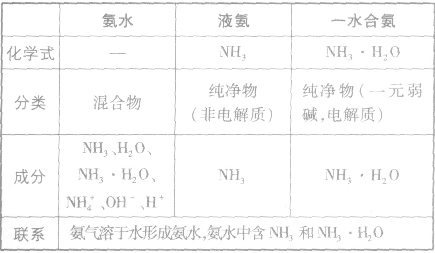
过氧化氢:
俗称,双氧水,基本结构为H-O-O-H,但并不是直线结构,因此有极性,是极性分子;O上有孤电子对,因此O-O键很弱易断。
过氧化氢和水的性质比较:


与“为保证鱼苗长距离顺利运输,必须满足三个条件:①保持适量的氧...”考查相似的试题有:
- 一定量碳酸氢钠与过氧化钠的混合物在密闭体系中充分加热后,排出气体,测出固体残留物中有两种成分,则该固体组成中一定含有( ...
- (7分)自2009年3月起,从墨西哥、美国等国逐渐扩散到全世界的甲型H1N1型流感暴发疫情,引起了全球关注和积极应对。防控专家...
- (13分)过氧化钠(化学式为NaNa2O2)可用在呼吸面具中作为氧气来源。Na2O2能跟CO2反应生成O2和另一种固体化合物(用X表示);它也...
- A、B、C是周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如下的关系:试完成下列...
- 试设计一套实验方案验证某白色粉末是纯碱。
- 下列各组比较不正确的是( )A.熔点:Li>Na>KB.碱性:LiOH>NaOH>KOHC.还原性:K >Na>LiD.氧化性:Cs+>Rb+>K+
- 金属钾与金属钠的金属性相近,且钾比钠略强。当利用金属钾与钠盐共熔制金属钠时,发现钾与钠的共熔体难以分离。如调整温度到...
- 某些金属氧化物跟熔融烧碱反应生成盐。根据以下化学反应框图填空(1)单质F是______________。(2)写出由E生成G的离子反应方...
- 如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是[ ]A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色B.若A为醋...
- 氧族元素的各种性质可归纳如下(部分):回答下列问题(1)氧离子的结构示意图_________,H2S的电子式__________(2)Te 的主...