本试题 “下图是组成生物体的某种物质,请分析完成下列问题:(1)A由_________等元素组成。(2)B的名称叫_________,其结构通式是_____________。(3)C是_________,其作...” 主要考查您对细胞中的元素
氨基酸
蛋白质的结构
蛋白质的功能
各种酶的作用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 细胞中的元素
- 氨基酸
- 蛋白质的结构
- 蛋白质的功能
- 各种酶的作用
(1)元素种类:
大量元素:C、H、O、N、P、S、K、Ca、Mg等
微量元素:Zn、Mo、Cu、B、Fe、Mn
(2)分类依据:大量元素
 按照含量占生物总质量万分之一
按照含量占生物总质量万分之一 微量元素
微量元素 生物界与非生物界的关系:
组成生物体的元素在非生物界都能找到,但是含量相差很大,体现了生物界与非生物界的差异性。
| 统一性 | 差异性 | |
| 体现 | ①生物界与非生物界都是由化学元素组成的 ②组成细胞的化学元素在无机自然界中都能找到,没有一种元素为细胞所特有 |
组成生物体的化学元素,在生物体内和无机自然界中含量相差很大 |
| 原因 | ①生命起源于非生物界 ②组成生物体的化学元素是从无机自然界中获取的 |
生物体有选择性地从无机自然界获取组成自身的物质 |
元素的特性:
微量元素在生物体内的含量虽然很少,但对生物体的生命活动却起着重要作用;
(1)锌和铁是微量元素,可以从食物中获得,如果刻意去补,可能会对身体有害。硼能影响花粉的萌发和花粉管的伸长,缺硼将产生“花而不实”的现象。
(2)植物缺乏锌元素,会影响生长素(IAA)的生成;生长素缺乏时会影响农作物的生长发育;锌为微量元素。
(3)镁元素是构成植物叶绿素的主要元素。
(4)铁是构成动物血红蛋白的主要元素,缺铁会贫血。
(5)碘元素是甲状腺激素的主要元素,成人缺碘会地方性甲状腺肿(大脖子病),小孩缺碘会患呆小症。
知识点拨:
1、细胞无论是干重还是鲜重,组成元素中C、H、O、N这四种元素的含量最多。
2、人体细胞鲜重的元素相对含量:O>C>H>N>P>S;人体细胞干重的元素相对含量:C>O>N>H>Ca>P>S。
3、大量元素和微量元素都是生物体生命活动所必需的,它们是根据含量区分的,不是从功能上划分的。
4、不同的生物,组成它们的化学元素种类大体相同,但各种元素的含量相差很大。
5、鲜重是指生物体(或细胞)在自然生活状态下测得的重量;干重是指生物体(或细胞)除去水以后测得的重量。占人体鲜重最多的元素是O,占人体干重最多的元素是C。
细胞中的元素分类:

C(干重下含量最高)O(鲜重下含量最高)
组成人体细胞的主要元素导图:
氨基酸及其种类:
1.氨基酸的组成元素:C、H、O、N,有的含有S。
2.氨基酸的结构通式:

3.氨基酸的结构特点
(1)氨基和羧基的数目:每个氨基酸都至少含有一个氨基和一个羧基,R基中也可能含有氨基或羧基。
(2)连接位点:构成蛋白质的氨基酸都有一个-NH2和一个-COOH连在同一个碳原子上,此特点为判断某化合物是否是构成蛋白质的氨基酸的依据。
氨基酸的分类及特性:
氨基酸分为必须氨基酸和非必须氨基酸
1、必需氨基酸(essentialaminoacid):指人体(或其它脊椎动物)不能合成或合成速度远不适应机体的需要,必需由食物蛋白供给,这些氨基酸称为必需氨基酸。成人必需氨基酸的需要量约为蛋白质需要量的20%~37%。
共有8种其作用分别是:
赖氨酸:促进大脑发育,是肝及胆的组成成分,能促进脂肪代谢,调节松果腺、乳腺、黄体及卵巢,防止细胞退化;
色氨酸:促进胃液及胰液的产生;
苯丙氨酸:参与消除肾及膀胱功能的损耗;
蛋氨酸(甲硫氨酸):参与组成血红蛋白、组织与血清,有促进脾脏、胰脏及淋巴的功能;
苏氨酸:有转变某些氨基酸达到平衡的功能;
异亮氨酸:参与胸腺、脾脏及脑下腺的调节以及代谢;
脑下腺属总司令部作用于甲状腺、性腺;
亮氨酸:作用平衡异亮氨酸;缬氨酸:作用于黄体、乳腺及卵巢。
2、半必需氨基酸和条件必需氨基酸:
精氨酸:精氨酸与脱氧胆酸制成的复合制剂(明诺芬)是主治梅毒、病毒性黄疸等病的有效药物。
组氨酸:可作为生化试剂和药剂,还可用于治疗心脏病,贫血,风湿性关节炎等的药物。人体虽能够合成精氨酸和组氨酸,但通常不能满足正常的需要,因此,又被称为半必需氨基酸或条件必需氨基酸,在幼儿生长期这两种是必需氨基酸。人体对必需氨基酸的需要量随着年龄的增加而下降,成人比婴儿显著下降。(近年很多资料和教科书将组氨酸划入成人必需氨基酸)
3、非必需氨基酸(nonessentialaminoacid):
指人(或其它脊椎动物)自己能由简单的前体合成,不需要从食物中获得的氨基酸。例如甘氨酸、丙氨酸等氨基酸。
思维拓展:
1、自然界中氨基酸的种类约100种,其中在生物体中组成蛋白质的氨基酸约有20种(8种必需氨基酸),但并非生物体内每一种蛋白质都一定含有20种氨基酸。
2、8种必需氨基酸可用谐音记忆“一(异亮氨酸)家(甲硫氨酸)人来(赖氨酸)写(缬氨酸)两(亮氨酸)三(色氨酸)本(苯丙氨酸)书(苏氨酸)”。
3、儿童必需氨基酸比成人多一种,为组氨酸。
1、蛋白质的结构层次:

2、蛋白质种类多样性的原因:
(1)氨基酸的原因:
①氨基酸的种类不同。
②氨基酸的数目成百上千。
③氨基酸的排列顺序千变万化。
(2)肽链的原因:
肽链的盘曲、折叠方式及其形成的空间结构千差万别。
知识点拨:
1、脱去的水分子中的氢来自氨基和羧基,氧来自羧基。
2、肽键的写法有以下几种,这三种都是正确的。
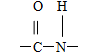 或-CO-NH-或-NH-CO-
或-CO-NH-或-NH-CO- 3、多肽中具体有几个氨基或几个羧基,应关注R基中是否有氨基或羧基。
4、若形成的多肽链是环状:氨基酸数=肽键数=失去水分子数。
5、在蛋白质分子量的计算中若通过图示或其他形式告知蛋白质分子中含有二硫键时,要考虑脱去氢的质量,每形成一个二硫键,脱去2个H。
知识拓展:
氨基酸形成多肽过程中的相关计算
1、蛋白质分子量、氨基酸数、肽链数、肽键数和脱去水分子数的关系
(1)肽键数=脱去水分子数=氨基酸数一肽链数;
(2)蛋白质分子量=氨基酸数目x氨基酸平均相对分子质量一脱去水分子数×18。
| 肽链数目 | 酸数氨基 | 脱去水分子数 | 多肽链分子量 | 氨基数目 | 羧基数目 | |
| 1条 | m | m-1 | m-1 | am-18(m-1) | 至少1个 | 至少1个 |
| 2条 | m | m-n | m-n | am-18(m-n) | 至少n个 | 至少1个 |
2、蛋白质中游离氨基或羧基数的计算
(1)至少含有的游离氨基或羧基数=肽链数
(2)游离氨基或羧基数=肽链数+R基中含有的氨基或羧基数
3、蛋白质中含有N、O原子数的计算 (1)N原子数=肽键数+肽链数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽键数+2×肽链数+R基上的O原子数=各氨基酸中O原子总数一脱去水分子数。
4、巧记氨基酸结构通式让学生把自己身体想象成一个氨基酸分子:中央C原子、头-H原子、右手——氨基(-NH2)左手——羧基(-COOH)、脚-R基(-R)
5、巧记脱水缩合过程 首先由两个人手拉手,一个人出左手拉住另一个人的右手,脱去一分子水,形成二肽。然后再加上一个人,又脱去一分子水,形成三肽,以此类推,形成多肽。
蛋白质的功能:
功能
举例
构成细胞和生物体结构的基本物质
构成动物和人体的肌肉,构成生物膜、核糖体、染色体
构成细胞和生物体的功能物质
催化作用
绝大多数酶是蛋白质
运输作用
红细胞中的血红蛋白、细胞膜上的载体蛋白
运动功能
肌动蛋白和肌球蛋白可使肌肉产生运动
信息传递作用、调节作用
多种激素都能调节生物体的生命活动
免疫作用
生物体内的抗体能消灭外来抗原物质
细胞内的能源物质
在糖类和脂肪被消耗后,机体也会分解蛋白质供能
知识拓展:
1、加热或用乙醇处理可使细菌因蛋白质变性而死亡,从而达到灭菌的目的。
2、吃熟鸡蛋容易消化,是因为高温使蛋白质分子的空间结构变得伸展、松散,易被蛋白酶水解。
例下列叙述中能对蛋白质的功能进行高度概括的是( )
A.细胞和生物体的重要结构物质
B.收缩、运输、免疫等生理活动的物质基础
C.生命活动的主要承担者
D.调节细胞和生物体新陈代谢的重要物质
答案C
酶(enzyme)催化特定化学反应的蛋白质、RNA或其复合体。是生物催化剂,能通过降低反应的活化能加快反应速度,但不改变反应的平衡点。绝大多数酶的化学本质是蛋白质。具有催化效率高、专一性强、作用条件温和等特点。
常见酶:
(1)淀粉酶:作用是催化淀粉水解为麦芽糖。按其产生部位分为唾液淀粉酶、胰淀粉酶、肠淀粉酶和植物淀粉酶。(淀粉遇碘变蓝)
(2)麦芽糖酶:作用是催化麦芽糖水解成葡萄糖,主要分布在发芽的大麦中。
(3)蔗糖酶:作用是催化蔗糖水解成葡萄糖和果糖,主要分布在甘蔗等生物体内。
(4)脂肪酶:作用是催化脂肪水解为脂肪酸和甘油。在动物体内分为胰脂肪酶和肠脂肪酶等。在动物的胰液、血浆和植物的种子中均有分布。
(5)蛋白酶:作用是催化蛋白质水解为短肽。在动物体内分为胰蛋白酶和胃蛋白酶等。在动物的胰液、胃液,植物组织和微生物中都有分布。
(6)纤维素酶:作用是催化纤维素水解成葡萄糖。在真菌、细菌和高等植物中含有。
(7)溶菌酶:广泛存在于动植物、微生物及其分泌物中,能溶解细菌细胞壁中的多糖,可使细菌失活。还可激活白细胞的吞噬功能,增强机体抵抗力。
(8)固氮酶:能使大气中的氮还原为氨,由两种含金属的蛋白质组成,一种为铁蛋白,另一种为钼铁蛋白。根瘤菌、蓝藻和土壤中各种固氮菌中都含有此酶。
(9)限制酶―磷酸二酯键、解旋酶―碱基间氢键、ATP水解酶―高能磷酸键、蛋白酶―肽键。
与“下图是组成生物体的某种物质,请分析完成下列问题:(1)A由___...”考查相似的试题有:
- 在高等植物细胞中有两种大量元素,淀粉中不含有,核酸中含有。关于这两种元素的相关叙述中,错误的一项是[ ]A.这两种元素是...
- 当红细胞内铁元素的含量降低时,其血红蛋白减少,红细胞运输氧气的功能相应地减弱,导致贫血的发生。这一事实说明了铁元素在...
- 想一想,氨基酸发生脱水缩合反应生成的水分子中氢原子和氧原子的来源?
- 苏云金芽孢杆菌是一种对昆虫有致病作用的细菌,其杀虫活性物质是一类伴孢晶体蛋白。某种苏云金芽孢杆菌所产生的伴孢晶体蛋白...
- 据下图回答下列问题:(1)图中A表示________,D表示________。(2)该化合物是由_____个氨基酸分子失去_____个分子的水形成的,...
- 狼体内有a种蛋白质,20种氨基酸,兔体内有b种蛋白质,20种氨基酸。狼捕食兔后,狼体内的一个细胞中含有的蛋白质种类和氨基酸...
- 牛胰岛素由两条肽链构成,共有51个氨基酸。则牛胰岛素含有的肽键数以及控制其合成的基因至少含有的脱氧核苷酸数目依次是[ ]A...
- 下图表示一个由153个氨基酸构成的蛋白质分子。下列叙述正确的是[ ]A.该分子中含有152个肽键B.参与构成该分子的氨基酸中至少...
- 分析一条多肽链E和一条多肽链F得到以下结果(单位:个)推测组成两条多肽链氨基酸的数目最可能是[ ]A.多肽链E:199 多肽链F:1...
- 在进行植物细胞融合实验时,要除去细胞壁,最好应选择[ ]A.淀粉酶和果胶酶B.蛋白质和纤维素酶C.纤维素酶和果胶酶D.盐酸