本试题 “如图所示,将密闭的相互连通的装置放在天平上,调节天平使之平衡。经过一段时间后,下列有关叙述正确的是[ ]A.指针偏左,食盐溶液一定变稀,烧碱潮解B.指针...” 主要考查您对饱和溶液,不饱和溶液
物质的变质
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 饱和溶液,不饱和溶液
- 物质的变质
饱和溶液和不饱和溶液的概念:
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液 不饱和溶液
不饱和溶液
(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水 不饱和石灰水
不饱和石灰水
概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)
溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液 饱和溶液
饱和溶液
溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)
溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液 不饱和溶液
不饱和溶液
溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
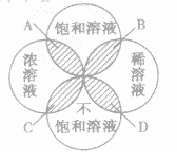 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
①饱和溶液:在一定温度下,在一定量的溶剂里,不能再溶解某种溶质的溶液,
叫做这种溶质的饱和溶液
②不饱和溶液:在一定温度下,在一定量的溶剂里,还能再继续溶解某种溶质的溶液,
叫做这种溶质的不饱和溶液
饱和溶液与不饱和溶液的相互转化方法:
(1)对于大多数固体:在一定量的水中溶解的最大量随温度升高而增大
饱和溶液
 不饱和溶液
不饱和溶液(2)对于Ca(OH)2:在一定量的水中溶解的最大量随温度升高而减少
饱和石灰水
 不饱和石灰水
不饱和石灰水概念的理解:
(1)溶液的饱和与不饱和跟温度和溶质的量的多少有关系。因此在谈饱和溶液与不饱和溶液时,一定要强调“在一定温度下”和“一定量的溶剂里”,否则就无意义。
(2)一种溶质的饱和溶液仍然可以溶解其他溶质。如氯化钠的饱和溶液中仍可溶解蔗糖。
(3)有些物质能与水以任意比例互溶,不能形成饱和溶液,如:酒精没有饱和溶液。
饱和溶液和不饱和溶液的相互转化:
一般,对饱和溶液与不饱和溶液相互转化过程中溶液组成的分析:
①饱和溶液
 不饱和溶液(或不饱和溶液
不饱和溶液(或不饱和溶液 饱和溶液。不发生结晶的前提下)
饱和溶液。不发生结晶的前提下)溶液中溶质、溶剂、溶液的质量不变,溶质质量分数不变。
②不饱和溶液
 饱和溶液
饱和溶液溶液的溶剂质量不变,溶质、溶液、溶质质量分数均增大。
③不饱和溶液
 饱和溶液(不发生结晶的前提下)
饱和溶液(不发生结晶的前提下)溶质质量不变,溶剂、溶液质量变小,溶质质量分数变大。
④饱和溶液
 不饱和溶液
不饱和溶液溶剂、溶液质量增大,溶质质量不变,溶质质量分数变小
判断溶液是否饱和的方法:
①观察法:当溶液底部有剩余溶质存在,且溶质的量不再减少时,表明溶液已饱和。
②实验法:当溶液底部无剩余溶质存在时,可向该溶液中加入少量该溶质,搅拌后,若能溶解或溶解一部分,表明该溶液不饱和;若不能溶解,则表明该溶液已饱和。
浓溶液,稀溶液与饱和溶液,不饱和溶液的关系:
为粗略地表示溶液中溶质含量的多少,常把溶液分为浓溶液和稀溶液。在一定量的溶液里含溶质的量相对较多的是浓溶液,含溶质的量相对较少的是稀溶液。它们与饱和溶液、不饱和溶液的关系如下图所示:
 A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液
A. 饱和浓溶液B.饱和稀溶液C.不饱和浓溶液D.不饱和稀溶液(1)溶液的饱和与不饱和与溶液的浓和稀没有必然关系。
(2)饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
(3)在一定温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
易变质的物质:
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
1. 由于吸水质量增加的物质:氢氧化钠固体,浓硫酸
2. 由于跟水反应质量增加的物质:氧化钙,氧化钠,硫酸铜
3. 由于和二氧化碳反应质量增加的物质:氢氧化钠,氢氧化钾,氢氧化钙
4. 由于挥发质量减少的物质:浓盐酸,浓硝酸,酒精,氨水
5. 由于风化质量减少的物质:碳酸钠晶体
氢氧化钠变质的知识归纳:
氢氧化钠变质主要考点包括:变质原因、检验变质的方法、检验变质的程度、 除去杂质得到就纯净的氢氧化钠。
1 、氢氧化钠变质的原因:
敞口放置, 与空气中的二氧化碳反应, 生成了碳酸钠。 2NaOH+CO 2 =Na 2 CO 3 +H 2 O
2 、检验氢氧化钠是否变质的方法: ( 分别滴加酸、碱、盐溶液,各为一种方法 )
①取少量样品于试管中, 滴加稀盐酸 ( 或者稀硫酸 ) , 如果产生气泡, 说明已变质。 Na 2 CO 3 +2HCl=2NaCl+H 2 O+CO 2 ↑
②取少量样品于试管中,滴加氢氧化钙溶液 ( 或者氢氧化钡溶液 ) ,如果产生白色 沉淀,说明已变质。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
③取少量样品于试管中,滴加氯化钙溶液 ( 或者硝酸钙等其它可溶性钙盐、钡盐 溶液 ) Na 2 CO 3 +CaCl 2 =CaCO 3 ↓ +2NaCl
3 、检验氢氧化钠变质程度的方法:
取少量样品于试管中,滴加足量的 CaCl2 溶液,有白色沉淀生成;静置,像上层澄清液中滴加少量酚酞溶液,如果溶液变红色,说明溶液部分变质;如果溶液呈无色,说明氢氧化钠完全变质。
解释:碳酸钠溶液呈碱性,它的存在会影响到氢氧化钠的检验,所以在检验氢氧化钠前必须把碳酸钠除去。除去碳酸钠时不能用酸,因为酸会与氢氧化钠反应; 不能用碱,因为碱会与碳酸钠反应生成氢氧化钠,干扰原来氢氧化钠的检验。
4 、如何除去部分变质的氢氧化钠中的碳酸钠。 滴加适量氢氧化钙溶液至刚好无沉淀生成为止,然后过滤,就得到氢氧化钠溶液,再蒸发,就得到氢氧化钠固体。 Na 2 CO 3 +Ca(OH) 2 =CaCO 3 ↓ +2NaOH
除杂方法:除杂时为了不引入新杂质,如果除去阴离子,所选择试剂的阴离子 与主题物质一致。
氧化钙和氢氧化钙的变质:
(1)变质的原因
氧化钙在空气中敞口放置会与空气中的水蒸气反应生成氢氧化钙 CaO+H 2 O===Ca(OH) 2 , 氢氧化钙继续与空气中的二氧化碳反应生成碳酸钙。 Ca(OH) 2 +CO 2 ====CaCO 3 ↓+H 2 O
(2)检验变质后物质存在的方法:
氧化钙:
取少量变质后的固体放入烧杯中,加入水充分溶解,用手摸烧杯外壁有灼热感。
氢氧化钙:
(1)取变质后物质溶于水,向其中通入二氧化碳气体,有白色沉淀生成。
(2)取变质后物质溶于水,向其中滴加碳酸钠溶液,有白色沉淀生成。 碳酸钙:取少量变质后固体,向其中滴加稀盐酸,有气泡冒出。 CaCO3 +2HCl===CaCl2 +H2O+CO2 ↑
【特殊强调】:有氧化钙存在的情况下,初中阶段检验不出氢氧化钙的存在。因为氧化钙溶于水后会生成氢氧化钙,会干扰原来氢氧化钙的检验。
其它常见物质变质的知识小结:
NaOH在空气中变质:2NaOH+CO2==Na2CO3+H2O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (Na 2 CO 3 +2HCl===2NaCl+H 2 O+CO 2 ↑ )
消石灰 [Ca(OH)2] 放在空气中变质: Ca(OH) 2 +CO 2 ====CaCO 3 ↓ +H 2 O
检验: 取样滴加稀 HCl,若有气泡产生,则已经变质 (CaCO 3 +2HCl===CaCl 2 +H 2 O+CO 2 ↑ )
生石灰 (CaO) 暴露在空气中变质: CaO+H 2 O===Ca(OH) 2
检验: 取样用试管加热,若试管内壁有小水珠产生,则已变质 [Ca(OH) 2 = 加热 =CaO+H 2 O]
铁生锈:4Fe+3O 2 ===2Fe2O3
检验:观察颜色 , 若有红色粉末在表面, 则已变质
铜生锈:2Cu+O 2 +CO 2 +H 2 O===Cu 2 (OH) 2 CO 3
检验:观察颜色 , 若有绿色粉末在表面,则已变质。
发现相似题
与“如图所示,将密闭的相互连通的装置放在天平上,调节天平使之...”考查相似的试题有:
- 下列有关溶液的说法,正确的是( )A.凡是均一、透明、无色的液体都是溶液B.饱和溶液析出晶体后就变成了不饱和溶液C.某饱...
- 下列说法中不正确的是( )A.溶液是由溶质和溶剂组成,所以溶液一定是混合物B.用适量的水区分硝酸铵固体和氢氧化钠固体C....
- 炎热的夏天,打开冰镇可乐的瓶盖,有大量的气泡产生,有关说法错误的是( )A.气体是二氧化碳B.瓶内气压减小使该气体的溶解...
- 如图为a.b.c三种不含结晶水的固体物质的溶解度曲线,下列说法正确的是[ ]A.物质a的溶解度最大B.浓的a溶液中含有少量b,通常采...
- 下列说法中正确的是( )A.原子中一定含有质子、中子和电子三种微粒B.饱和溶液在升高温度后都会变成不饱和溶液C.根据质量...
- 下列有关溶液的叙述正确的是( )A.稀溶液一定是不饱和溶液B.饱和溶液就是不能再溶解任何物质的溶液C.溶质在溶解的过程中...
- 通常情况下,欲将一杯不饱和的蔗糖溶液变成饱和溶液,最适宜的方法是( )A.加蔗糖B.加水C.升温D.增大压强
- 甲、乙两同学为了探究实验室中久置的氢氧化钠固体是否变质,进行了如下实验.请与他们一起完成探究活动.【提出问题】氢氧化...
- 实验室中有些药品需密封保存,某同学将其原因归纳为下列两种情况:①药品能吸收空气中的水蒸气; ②药品能与空气中的某些成分发...
- 固体NaOH具有以下性质:①白色固体 ②有腐蚀性 ③易吸收水分而潮解 ④能与空气中的CO2反应.请判断实验室中必须将它密封保存的主...