本试题 “黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一.其中炉渣的主要成分是Fe0、Fe203、Si02、Al203.各物质有如下转化关系,请回答:(1)写出能证明SO2具有...” 主要考查您对二氧化硫
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 二氧化硫
二氧化硫:
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的制备:
工业制法:

实验室制法:
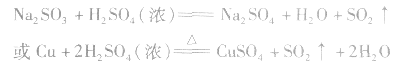
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


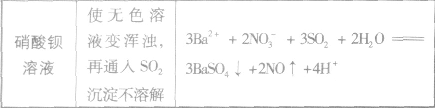
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表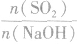 ,如下数轴所示:
,如下数轴所示: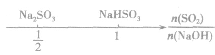
分析数轴可得:
(1)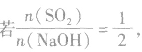 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)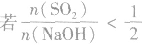 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)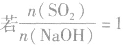 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)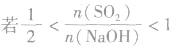 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)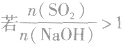 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
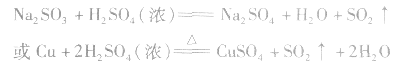
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

发现相似题
与“黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一.其中炉...”考查相似的试题有:
- 以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3•6H2O)的工艺流程如下:回答下列问题:(1)在一定条件下,SO2转化...
- 长期存放的亚硫酸钠可能会被部分氧化,现通过实验来测定某无水亚硫酸钠试剂的纯度。实验步骤如下:①称量ag样品,置于烧杯中。...
- 常见的污染物分为一次污染物和二次污染物.二次污染物是排入环境中的一次污染物在物理化学因素或微生物作用下发生变化所生成...
- 在二氧化碳中混有少量的二氧化硫、三氧化硫、氯化氢杂质。设计一种一步只除去一种杂质,最后得到干燥纯净二氧化碳的实验方案...
- 下列物质中,不可作漂白剂的是( )A.SO2B.Ca(ClO)2C.Na2CO3D.Na2O2
- 向盐酸中加入浓硫酸时产生白雾,下列叙述不属于产生该现象的原因是( )A.浓硫酸具有脱水性B.浓硫酸具有吸水性C.盐酸具有...
- 关于C、N、S非金属元素及其化合物的下列说法中,错误的是A.金刚石、石墨、C60都是碳元素组成的单质,属于碳的同素异形体B.氮...
- 根据要求完成下列实验。(a、b 为弹簧夹,其他装置略去)(一)验证酸性的相对强弱:碳酸>苯酚。(已知酸性:亚硫酸 >碳酸)(1)...
- 下列有关臭氧的叙述不正确的是( )A.臭氧的氧化性比氧气强,常温下能将银、汞等较不活泼的金属氧化B.臭氧可以杀死许多细菌,...
- 某兴趣活动小组利用物质间的相互转化,设计成一个平面魔方,如下图所示已知①A、B、C、D、G含有同种元素.②③E是通常情况下密度...