本试题 “以石灰石、水、纯碱为原料,如何制取烧碱?写出有关反应的化学方程式,并说明基本反应类型。(1)________________________________,属于_________反应。(2...” 主要考查您对化合反应
分解反应
复分解反应
碳酸钠
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化合反应
- 分解反应
- 复分解反应
- 碳酸钠
化合反应的定义:
化合反应指的是由两种或两种以上的物质生成一种新物质的反应。
化合反应的一般类型有:
1.金属+氧气→金属氧化物:很多金属都能跟氧气直接化合。例如常见的金属铝接触空气,它的表面便能立即生成一层致密的氧化膜,可阻止内层铝继续被氧化。4Al+3O2=2Al2O3
2.非金属+氧气→非金属氧化物: 一经点燃,许多非金属都能在氧气里燃烧,如:C+O2=点燃=CO2
3.金属+非金属→无氧酸盐:很多金属能与非金属氯、硫等直接化合成无氧酸盐。如 2Na+Cl2=点燃==2NaCl
4.氢气+非金属→气态氢化物:因氢气性质比较稳定,反应一般需在点燃或加热条件下进行。如 2H2+O2=点燃=2H2O
5. 碱性氧化物+水→碱:多数碱性氧化物不能跟水直接化合。判断某种碱性氧化物能否跟水直接化合,一般的方法是看对应碱的溶解性,对应的碱是可溶的或微溶的,则该碱性氧化物能与水直接化合。如: Na2O+H2O=2NaOH. 对应的碱是难溶的,则该碱性氧化物不能跟水直接化合。如CuO、Fe2O3都不能跟水直接化合。
6.酸性氧化物+水→含氧酸:除SiO2外,大多数酸性氧化物能与水直接化合成含氧酸。如: CO2+H2O=H2CO3
7.碱性氧化物+酸性氧化物→含氧酸盐:大多数碱性氧化物和酸性氧化物可以进行这一反应。其碱性氧化物对应的碱碱性越强,酸性氧化物对应的酸酸性越强,反应越易进行。如Na2O+CO2=Na2CO3
8.氨+氯化氢→氯化铵:氨气易与氯化氢化合成氯化铵。如: NH3+HCl=NH4Cl
9. 和氧气在点燃的情况下形成二氧化硫:S+O2==点燃==SO2
化合反应的模型:
A+B+…+N→X
化合反应与氧化还原反应的关系:
有单质参加的化合反应一定属于氧化还原反应。此外,化合反应一般释放出能量。
分解反应:
一种化合物在特定条件下(如加热、通直流电、催化剂等)分解成两种或两种以上较简单的单质或化合物的反应
分解反应类型:
氧化物分解: 2H2O=(通电)2H2↑+O2↑ 2H2O2=(MnO2)2H2O+O2↑
含氧酸分解: H2CO3=(△)H2O+CO2↑ H2SO3=(△)H2O+SO2↑
碱的分解: Mg(OH)2=(高温)MgO+H2O Cu(OH)2=(△)CuO+H2O 2Fe(OH)3=(高温)Fe2O3+3H2O
2Al(OH)3=(高温)Al2O3+3H2O (注:不溶性碱高温时可分解为金属氧化物和水)
盐的分解: 2NaHCO3=(△)Na2CO3+CO2↑+H2O Ca(HCO3)2=(△)CaCO3+CO2↑+H2O CaCO3=(高温)CaO+CO2↑
2KMnO4=(△)K2MnO4+MnO2+O2↑ 2KClO3=(△,MnO2)2KCl+3O2↑
分解反应的模型:
A=B+C 可以简单理解为“一变多”,也可以理解成为由一种反应物发生化学反应后生成两种或两种以上的物质的反应。
分解反应与氧化还原反应的关系:
分解反应不一定是氧化还原反应,例如:2Al(OH)3=(高温)Al2O3+3H2O
只有能产生单质的分解反应才是氧化还原反应,例如:2H2O=(通电)2H2↑+O2↑
复分解反应的定义:
复分解反应是由两种化合物,通过互相交换成分并生成两种新化合物的反应,模式为AB+CD→AD+CB。它是基本类型的化学反应之一。复分解都不是氧化还原反应。
复分解反应发生的条件:
1.生成难溶的物质:如生成BaSO4、AgCl、CaCO3等沉淀。
2.生成气体或易挥发物质:如生成CO2、H2S等气体。
3.有弱电解质生成:如生成H2O、弱酸、弱碱等。
复分解反应的分类:
- 酸与盐 例如:2HCl+CaCO3=CaCl2+H2O+CO2↑
- 酸与碱 例如:H2SO4+Ba(OH)2=BaSO4↓+2H2O
- 盐与盐(可溶) 例如:Na2CO3+CaCl2=2NaCl+CaCO3↓
- 盐与碱 例如:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
- 酸与金属氧化物 例如:盐酸除铁锈:Fe2O3+6HCl=2FeCl3+3H2O
复分解反应的模型:
AB+CD→AD+CB
复分解反应与氧化还原反应的关系:
复分解都不是氧化还原反应。
碳酸钠(Na2CO3):
(1)俗名:纯碱或苏打;白色粉末,易溶于水,稳定;可用于制玻璃、肥皂、造纸、防治等
(2)与H+反应:CO32-+2H+==CO2↑+H2O
(3)与NaOH不反应
(4)与石灰水反应:CO32-+Ca2+==CaCO3↓
(5)与氯化钡反应:CO32-+Ba2+==BaCO3↓
(6)与CO2反应:CO32-+CO2+H2O==2HCO3-
碳酸钠的物理性质:
碳酸钠常温下为白色粉末或颗粒。溶于水和甘油,不溶于乙醇。水溶液呈强碱性,pH11.6。
碳酸钠是一种强碱盐,溶于水后发生水解反应(碳酸钠水解会产生碳酸氢钠和氢氧化钠),使溶液显碱性,有一定的腐蚀性,能与酸进行复分解反应。
稳定性 稳定性较强,但高温下也可分解,生成氧化钠和二氧化碳。长期暴露在空气中能吸收空气中的水分及二氧化碳,生成碳酸氢钠,并结成硬块。吸湿性很强,很容易结成硬块,在高温下也不分解。含有结晶水的碳酸钠有3种:Na2CO3·H2O、Na2CO3·7H2O和Na2CO3·10H2O。
碳酸钠的用途:
用于制玻璃、肥皂、造纸、纺织等工业,也用作食品工业发酵剂。
Na2CO3、NaHCO3的性质比较:
| 表示 | 名称 | 碳酸钠 | 碳酸氢钠 |
| 化学式 | Na2CO3 | NaHCO3 | |
| 俗称 | 苏打 | 小苏打 | |
| 物理性质 | 色态 | 白色粉末 | 白色晶体 |
| 溶解性 | 易溶于水 | 能溶于水 | |
| 化学性质 | 与盐酸反应 | Na2CO3+2HCl=2NaCl+H2O+CO2↑ | NaHCO3+HCl=NaCl+H2O+CO2↑ |
| 热稳定性 | 很稳定 | 受热分解:2NaHCO3=(加热)=Na2CO3+H2O+CO2↑ | |
| 与NaOH反应 | 不反应 | NaHCO3+NaOH=Na2CO3+H2O | |
| 相互转化 | Na2CO3+H2O+CO2=2NaHCO3 | NaHCO3+NaOH=Na2CO3+H2O 2NaHCO3=(加热)=Na2CO3+H2O+CO2↑ |
Na2CO3、NaHCO3的鉴别:

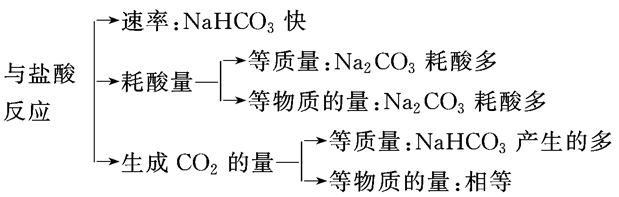
Na2CO3、NaHCO3与足量盐酸反应的比较:
Na2CO3溶液与盐酸反应:
滴加顺序不同,现象不同,化学方程式不同。
①向盐酸里逐滴加入Na2CO3溶液(开始时酸过量) 2HCl+Na2CO3===2NaCl+CO2↑+H2O
②向Na2CO3溶液里逐滴加入盐酸(开始时酸不足) HCl+Na2CO3==NaCl+NaHCO3(无气泡) HCl+NaHCO3==NaCl+CO2↑+H2O(后来有气泡)
[特别提醒]
(1)Na2CO3和盐酸可以用互滴法鉴别。
(2)滴加顺序不同,放出CO2的量可能相同,也可能不同。
碳酸钠、碳酸氢钠与盐酸反应的基本图像的归纳总结:
(1)向Na2CO3中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图1所示;
(2)向NaHCO3中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图2所示;
(3)向NaOH、Na2CO3的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图3所示(设NaOH、Na2CO3的物质的量之比x∶y=1∶1,其他比例时的图像略);
(4)向Na2CO3、NaHCO3的混合物中逐滴加入盐酸,消耗HCl的体积与产生CO2的体积的关系如图4所示(设Na2CO3、NaHCO3的物质的量之比m∶n=1∶1,其他比例时的图像略)。
与“以石灰石、水、纯碱为原料,如何制取烧碱?写出有关反应的化...”考查相似的试题有:
- 按下列化学反应基本类型依次填入四个化学方程式,要求后一个反应的反应物必须含有前一个反应的生成物(1)分解反应:________...
- CaC2、ZnC2、AlC3、Mg2C3、Li2C2等同属于离子型碳化物,请通过CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应...
- 有关钠的说法中,错误的是[ ]A.是两种核素,的中子数为14B.Na2O和Na2O2都属于碱性氧化物C.热稳定性:Na2CO3>NaHCO3D.钠...
- X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无气味的气体。这四种化合...
- 为了得到比较纯净的物质,使用的方法恰当的是[ ]A.向Na2CO3饱和溶液中,通入过量的CO2后,在减压、加热的条件下,蒸发得NaHC...
- 下列关于钠及其化合物的说法正确的是[ ]A.钠的化学性质活泼,可用于制取一些贵重金属B.由于钠比较活泼,所以它能从盐溶液中...
- 下列说法不正确的是[ ]A.用丁达尔现象可以区分食盐水和硫酸铜溶液B.用热的纯碱溶液可以更好地去除油污C.外加直流电源,将...
- A、B、C、D、E5种物质的焰色反应都呈黄色,A、B与水反应都有气体产生。A与水反应生成的气体具有还原性,B与水反应生成的气体...
- 某活动课程小组拟用50 mL NaOH溶液吸收CO2气体,制备Na2CO3溶液。为了防止通入过量的CO2气体生成NaHCO3,设计了如下实验步骤...
- 下图表示的是A-E五种物质间的相互转化关系,其中A为淡黄色固体,B为单质。试推出各物质的化学式,并写出B→C、C→D、D→E反应的...