本试题 “利用化学知识对下列说法进行判断,其中正确的是( )A.咀嚼米饭时会出现甜味,这一过程属于物理变化B.绿色植物合成葡萄糖的过程中将太阳能转化为化学能C....” 主要考查您对六大营养素
关于溶液的计算
固体溶解度
物理变化和化学变化的特征和判别
光合作用和呼吸作用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 六大营养素
- 关于溶液的计算
- 固体溶解度
- 物理变化和化学变化的特征和判别
- 光合作用和呼吸作用
人类需要的营养素:
人类为了维持生命和健康,必须摄取食物。食物的成分主要有蛋白质、糖类、油脂、维生素、无机盐和水六大类,通常称为六大基本营养素。
六大营养素的特性:
1.蛋白质
蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料。
(1)蛋白质的多样性:蛋白质是由多种氨基酸构成的极为复杂的有机化合物,相对分子质量很大,从几万到几百万。构成氨基酸的基本元素有氢、氧、碳、氮,但不同种类的蛋白质中可能含有其他元素,如血红蛋白。
(2)蛋白质的存在:主要存在于动物肌肉、皮肤、毛发、蹄、角、血液和各种酶中,许多植物(如大豆、花生) 的种子里也含有丰富的蛋白质。
(3)氨基酸在人体内的转化:人体通过食物获得的蛋白质在胃肠道里与水发生反应,生成氨基酸。氨基酸通过肠壁进入血液循环,一部分氨基酸被氧化,生成尿素、二氧化碳和水等排出体外,同时放出热量供人体活动的需要。每克蛋白质完全氧化放出约18kJ的能量。另一部分氨基酸再重新形成人体所需要的各种蛋白质,维持人体的生长发育和组织更新。
(4)蛋白质的功能:
a. 血红蛋白的作用:人体内氧气的传输者,起载体作用。正常呼吸时,在肺部,血红蛋白中血红素的Fe2+与氧结合成为氧合血红蛋白,随着血液流到机体的各个组织和器官,放出氧气,供体内氧化用。同时血红蛋白结合血液中的二氧化碳,携带到肺部呼出。人的呼吸作用就是这样反复进行的过程。血红蛋白+O2→氧合血红蛋白血红蛋白也能与一氧化碳结合,而且结合能力很强,大约是氧气的200~300倍。结合了一氧化碳的血红蛋白很难再与氧气结合,人就会因缺氧而中毒,甚至窒息死亡。
b. 酶的作用:酶是一类重要的蛋白质,是生物催化剂,能催化生物体内的反应。一种酶只能催化一类反应,而且反应一般是在体温和接近中性的条件下进行的。酶的催化具有专一性、高效性的特点。
(5)蛋白质的变性当蛋白质分子受到某些物理因素(如高温、紫外线、超声波、高电压等)和化学因素(如酸、碱、有机溶剂、重金属盐等)的影响时,其结构会被破坏,导致其失去生理活性(称为蛋白质的变性)。如甲醛(防腐剂福尔马林的主要成分)会与蛋白质中反应,使蛋白质分子结构发生变化,从而失去生理活性并发生凝固。
(6)蛋白质与健康
a.蛋白质缺乏成年人:肌肉消瘦、机体免疫力下降、贫血,严重者将发生水肿。成人每天需从食物中摄取60.70g的蛋白质。未成年人:生长发育停滞、贫血、智力发育差、视觉差。。青少年每天需从食物中摄取75—90g的蛋白质。
b.蛋白质过量蛋白质在体内不能储存,多了机体无法吸收,过量摄入蛋白质,将会因代谢障碍产生蛋白质中毒甚至死亡。
2.糖类
(1)糖类的组成糖类是人类食物的重要成分,由C、H、O三种元素组成,又称碳水化合物。
(2)糖类的生理功能为机体活动提供能量,糖类所提供的能量占人类食物所提供的总能量的60%~70%;构成机体的重要物质;调节食品风味;维持大脑功能必需的能量;调节脂肪代谢;提供膳食纤维。
(3)食物中的糖类分成两类:人可以吸收利用的有效糖类如单糖,多糖,双糖和人不能消化的无效糖类如纤维素。
(4)常见的糖类物质
a. 淀粉:它是绿色植物光合作用的产物,化学式为(C6H10O5)n。
b.葡萄糖
葡萄糖的化学式为C6H12O5。葡萄糖经过肠壁吸收进入血液成为血液,输送到人体的各个组织和器官,为人体组织提能量.又在酶的作用下,转变为糖原贮藏在肝脏和肌肉中。在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,机体活动和维持恒定体温的需耍。
注意:葡萄糖与新制Cu(OH)2悬浊液反应生成红色氧化亚铜沉淀.医疗上用此反应原理检验血糖。
c.蔗糖
(5)糖类与健康
人体中缺乏糖类会导敛全身无力、头帚、心悸、脑功能障碍等,低血糖严重者会导致昏迷。因为葡萄糖不经过转化即可为人体吸收,所以低血糖患者可利用静脉注射葡萄糖溶液的方法迅速补允营养,时间允许时可以服用蔗糖水临水临时代替。当糖类过多时,人体组织吸收不了,就会转化成脂肪储存于体内,使人过于肥胖而诱发各种疾病,如高血脂、冠心病等。
3.油脂
(1)油脂的分布在常温下,植物油脂呈液态,如花生油、豆油等;动物油脂呈固态,如牛油等。
(2)功能:油脂是重要的供能物质,每克油脂在人体内完全氧化时放出约39kJ的能量,比糖类多一倍以上,因此它是重要的供能物质。在正常情况下,每人每日需摄人50~60g油脂,它供给人体每日所需能量的 20%~25%。
(3)油脂与健康
一般成人体内贮存的脂肪约占人体质量的10%~20%,它是维持生命活动的备用能源。当人进食量小、摄入食物的能量小足以支付机体消牦的能量时,就要消耗自身的脂肪来满足机体的需要,此时人就会消瘦。但是过多地摄入油脂容易诱发心脑血管疾病、肥胖症,还会诱发高血压、糖尿病等。
4. 维生素
注意:维生素并非“多多益姜”
维牛素A超量摄入的副作用:导致中毒,急性中毒表现为头晕、嗜睡、头痛、呕叶、腹泻等症状。超量服用维生素B。在200mg以上,将会产生药物依赖,严重者能出现步态不稳、手足麻木等。
维生素C如果每次服用超过1g时,就可能为病毒提供养料,可谓得不偿失,还可能导致腹痛、腹泻、尿频,影响儿童生长发育、影响孕妇的胎儿发育,甚至患先天性坏血病等。
维生素D长期超量服用在1800mg后,就会出现生长停滞,影响儿童生长发育。
维生素E每日用量400~800mg后,可引起视力模糊,乳腺肿大,头痛,头晕,恶心等。长期服用超过800mg,将改变分泌代谢,免疫功能下降等。
5.无机盐
(1)人体内无机盐的作用无机盐是人体内的营养元素之一,含量虽少但对正常生理活动有重要影响。主要有以下作用:为构成人体组织的重要成分;维持机体的渗透压和体液酸碱平衡;维持神经细胞兴奋性;构成酶的成分或激活酶的活性;参与体内物质代谢等。
(2)人体内无机盐的获取及缺乏症机体在新陈代谢过程中,随时都有一定量的矿物质以不同的途径排出体外,如汗液、尿液,因此必须及时适量补充。矿物质在食物和水中广泛存在,一般不易引起缺乏。不同的生理状况和不同的地理环境或其他特殊件会引起某些元素的缺乏或过量,导致诸如克山病、骨节病等地方病的发生。
6.水
(1)水在人体内的作用水在人体中的功能是维持细胞状态,增强代谢能,调节血液的正常循环,溶解营养素,使之易于吸收和运输;水还能帮助机体排泄废弃物,散发热量,调节体温,并使血液保持酸碱平衡;水在食物消化、促进血液循环、润滑关节和各内脏器官保持它们正常的生理机能中起着重要作用;人体内的水还能使体内器官减缓震荡。
(2)人体内水的流失和获取途径
a.人体内水的流失途径:排尿、呼吸、体表排汗排粪。
b.人体内水的获取途径:饮水、食物、体内物代谢。
c.如果身体摄入水分不足,开始时人体可通过节机体减少水分的排出量,保持机体水平衡,但严重不足时,自身就无法控制了。当体内水分减少达体重的2%时,身体可因脱水而造成代谢障碍;减少7%—14% 时,出现严重的脱水症状;减少15%以上,即有生命危险。
知识点拨:
1. 纤维和纤维素:
很多学生常常存在一个认识上的误区,认为“纤维:纤维素”,其实这是两个不同的概念。纤维素是指一种特定的化学物质。纤维素通常为白色、无臭、无味、不溶于水,也不溶于一般的有机溶剂,其化学式为 (C6H10O5)n,属于多糖物质。纤维素广泛存在于自然界的植物体中,木材中有一半是纤维素,棉花是自然界中较纯粹的纤维素,脱脂棉和滤纸差不多是纯粹的纤维素纤维是指细而柔软的一类物质,分为天然纤维和化学纤维:天然纤维有植物纤维、动物纤维和矿物纤维化学纤维分为人造纤维和合成纤维。人造纤维是指利用含有纤维素的原料经化学处理和机械加工而制成的纤维。合成纤维是指利用石油、灭然气、煤为原料制成单体,再经聚合反应而生成的高分子化合物最后经拉丝工艺获得的纤维。
2. 人不能消化纤维素的原因
纤维素[(C6H10O5)n]也属于糖类,主要存存于植物体内.如树木的茎主要成分是纤维素,棉花的主要成分也是纤维素。同样是糖类,人可以从食物中摄食淀粉,并在体内将淀粉最终消化成葡萄糖加以吸收利用,但人不能消化纤维素,原因在于人体内没有纤维素酶,不能使纤维素在人体内水解。
3. 几种维生素的生理功能及来源
知识拓展:
1. 食品添加剂:
(1)食品添加剂的界定根据1962年FAO/WHO食品法典委员会(CA 对食品添加剂的定义,食品添加剂是指:有意识地一以少量添加于食品,以改善食品的外观、风味和组织构或贮存性质的非营养物质。
(2)分类根据我国的《食品添加剂使用卫生标准》将其为:防腐剂、抗氧化剂、发色剂、漂白剂、酸味剂、凝剂、疏松剂、增稠剂、消泡剂、甜味剂、着色剂、乳化剂品质改良剂、抗结剂、增昧剂、酶制剂、被膜剂、发泡剂保鲜剂、香料、营养强化剂以及其他添加剂。
2. 认识服装的标签
当你买衣服时,怎样知道服装面料的种类呢?看服装上的标签。服装标签一般包括服装的型号、面料的纤维种类及含量、洗涤熨烫说明等内容。如果服装面料是由一种纤维材料制成的,则用“纯×”或“100% x”来表示,如“纯棉…‘纯毛”或“100%毛”;如果服装是由两种或两种以上的纤维制成的,标签上应注明每种纤维的含量,如“涤纶20%、棉80%”等。
3. 各种纤维素的燃烧鉴别法
人类为了维持生命和健康,必须摄取食物。食物的成分主要有蛋白质、糖类、油脂、维生素、无机盐和水六大类,通常称为六大基本营养素。
六大营养素的特性:
1.蛋白质
蛋白质是构成细胞的基本物质,是机体生长及修补受损组织的主要原料。
(1)蛋白质的多样性:蛋白质是由多种氨基酸构成的极为复杂的有机化合物,相对分子质量很大,从几万到几百万。构成氨基酸的基本元素有氢、氧、碳、氮,但不同种类的蛋白质中可能含有其他元素,如血红蛋白。
(2)蛋白质的存在:主要存在于动物肌肉、皮肤、毛发、蹄、角、血液和各种酶中,许多植物(如大豆、花生) 的种子里也含有丰富的蛋白质。
(3)氨基酸在人体内的转化:人体通过食物获得的蛋白质在胃肠道里与水发生反应,生成氨基酸。氨基酸通过肠壁进入血液循环,一部分氨基酸被氧化,生成尿素、二氧化碳和水等排出体外,同时放出热量供人体活动的需要。每克蛋白质完全氧化放出约18kJ的能量。另一部分氨基酸再重新形成人体所需要的各种蛋白质,维持人体的生长发育和组织更新。
(4)蛋白质的功能:
a. 血红蛋白的作用:人体内氧气的传输者,起载体作用。正常呼吸时,在肺部,血红蛋白中血红素的Fe2+与氧结合成为氧合血红蛋白,随着血液流到机体的各个组织和器官,放出氧气,供体内氧化用。同时血红蛋白结合血液中的二氧化碳,携带到肺部呼出。人的呼吸作用就是这样反复进行的过程。血红蛋白+O2→氧合血红蛋白血红蛋白也能与一氧化碳结合,而且结合能力很强,大约是氧气的200~300倍。结合了一氧化碳的血红蛋白很难再与氧气结合,人就会因缺氧而中毒,甚至窒息死亡。
b. 酶的作用:酶是一类重要的蛋白质,是生物催化剂,能催化生物体内的反应。一种酶只能催化一类反应,而且反应一般是在体温和接近中性的条件下进行的。酶的催化具有专一性、高效性的特点。
(5)蛋白质的变性当蛋白质分子受到某些物理因素(如高温、紫外线、超声波、高电压等)和化学因素(如酸、碱、有机溶剂、重金属盐等)的影响时,其结构会被破坏,导致其失去生理活性(称为蛋白质的变性)。如甲醛(防腐剂福尔马林的主要成分)会与蛋白质中反应,使蛋白质分子结构发生变化,从而失去生理活性并发生凝固。
(6)蛋白质与健康
a.蛋白质缺乏成年人:肌肉消瘦、机体免疫力下降、贫血,严重者将发生水肿。成人每天需从食物中摄取60.70g的蛋白质。未成年人:生长发育停滞、贫血、智力发育差、视觉差。。青少年每天需从食物中摄取75—90g的蛋白质。
b.蛋白质过量蛋白质在体内不能储存,多了机体无法吸收,过量摄入蛋白质,将会因代谢障碍产生蛋白质中毒甚至死亡。
2.糖类
(1)糖类的组成糖类是人类食物的重要成分,由C、H、O三种元素组成,又称碳水化合物。
(2)糖类的生理功能为机体活动提供能量,糖类所提供的能量占人类食物所提供的总能量的60%~70%;构成机体的重要物质;调节食品风味;维持大脑功能必需的能量;调节脂肪代谢;提供膳食纤维。
(3)食物中的糖类分成两类:人可以吸收利用的有效糖类如单糖,多糖,双糖和人不能消化的无效糖类如纤维素。
(4)常见的糖类物质
a. 淀粉:它是绿色植物光合作用的产物,化学式为(C6H10O5)n。
| 存在 | 植物种子或块茎中,如水稻,小麦,马铃薯等 |
| 消化 | 食物淀粉在人体内经酶的作用,与水作用最终变成葡萄糖,然后再被人体吸收 |
| 检验 | 淀粉遇到碘单质(常用碘水或碘酒做试验)会变蓝色,以此检验淀粉的存在 |
葡萄糖的化学式为C6H12O5。葡萄糖经过肠壁吸收进入血液成为血液,输送到人体的各个组织和器官,为人体组织提能量.又在酶的作用下,转变为糖原贮藏在肝脏和肌肉中。在人体组织里,葡萄糖在酶的作用下经缓慢氧化转变成二氧化碳和水,同时放出能量,机体活动和维持恒定体温的需耍。
注意:葡萄糖与新制Cu(OH)2悬浊液反应生成红色氧化亚铜沉淀.医疗上用此反应原理检验血糖。
c.蔗糖
| 存在 | 贮藏在某些植物(如甘蔗、甜菜等)中,化学式为C12H22O11 |
| 用途 | 日常生活中常用的白糖、冰糖和红糖的主要成分就是蔗糖,它是食品中常用的甜味剂 |
(5)糖类与健康
人体中缺乏糖类会导敛全身无力、头帚、心悸、脑功能障碍等,低血糖严重者会导致昏迷。因为葡萄糖不经过转化即可为人体吸收,所以低血糖患者可利用静脉注射葡萄糖溶液的方法迅速补允营养,时间允许时可以服用蔗糖水临水临时代替。当糖类过多时,人体组织吸收不了,就会转化成脂肪储存于体内,使人过于肥胖而诱发各种疾病,如高血脂、冠心病等。
3.油脂
(1)油脂的分布在常温下,植物油脂呈液态,如花生油、豆油等;动物油脂呈固态,如牛油等。
(2)功能:油脂是重要的供能物质,每克油脂在人体内完全氧化时放出约39kJ的能量,比糖类多一倍以上,因此它是重要的供能物质。在正常情况下,每人每日需摄人50~60g油脂,它供给人体每日所需能量的 20%~25%。
(3)油脂与健康
一般成人体内贮存的脂肪约占人体质量的10%~20%,它是维持生命活动的备用能源。当人进食量小、摄入食物的能量小足以支付机体消牦的能量时,就要消耗自身的脂肪来满足机体的需要,此时人就会消瘦。但是过多地摄入油脂容易诱发心脑血管疾病、肥胖症,还会诱发高血压、糖尿病等。
4. 维生素
| 种类 | 维生素有20多种,多数在人体内小能合成,需要从食物中摄取 |
| 存在 | 水果、蔬菜、种了食物、动物肝脏、鱼类、鱼肝油、蛋类、牛奶等均含丰富的维生素 |
| 功能 | 调节新陈代谢,预防疾病,维持身体健康。如维生素C有防癌作用,它能促进人体生长发育,增强对疾病的抵抗力 |
| 缺乏的后果 | 缺乏某种维生素会使人患病。如:缺乏维生素A,会引起夜盲症;缺乏维生素C,会引起坏血病;缺乏维生素B,会引起皮炎、贫血、肌肉萎缩等;缺乏维生素D,会使青少年发育不良而得佝偻病,老年人会发生骨质疏松 |
注意:维生素并非“多多益姜”
维牛素A超量摄入的副作用:导致中毒,急性中毒表现为头晕、嗜睡、头痛、呕叶、腹泻等症状。超量服用维生素B。在200mg以上,将会产生药物依赖,严重者能出现步态不稳、手足麻木等。
维生素C如果每次服用超过1g时,就可能为病毒提供养料,可谓得不偿失,还可能导致腹痛、腹泻、尿频,影响儿童生长发育、影响孕妇的胎儿发育,甚至患先天性坏血病等。
维生素D长期超量服用在1800mg后,就会出现生长停滞,影响儿童生长发育。
维生素E每日用量400~800mg后,可引起视力模糊,乳腺肿大,头痛,头晕,恶心等。长期服用超过800mg,将改变分泌代谢,免疫功能下降等。
5.无机盐
(1)人体内无机盐的作用无机盐是人体内的营养元素之一,含量虽少但对正常生理活动有重要影响。主要有以下作用:为构成人体组织的重要成分;维持机体的渗透压和体液酸碱平衡;维持神经细胞兴奋性;构成酶的成分或激活酶的活性;参与体内物质代谢等。
(2)人体内无机盐的获取及缺乏症机体在新陈代谢过程中,随时都有一定量的矿物质以不同的途径排出体外,如汗液、尿液,因此必须及时适量补充。矿物质在食物和水中广泛存在,一般不易引起缺乏。不同的生理状况和不同的地理环境或其他特殊件会引起某些元素的缺乏或过量,导致诸如克山病、骨节病等地方病的发生。
6.水
(1)水在人体内的作用水在人体中的功能是维持细胞状态,增强代谢能,调节血液的正常循环,溶解营养素,使之易于吸收和运输;水还能帮助机体排泄废弃物,散发热量,调节体温,并使血液保持酸碱平衡;水在食物消化、促进血液循环、润滑关节和各内脏器官保持它们正常的生理机能中起着重要作用;人体内的水还能使体内器官减缓震荡。
(2)人体内水的流失和获取途径
a.人体内水的流失途径:排尿、呼吸、体表排汗排粪。
b.人体内水的获取途径:饮水、食物、体内物代谢。
c.如果身体摄入水分不足,开始时人体可通过节机体减少水分的排出量,保持机体水平衡,但严重不足时,自身就无法控制了。当体内水分减少达体重的2%时,身体可因脱水而造成代谢障碍;减少7%—14% 时,出现严重的脱水症状;减少15%以上,即有生命危险。
知识点拨:
1. 纤维和纤维素:
很多学生常常存在一个认识上的误区,认为“纤维:纤维素”,其实这是两个不同的概念。纤维素是指一种特定的化学物质。纤维素通常为白色、无臭、无味、不溶于水,也不溶于一般的有机溶剂,其化学式为 (C6H10O5)n,属于多糖物质。纤维素广泛存在于自然界的植物体中,木材中有一半是纤维素,棉花是自然界中较纯粹的纤维素,脱脂棉和滤纸差不多是纯粹的纤维素纤维是指细而柔软的一类物质,分为天然纤维和化学纤维:天然纤维有植物纤维、动物纤维和矿物纤维化学纤维分为人造纤维和合成纤维。人造纤维是指利用含有纤维素的原料经化学处理和机械加工而制成的纤维。合成纤维是指利用石油、灭然气、煤为原料制成单体,再经聚合反应而生成的高分子化合物最后经拉丝工艺获得的纤维。
2. 人不能消化纤维素的原因
纤维素[(C6H10O5)n]也属于糖类,主要存存于植物体内.如树木的茎主要成分是纤维素,棉花的主要成分也是纤维素。同样是糖类,人可以从食物中摄食淀粉,并在体内将淀粉最终消化成葡萄糖加以吸收利用,但人不能消化纤维素,原因在于人体内没有纤维素酶,不能使纤维素在人体内水解。
3. 几种维生素的生理功能及来源
| 维生素A (视黄醇) | 促进人体的生长发育和防止角膜炎、夜盲症等疾病 | 鱼肝油、绿色蔬菜 |
| 维生素B1 (硫胺素) | 促进人体发育,帮助消化,防止脚气病、神经炎,可治疗皮肤病 | 酵母、谷类、肝、豆类、瘦肉 |
| 维生索B2 (核黄索) | 可防治口角炎、皮肤炎、舌炎等,能参与体内生物氧化作用 | 酵母、肝、蛋、蔬菜 |
| 维生素C (抗坏血酸) | 降低毛细血管的脆性,促进外伤的愈合,并能增强机体的抵抗力,促进胆固醇代谢 | 新鲜蔬菜和水果 |
| 维生素D (抗佝偻病) | 可预防佝偻病、软骨病和小儿出齿迟,牙齿不健全等疾病,能调节Ca、P 代谢 | 鱼肝油、蛋黄、乳类、酵母 |
| 维生素E (生育酚) | 对防止记忆力减退、抗机体早衰、预防不育症和习惯。降流产有一定作用 | 鸡蛋、肉、肝、鱼、植物油 |
知识拓展:
1. 食品添加剂:
(1)食品添加剂的界定根据1962年FAO/WHO食品法典委员会(CA 对食品添加剂的定义,食品添加剂是指:有意识地一以少量添加于食品,以改善食品的外观、风味和组织构或贮存性质的非营养物质。
(2)分类根据我国的《食品添加剂使用卫生标准》将其为:防腐剂、抗氧化剂、发色剂、漂白剂、酸味剂、凝剂、疏松剂、增稠剂、消泡剂、甜味剂、着色剂、乳化剂品质改良剂、抗结剂、增昧剂、酶制剂、被膜剂、发泡剂保鲜剂、香料、营养强化剂以及其他添加剂。
2. 认识服装的标签
当你买衣服时,怎样知道服装面料的种类呢?看服装上的标签。服装标签一般包括服装的型号、面料的纤维种类及含量、洗涤熨烫说明等内容。如果服装面料是由一种纤维材料制成的,则用“纯×”或“100% x”来表示,如“纯棉…‘纯毛”或“100%毛”;如果服装是由两种或两种以上的纤维制成的,标签上应注明每种纤维的含量,如“涤纶20%、棉80%”等。
3. 各种纤维素的燃烧鉴别法
| 织物 | 现象 |
| 尼龙 | 易燃,燃烧时有臭味,有火焰,余烬为灰褐色 |
| 涤纶 | 近火焰即熔缩,燃烧时边熔化边冒黑烟,燃烧后呈黑褐色块状.可压碎 |
| 腈纶 | 近火时先收缩,后燃烧,冒黑烟,有臭味,余烬呈黑色圆球 |
| 棉布 | 易燃烧,燃烧时无异味,余烬呈灰白色 |
| 羊毛 | 燃烧时发泡,有火焰,有烧焦羽毛的气味,余烬呈黑褐色 |
| 丝绸 | 燃烧缓慢,有臭味,余烬为黑色小球,容易压碎 |
溶质质量分数:
1. 概念:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2. 表达式:
溶质质量分数= =
=
3. 含义:溶质质量分数的含义是指每100份质量的溶液中含有溶质的质份为多少。如100g10%的NaCl溶液中含有10gNaCl.。不要误认为是100g水中含有10gNaCl。
应用溶质质量分数公式的注意事项:
①溶质的质量是指形成溶液的那部分溶质,没有进入溶液的溶质不在考虑范围之内。如在20℃时,100g水中最多能溶解36gNaCl,则20gNaCl放入50g 水中溶解后,溶质的质量只能是18g。
②溶液的质量是该溶液中溶解的全部溶质的质量与溶剂的质量之和(可以是一种或几种溶质)。
③计算时质量单位应统一。
④由于溶液的组成是指溶液中各成分在质量方面的关系,因此,对溶液组成的变化来说,某物质的质量分数只有在不超过其最大溶解范围时才有意义。
例如在20℃时,NaCl溶液中溶质的质量分数最大为26.5%,此时为该温度下氯化钠的饱和溶液,再向溶液中加入溶质也不会再溶解,浓度也不会再增大。因此离开实际去讨论溶质质量分数更大的NaCl溶液是没有意义的。
⑤运用溶质质量分数表示溶液时,必须分清溶质的质量、溶剂的质量和溶液的质量。
a.结晶水合物溶于水时,其溶质指不含结晶水的化合物。如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数= ×100%
×100%
b.当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数= 。
。
c.若两种物质能发生反应,有沉淀或气体生成,此时溶液中的溶质质量分数=
影响溶质质量分数的因素:
(1)影响溶质质量分数的因素是溶质、溶剂的质录,与温度、是否饱和无关。在改变温度的过程中若引起溶液中溶质、溶剂质量改变,溶质的质量分数也会改变,但归根结底,变温时必须考虑溶质、溶剂的质量是否改变。因而,影响溶质的质量分数的因素还是溶质、溶剂的质量。例如:
①将饱和的NaNO3溶液降低温度,由于析出品体,溶液中溶质的质缺减少,溶剂的质量不变,所以溶液中溶质的质量分数变小。
②将饱和的NaNO3溶液升高温度,只是溶液变成了不饱和溶液,溶液中溶质、溶剂的质量不变,因而溶液中溶质的质量分数不变。
(2)不要认为饱和溶液变成不饱和溶液,溶质的质量分数就变小;也不要认为不饱和溶液变成饱和溶液,溶质的质量分数就变大;要具体问题具体分析。
有关溶质质量分数计算的类型
(1)利用公式的基本计算
①已知溶质、溶剂的质量,求溶质的质量分数。
直接利用公式:溶质的质量分数= ×100%
×100%
②已知溶液、溶质的质量分数,求溶质、溶剂的质量。
利用公式:溶质的质量=溶液的质量×溶质的质量分数
溶剂的质量=溶液的质量一溶质的质量
③已知溶质的质量、溶质的质量分数,求溶液的质量。
利用公式:溶液的质量=溶质的质量÷溶质的质量分数
④质量、体积、密度与溶质质量分数的换算
当溶液的量用体积表示时,计算时应首先将溶液的体积换算成质量后再进行相关计算。因为计算溶质的质量分数的公式中各种量都是以质量来表示的,不能以体积的数据来代替。
利用公式:溶液的质量=溶液的体积×溶液的密度
(2)溶液的稀释与浓缩
注意:
a.几种溶液混合,溶液的体积不能简单相加,即V总≠VA+VB
b.混合后溶液的质量、溶质的质量可以相加,即m总=mA+mB
c. 要求混合后溶液的总体积,必须依据公式V=m/ρ,所以要知道混合溶液的密度才能求出总体积。
(3)饱和溶液中溶质质量分数的计算
a. 固体溶解度的计算公式
根据固体溶解度的计算公式[溶解度(S)= ×100g]可推导出:
×100g]可推导出: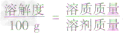 ,
,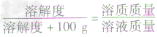
b. 溶解度与溶质质量分数的关系
特殊的溶质质量分数的计算:
(1)结晶水合物溶于水时,其溶质指不含结晶水的化合物。
如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数= ×100%
×100%
(2)溶质只能是已溶解的那一部分,没有溶解的不能做溶质计算
如20℃时,20gNaCl投入到50g中水中(20℃时,NaCl的溶解度为36g)。20℃时50g水最多只能溶解18gNaCl,如溶质的质量为18g,而不是20g,所以该NaCl溶液的质量分数=18g/(50g+18g)×100%=26.5%。
(3)当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数= 。
。
(4)某混合物溶于水,要计算某一溶质的质量分数,溶液的质量包括混合物与水的质量
如5gNaCl和1gKNO3的混合物溶于100g水,计算NaCl的溶质质量分数:
ω(NaCl)=5g/(5g+1g+100g)×100%=4.7%。
(5)利用元素的质量分数进行计算
溶液中溶质的质量分数与溶质中某元素的质量分数之间有着联系。溶液的溶质质量分数×溶质中某元素的质量分数=溶液中某元素的质量分数。
溶质质量分数的不变规律:
(1)从一瓶溶液中不论取出多少溶液,取出溶液及剩余溶液的溶质质量分数与原来溶液中溶质质量分数相同。
(2)溶质、溶质质量分数均相同的两种溶液混合,所得溶液的质量分数保持不变。
(3)一定温度时,向某饱和溶液中加入该溶质,所得溶液的溶质质量分数保持不变。
(4)一定温度时,对某饱和溶液恒温蒸发溶剂,所得溶液的溶质质量分数保持不变。
(5)对于溶解度随温度升高而增大的物质来说,将其饱和溶液(底部没有固体时)升高温度,所得溶液的溶质质量分数保持不变。而对于溶解度随温度升高而减小的物质(熟石灰)来说,降低温度,所得溶液的溶质质量分数保持不变。
1. 概念:溶液中溶质的质量分数是溶质质量与溶液质量之比。
2. 表达式:
溶质质量分数=
 =
=
3. 含义:溶质质量分数的含义是指每100份质量的溶液中含有溶质的质份为多少。如100g10%的NaCl溶液中含有10gNaCl.。不要误认为是100g水中含有10gNaCl。
应用溶质质量分数公式的注意事项:
①溶质的质量是指形成溶液的那部分溶质,没有进入溶液的溶质不在考虑范围之内。如在20℃时,100g水中最多能溶解36gNaCl,则20gNaCl放入50g 水中溶解后,溶质的质量只能是18g。
②溶液的质量是该溶液中溶解的全部溶质的质量与溶剂的质量之和(可以是一种或几种溶质)。
③计算时质量单位应统一。
④由于溶液的组成是指溶液中各成分在质量方面的关系,因此,对溶液组成的变化来说,某物质的质量分数只有在不超过其最大溶解范围时才有意义。
例如在20℃时,NaCl溶液中溶质的质量分数最大为26.5%,此时为该温度下氯化钠的饱和溶液,再向溶液中加入溶质也不会再溶解,浓度也不会再增大。因此离开实际去讨论溶质质量分数更大的NaCl溶液是没有意义的。
⑤运用溶质质量分数表示溶液时,必须分清溶质的质量、溶剂的质量和溶液的质量。
a.结晶水合物溶于水时,其溶质指不含结晶水的化合物。如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数=
 ×100%
×100%b.当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数=
 。
。c.若两种物质能发生反应,有沉淀或气体生成,此时溶液中的溶质质量分数=

影响溶质质量分数的因素:
(1)影响溶质质量分数的因素是溶质、溶剂的质录,与温度、是否饱和无关。在改变温度的过程中若引起溶液中溶质、溶剂质量改变,溶质的质量分数也会改变,但归根结底,变温时必须考虑溶质、溶剂的质量是否改变。因而,影响溶质的质量分数的因素还是溶质、溶剂的质量。例如:
①将饱和的NaNO3溶液降低温度,由于析出品体,溶液中溶质的质缺减少,溶剂的质量不变,所以溶液中溶质的质量分数变小。
②将饱和的NaNO3溶液升高温度,只是溶液变成了不饱和溶液,溶液中溶质、溶剂的质量不变,因而溶液中溶质的质量分数不变。
(2)不要认为饱和溶液变成不饱和溶液,溶质的质量分数就变小;也不要认为不饱和溶液变成饱和溶液,溶质的质量分数就变大;要具体问题具体分析。
有关溶质质量分数计算的类型
(1)利用公式的基本计算
①已知溶质、溶剂的质量,求溶质的质量分数。
直接利用公式:溶质的质量分数=
 ×100%
×100% ②已知溶液、溶质的质量分数,求溶质、溶剂的质量。
利用公式:溶质的质量=溶液的质量×溶质的质量分数
溶剂的质量=溶液的质量一溶质的质量
③已知溶质的质量、溶质的质量分数,求溶液的质量。
利用公式:溶液的质量=溶质的质量÷溶质的质量分数
④质量、体积、密度与溶质质量分数的换算
当溶液的量用体积表示时,计算时应首先将溶液的体积换算成质量后再进行相关计算。因为计算溶质的质量分数的公式中各种量都是以质量来表示的,不能以体积的数据来代替。
利用公式:溶液的质量=溶液的体积×溶液的密度
(2)溶液的稀释与浓缩
| 方法 | 计算依据 | 计算公式 | |
| 溶液的稀释 | ①加水稀释 ②加稀溶液稀释 |
①加水稀释前后,溶液中溶质的质量不变 ②用稀溶液稀释浓溶液时。稀溶液中溶质的质量与浓溶液中溶质的质量之和等于混合后溶液中溶质的质量 |
加水稀释:稀释前后溶液中溶质的质量不变 m浓×ω浓%=(m浓+m水)×ω稀% |
| 溶液的浓缩 | ①添加溶质 ②蒸发溶剂 ③加入浓溶液 | ①原溶液中的溶质与后加入的溶质质量之和等于混合后溶液中的溶质质量 ②蒸发溶剂前后溶液中溶质的质量不变(没有溶质析出) ③原溶液中的溶质与后加入浓溶液中的溶质质量之和等于混合后溶液中的溶质质量 |
蒸发浓缩:浓缩前后溶液中溶质的质量不变(m稀-m水)×ω浓%=m稀×ω稀% |
a.几种溶液混合,溶液的体积不能简单相加,即V总≠VA+VB
b.混合后溶液的质量、溶质的质量可以相加,即m总=mA+mB
c. 要求混合后溶液的总体积,必须依据公式V=m/ρ,所以要知道混合溶液的密度才能求出总体积。
(3)饱和溶液中溶质质量分数的计算
a. 固体溶解度的计算公式
根据固体溶解度的计算公式[溶解度(S)=
 ×100g]可推导出:
×100g]可推导出: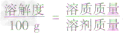 ,
,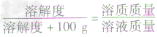
b. 溶解度与溶质质量分数的关系
| 溶解度 | 溶质质量分数 | |
| 意义 | 物质溶解性的量度,受外界温度的影响 | 表示溶液中溶质质量的多少,不受外界条件影响 |
| 容积要求 | 100g | 无要求 |
| 温度要求 | 与温度有关 | 一般与温度无关 |
| 溶液是否饱和 | 一定达到饱和 | 不一定饱和 |
| 计算公式 |  ×100g ×100g |
 |
| 单位 | 克 | 无单位 |
| 联系 | 饱和溶液中溶质的质量分数= | |
特殊的溶质质量分数的计算:
(1)结晶水合物溶于水时,其溶质指不含结晶水的化合物。
如CuSO4·5H2O溶于水时,溶质是CuSO4。
溶质质量分数=
 ×100%
×100%(2)溶质只能是已溶解的那一部分,没有溶解的不能做溶质计算
如20℃时,20gNaCl投入到50g中水中(20℃时,NaCl的溶解度为36g)。20℃时50g水最多只能溶解18gNaCl,如溶质的质量为18g,而不是20g,所以该NaCl溶液的质量分数=18g/(50g+18g)×100%=26.5%。
(3)当某些化合物溶于水时与水发生了反应,此时溶液中的溶质是反应后生成的物质。如Na2O溶于水时发生如下反应:Na2O+H2O==2NaOH。反应后的溶质是NaOH,此
溶液的溶质质量分数=
 。
。(4)某混合物溶于水,要计算某一溶质的质量分数,溶液的质量包括混合物与水的质量
如5gNaCl和1gKNO3的混合物溶于100g水,计算NaCl的溶质质量分数:
ω(NaCl)=5g/(5g+1g+100g)×100%=4.7%。
(5)利用元素的质量分数进行计算
溶液中溶质的质量分数与溶质中某元素的质量分数之间有着联系。溶液的溶质质量分数×溶质中某元素的质量分数=溶液中某元素的质量分数。
溶质质量分数的不变规律:
(1)从一瓶溶液中不论取出多少溶液,取出溶液及剩余溶液的溶质质量分数与原来溶液中溶质质量分数相同。
(2)溶质、溶质质量分数均相同的两种溶液混合,所得溶液的质量分数保持不变。
(3)一定温度时,向某饱和溶液中加入该溶质,所得溶液的溶质质量分数保持不变。
(4)一定温度时,对某饱和溶液恒温蒸发溶剂,所得溶液的溶质质量分数保持不变。
(5)对于溶解度随温度升高而增大的物质来说,将其饱和溶液(底部没有固体时)升高温度,所得溶液的溶质质量分数保持不变。而对于溶解度随温度升高而减小的物质(熟石灰)来说,降低温度,所得溶液的溶质质量分数保持不变。
概念:
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里,该温度下的溶解度。
正确理解溶解度概念的要素:
①条件:在一定温度下,影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
②标准:“在100g溶剂里”,需强调和注意的是:此处100g是溶剂的质量,而不是溶液的质量。
③状态:“达到饱和状态”,溶解度是衡址同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”。
④单位:溶解度是所溶解的质量,常用单位为克(g)。
概念的理解:
①如果不指明溶剂,通常所说的溶解度是指固体物质在水中的溶解度。
②溶解度概念中的四个关键点:“一定温度,100g 溶剂、饱和状态、溶解的质量”是同时存在的,只有四个关键点都体现出来了,溶解度的概念和应用才是有意义的,否则没有意义,说法也是不正确的。
溶解度曲线:
在平面直角坐标系里用横坐标表示温度,纵坐标表示溶解度,画出某物质的溶解度随温度变化的曲线,叫这种物质的溶解度曲线。
①表示意义
a.表示某物质在不同温度下的溶解度和溶解度随温度变化的情况;
b.溶解度曲线上的每一个点表示该溶质在某一温度下的溶解度;
c.两条曲线的交点表示这两种物质在某一相同温度下具有相同的溶解度;
d.曲线下方的点表示溶液是不饱和溶液;
e.在溶解度曲线上方靠近曲线的点表示过饱和溶液(一般物质在较高温度下制成饱和溶液,快速地降到室温,溶液中溶解的溶质的质量超过室温的溶解度,但尚未析出晶体时的溶液叫过饱和溶液)。
②溶解度曲线的变化规律
a.有些固体物质的溶解度受温度影响较大,表现在曲线“坡度”比较“陡”,如KNO3;
b.少数固体物质的溶解度受温度的影响很小,表现在曲线“坡度”比较“平”,如NaCl 。
c.极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如Ca(OH)2
③应用
a.根据溶解度曲线可以查出某物质在一定温度下的溶解度;
b.可以比较不同物质在同一温度下的溶解度大小;
c.可以知道某物质的溶解度随温度的变化情况;
d.可以选择对混合物进行分离或提纯的方法;
e.确定如何制得某温度时某物质的饱和溶液的方法等。
运用溶解度曲线判断混合物分离、提纯的方法:
根据溶解度曲线受温度变化的影响,通过改变温度或蒸发溶剂,使溶质结晶折出,从而达到混合物分离、提纯的目的。如KNO3和NaCl的混合物的分离。 (KNO3,NaCl溶解度曲线如图)
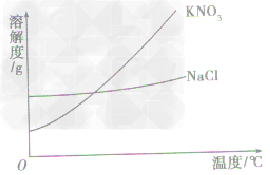
(1)温度变化对物质溶解度影响较大,要提纯这类物质。可采用降温结晶法。
具体的步骤为:①配制高温时的饱和溶液,②降温,③过滤,④干燥。如KNO3中混有少量的NaCl,提纯KNO3可用此法。
(2)温度变化对物质溶解度影响较小,要提纯这类物质,可用蒸发溶剂法。
具体步骤为:①溶解,②蒸发溶剂,③趁热过滤,④干燥。如NaCl中混有少量KNO3,要提纯NaCl,可配制溶液,然后蒸发溶剂,NaCl结晶析出,而KNO3在较高温度下,还没有达到饱和,不会结晶,趁热过滤,可得到较纯净的NaCl。
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量,叫做这种物质在这种溶剂里,该温度下的溶解度。
正确理解溶解度概念的要素:
①条件:在一定温度下,影响固体物质溶解度的内因是溶质和溶剂的性质,而外因就是温度。如果温度改变,则固体物质的溶解度也会改变,因此只有指明温度时,溶解度才有意义。
②标准:“在100g溶剂里”,需强调和注意的是:此处100g是溶剂的质量,而不是溶液的质量。
③状态:“达到饱和状态”,溶解度是衡址同一条件下某种物质溶解能力大小的标准,只有达到该条件下溶解的最大值,才可知其溶解度,因此必须要求“达到饱和状态”。
④单位:溶解度是所溶解的质量,常用单位为克(g)。
概念的理解:
①如果不指明溶剂,通常所说的溶解度是指固体物质在水中的溶解度。
②溶解度概念中的四个关键点:“一定温度,100g 溶剂、饱和状态、溶解的质量”是同时存在的,只有四个关键点都体现出来了,溶解度的概念和应用才是有意义的,否则没有意义,说法也是不正确的。
溶解度曲线:
在平面直角坐标系里用横坐标表示温度,纵坐标表示溶解度,画出某物质的溶解度随温度变化的曲线,叫这种物质的溶解度曲线。
①表示意义
a.表示某物质在不同温度下的溶解度和溶解度随温度变化的情况;
b.溶解度曲线上的每一个点表示该溶质在某一温度下的溶解度;
c.两条曲线的交点表示这两种物质在某一相同温度下具有相同的溶解度;
d.曲线下方的点表示溶液是不饱和溶液;
e.在溶解度曲线上方靠近曲线的点表示过饱和溶液(一般物质在较高温度下制成饱和溶液,快速地降到室温,溶液中溶解的溶质的质量超过室温的溶解度,但尚未析出晶体时的溶液叫过饱和溶液)。
②溶解度曲线的变化规律
a.有些固体物质的溶解度受温度影响较大,表现在曲线“坡度”比较“陡”,如KNO3;
b.少数固体物质的溶解度受温度的影响很小,表现在曲线“坡度”比较“平”,如NaCl 。
c.极少数固体物质的溶解度随温度的升高而减小,表现在曲线“坡度”下降,如Ca(OH)2
③应用
a.根据溶解度曲线可以查出某物质在一定温度下的溶解度;
b.可以比较不同物质在同一温度下的溶解度大小;
c.可以知道某物质的溶解度随温度的变化情况;
d.可以选择对混合物进行分离或提纯的方法;
e.确定如何制得某温度时某物质的饱和溶液的方法等。
运用溶解度曲线判断混合物分离、提纯的方法:
根据溶解度曲线受温度变化的影响,通过改变温度或蒸发溶剂,使溶质结晶折出,从而达到混合物分离、提纯的目的。如KNO3和NaCl的混合物的分离。 (KNO3,NaCl溶解度曲线如图)

(1)温度变化对物质溶解度影响较大,要提纯这类物质。可采用降温结晶法。
具体的步骤为:①配制高温时的饱和溶液,②降温,③过滤,④干燥。如KNO3中混有少量的NaCl,提纯KNO3可用此法。
(2)温度变化对物质溶解度影响较小,要提纯这类物质,可用蒸发溶剂法。
具体步骤为:①溶解,②蒸发溶剂,③趁热过滤,④干燥。如NaCl中混有少量KNO3,要提纯NaCl,可配制溶液,然后蒸发溶剂,NaCl结晶析出,而KNO3在较高温度下,还没有达到饱和,不会结晶,趁热过滤,可得到较纯净的NaCl。
物理变化:
1. 定义:没有生成其他物质的变化
2. 实例:灯泡发光,冰融化成水;水蒸发变成水蒸气;碘,干冰的升华,汽油挥发,蜡烛熔化等都是物理变化。
化学变化:
1. 定义:物质发生变化时生成其他物质的变化。
2. 实例:木条燃烧,铁生锈,食物腐烂
3. 现象:化学变化在生成新物质的同时,时常伴随着一些反应现象,表现为颜色改变,放出气体,生成沉淀等,化学变化不但生成其他物质,而且哈伴随着能量的变化,这种能量变化常表现为吸热,放热,发光等。
物理变化概念的理解:
(1)扩散,聚集,膨胀,压缩,挥发,摩擦生热,升温,活性炭吸附氯气等都是物理变化
(2)石墨在一定条件下变成金刚石不是物理变化而是化学变化,因为变成了另一种物质
(3)物理变化前后,物质的种类不变,组成不变,化学性质不变
(4)物理变化的实质是分子的聚集状态发生了改变,导致物质的外形或状态随之改变。
成语、俗语、古诗词蕴含的化学知识
(1)成语、俗语中的变化
①物理变化:只要功夫深,铁柞磨成针;
冰冻三尺非一日之寒;
木已成舟;滴水成冰;花香四溢等。
②化学变化:百炼成钢、点石成金、蜡炬成灰等。
(2)古诗词中的变化于谦的《石灰吟》:
千锤万凿出深山—物理变化
烈火焚烧若等闲—化学变化
粉身碎骨浑不怕—化学变化
要留清白在人间—化学变化
物质的三态变化
(1)物态变化是指同一种物质可在固态,气态,液态三种状态发生转化的过程,如下图,物态变化过程没有新物质生成,属于物理变化。

(2)物态变化过程中的名称和热量变化
1. 定义:没有生成其他物质的变化
2. 实例:灯泡发光,冰融化成水;水蒸发变成水蒸气;碘,干冰的升华,汽油挥发,蜡烛熔化等都是物理变化。
化学变化:
1. 定义:物质发生变化时生成其他物质的变化。
2. 实例:木条燃烧,铁生锈,食物腐烂
3. 现象:化学变化在生成新物质的同时,时常伴随着一些反应现象,表现为颜色改变,放出气体,生成沉淀等,化学变化不但生成其他物质,而且哈伴随着能量的变化,这种能量变化常表现为吸热,放热,发光等。
物理变化:
1. 特征:没有新物质生成。
2. 微观实质:分子本身没有变(对于由分子构成的物质),主要指形状改变或三态变化。
化学变化:
1. 特征:有新物质生成
2. 微观实质:物质发生化学变化时,反应物的分子在化学反应中分成了原子,原子重新组成构成新分子。
物理变化概念的理解:
(1)扩散,聚集,膨胀,压缩,挥发,摩擦生热,升温,活性炭吸附氯气等都是物理变化
(2)石墨在一定条件下变成金刚石不是物理变化而是化学变化,因为变成了另一种物质
(3)物理变化前后,物质的种类不变,组成不变,化学性质不变
(4)物理变化的实质是分子的聚集状态发生了改变,导致物质的外形或状态随之改变。
成语、俗语、古诗词蕴含的化学知识
(1)成语、俗语中的变化
①物理变化:只要功夫深,铁柞磨成针;
冰冻三尺非一日之寒;
木已成舟;滴水成冰;花香四溢等。
②化学变化:百炼成钢、点石成金、蜡炬成灰等。
(2)古诗词中的变化于谦的《石灰吟》:
千锤万凿出深山—物理变化
烈火焚烧若等闲—化学变化
粉身碎骨浑不怕—化学变化
要留清白在人间—化学变化
物质的三态变化
(1)物态变化是指同一种物质可在固态,气态,液态三种状态发生转化的过程,如下图,物态变化过程没有新物质生成,属于物理变化。

(2)物态变化过程中的名称和热量变化
| 变化过程 | 名称 | 热量变化 |
| 固态→气态 | 升华 | 吸热 |
| 气态→固态 | 凝华 | 放热 |
| 固态→液态 | 熔化 | 吸热 |
| 液态→固态 | 凝固 | 放热 |
| 液态→气态 | 汽化 | 吸热 |
| 气态→液态 | 液化 | 放热 |
光合作用:
光合作用(Photosynthesis),即光能合成作用,是植物、藻类和某些细菌,在可见光的照射下,经过光反应和暗反应,利用光合色素,将二氧化碳(或硫化氢)和水转化为有机物,并释放出氧气(或氢气)的生化过程。光合作用是一系列复杂的代谢反应的总和,是生物界赖以生存的基础,也是地球碳氧循环的重要媒介。
呼吸作用:
生物体内的有机物在细胞内经过一系列的氧化分解,最终生成二氧化碳或其他产物,并且释放出能量的总过程,叫做呼吸作用。呼吸作用,是生物体在细胞内将有机物氧化分解并产生能量的化学过程,是所有的动物和植物都具有一项生命活动。生物的生命活动都需要消耗能量,这些能量来自生物体内糖类、脂类和蛋白质等有机物的氧化分解。生物体内有机物的氧化分解为生物提供了生命所需要的能量,具有十分重要的意义。
光合作用:
二氧化碳可促进植物的光合作用:
6CO2+6H2O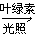 C6H12O6+6O2(是一个消耗二氧化碳放出氧气的过程)
C6H12O6+6O2(是一个消耗二氧化碳放出氧气的过程)
呼吸作用:
C6H12O6+6O2===6CO2+6H2O(是一个消耗氧气和能量放出二氧化碳的过程)
光合作用(Photosynthesis),即光能合成作用,是植物、藻类和某些细菌,在可见光的照射下,经过光反应和暗反应,利用光合色素,将二氧化碳(或硫化氢)和水转化为有机物,并释放出氧气(或氢气)的生化过程。光合作用是一系列复杂的代谢反应的总和,是生物界赖以生存的基础,也是地球碳氧循环的重要媒介。
呼吸作用:
生物体内的有机物在细胞内经过一系列的氧化分解,最终生成二氧化碳或其他产物,并且释放出能量的总过程,叫做呼吸作用。呼吸作用,是生物体在细胞内将有机物氧化分解并产生能量的化学过程,是所有的动物和植物都具有一项生命活动。生物的生命活动都需要消耗能量,这些能量来自生物体内糖类、脂类和蛋白质等有机物的氧化分解。生物体内有机物的氧化分解为生物提供了生命所需要的能量,具有十分重要的意义。
光合作用:
二氧化碳可促进植物的光合作用:
6CO2+6H2O
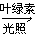 C6H12O6+6O2(是一个消耗二氧化碳放出氧气的过程)
C6H12O6+6O2(是一个消耗二氧化碳放出氧气的过程) 呼吸作用:
C6H12O6+6O2===6CO2+6H2O(是一个消耗氧气和能量放出二氧化碳的过程)
发现相似题
与“利用化学知识对下列说法进行判断,其中正确的是( )A.咀嚼...”考查相似的试题有:
- “徐福记沙琪玛”是人们喜爱的食品之一,下图是其标签中的一部分,其中小麦粉、鸡蛋、食用棕榈油依次宿含六大营养索(蛋白质、...
- 食物的主要营养素有蛋白质、维生素、无机盐、油脂、______、______等六大类.食品保鲜有多种方法,在食品保鲜中,下列物质经...
- 以下列举的是生活和学习中可能遇到的某些情况,根据你所学的知识与掌握的技能回答:(1)通常所说的煤气中毒是指 引起的中毒...
- 生活中下列说法正确的是[ ]A. 喜欢吃什么,就吃什么B. 对垃圾进行分类存放C. 用金属器皿盛装酸性食物D. 用甲醛水溶液浸泡食用...
- 为了测定生铁中含铁量,甲、乙、丙三位同学分别取该生铁与溶质质量分数相同的稀盐酸进行实验,其中只有一位同学所取盐酸与生...
- 请仔细阅读溶解度曲线图,回答下列问题:(1)P点表示的意义是______(2)t1℃时,三种物质的溶解度从大到小的顺序是______(3...
- 图1是甲、乙、丙三种固体物质的溶解度曲线。根据图1、图2回答:(1)50℃时,甲、乙、丙三种固体物质的溶解度由大到小的顺序是...
- 某温度时,将KCl的饱和溶液11.2克,蒸于后得到3.2克KCl固体,则该温度时KCl的溶解度为( )A.8.0克B.28.6克C.40.0克D.71.4克
- 分别称取36g NaCl、KNO3固体放入两只烧杯中,在20℃时分别加入100g水,充分搅拌后,有如图所示的现象.请结合NaCl、KNO3的溶解...
- 植物气孔的主要作用中.除了散发燕腾作用过程中的水蒸气以外,还具有下列哪项作用( )A.吸收水分B.吸收无机盐C.二氧化碳...