本试题 “下列关于空气的说法中,错误的是[ ]A.氯酸钾和二氧化锰制氧气不属于分解反应,因为反应物有两种B.空气是一种十分重要的天然资源C.若少量有害物质进入空气...” 主要考查您对空气的成分
空气的污染和防治
分解反应
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 空气的成分
- 空气的污染和防治
- 分解反应
空气的成分:
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
氧气,二氧化碳,氢气,氮气,稀有气体;按体积分:N2占78%,O2占21%,稀有气体占0.94%,二氧化碳占0.03%,其他气体和杂质占0.03%。
易错点:
空气中各成分的含量在一定时间和一定范围内基本恒定,但随着人类活动的延续,气体的排放,空气的成分也在不停地变化,因此不能认为空气的成分是一成不变的。
空气污染:
即空气中含有一种或多种污染物,其存在的量、性质及时间会伤害到人类、植物及动物的生命,损害财物、或干扰舒适的生活环境,如臭味的存在。换言之,只要是某一种物质其存在的量,性质及时间足够对人类或其他生物、财物产生影响者,我们就可以称其为空气污染物;而其存在造成之现象,就是空气污染。换言之,某些物质在空气中不正常的增量就产生空气污染的情形。
空气污染治理:
1. 空气污染及来源
导致空气质量下降的污染物很多。目前量多且危害严重的空气污染物主要有二氧化硫(SO2)、氮氧化物 (NO2)、一氧化碳(CO)和可吸入颗粒物等。如下表所示:
2. 空气污染的危害
①酸雨:SO2、NOx等气体形成酸雨。
②臭氧层破坏:氟利昂的释放,加速臭氧分解。
③其他危害:空气污染严重危害了人体健康,影响了农作物生长,破坏了生态平衡。
3. 空气污染的防治
①改善燃料结构,尽量充分燃烧液体燃料和气体燃料。
②对化石燃料进行脱硫、脱氮处理,工厂的废气要经过处理再排放。
③开发新能源,如太阳能、风能、水能、地热能等。
④大力开展植树造林活动,提高环境的自我净化能力。
空气质量日报:
空气质量日报的主要内容:空气污染指数,首要污染物,空气质量级别,空气质量状况。
计入空气污染指数的项目:二氧化硫,一氧化碳,二氧化氮,可吸入颗粒物,臭氧等。
空气质量级别:
PM2.5
(1)什么是PM2.5:PM2.5是指大气中小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。它的直径还不到人的头发丝粗细的1/20。虽然PM2.5只是地球大气成分中含量很少的组分,但对空气质量和能见度等有重要影响。
(2)PM2.5的性状:与较粗的大气颗粒物相比,PM2.5粒径小,富含大量的有毒,有害物质且能在大气中停留时间长,输送距离远,因而对人体健康和大气环境质量的影响更大。
(3)PM2.5的来源:主要来源是日常发电,工业生产,汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属的等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自道路扬尘等,2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(机动车尾气,燃烧)、挥发性有机物等。
(4)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。
室内空气污染:
指由于各种原因导致的室内空气中有害物质超标.进而影响人体健康的室内环境污染。有害物质包括甲醛、苯、氨、放射性物质等。
即空气中含有一种或多种污染物,其存在的量、性质及时间会伤害到人类、植物及动物的生命,损害财物、或干扰舒适的生活环境,如臭味的存在。换言之,只要是某一种物质其存在的量,性质及时间足够对人类或其他生物、财物产生影响者,我们就可以称其为空气污染物;而其存在造成之现象,就是空气污染。换言之,某些物质在空气中不正常的增量就产生空气污染的情形。
空气污染治理:
1. 空气污染及来源
导致空气质量下降的污染物很多。目前量多且危害严重的空气污染物主要有二氧化硫(SO2)、氮氧化物 (NO2)、一氧化碳(CO)和可吸入颗粒物等。如下表所示:
| 空气污染物 | 主要来源 |
| 二氧化硫 | 煤、石油等燃料的燃烧,生产硫酸等工厂排放的尾气 |
| 一氧化碳 | 化石燃料等不完全燃烧 |
| 氮氧化物 | 机动车辆等排放的废气 |
| 可吸入颗粒物 | 地面扬尘、燃煤排放的粉尘等 |
2. 空气污染的危害
①酸雨:SO2、NOx等气体形成酸雨。
②臭氧层破坏:氟利昂的释放,加速臭氧分解。
③其他危害:空气污染严重危害了人体健康,影响了农作物生长,破坏了生态平衡。
3. 空气污染的防治
①改善燃料结构,尽量充分燃烧液体燃料和气体燃料。
②对化石燃料进行脱硫、脱氮处理,工厂的废气要经过处理再排放。
③开发新能源,如太阳能、风能、水能、地热能等。
④大力开展植树造林活动,提高环境的自我净化能力。
空气质量日报:
空气质量日报的主要内容:空气污染指数,首要污染物,空气质量级别,空气质量状况。
计入空气污染指数的项目:二氧化硫,一氧化碳,二氧化氮,可吸入颗粒物,臭氧等。
空气质量级别:
| 污染指数 | 50以下 | 51-100 | 101-150 | 151-200 | 201-250 | 251-300 | 300以上 |
| 质量级别 | Ⅰ | Ⅱ | Ⅲ⑴ | Ⅲ⑵ | Ⅳ⑴ | Ⅳ⑵ | Ⅴ |
| 质量状况 | 优 | 良 | 轻微污染 | 轻度污染 | 中度污染 | 中度重污染 | 重度污染 |
PM2.5
(1)什么是PM2.5:PM2.5是指大气中小于或等于2.5微米的颗粒物,也称为可入肺颗粒物。它的直径还不到人的头发丝粗细的1/20。虽然PM2.5只是地球大气成分中含量很少的组分,但对空气质量和能见度等有重要影响。
(2)PM2.5的性状:与较粗的大气颗粒物相比,PM2.5粒径小,富含大量的有毒,有害物质且能在大气中停留时间长,输送距离远,因而对人体健康和大气环境质量的影响更大。
(3)PM2.5的来源:主要来源是日常发电,工业生产,汽车尾气排放等过程中经过燃烧而排放的残留物,大多含有重金属的等有毒物质。一般而言,粒径2.5微米至10微米的粗颗粒物主要来自道路扬尘等,2.5微米以下的细颗粒物(PM2.5)则主要来自化石燃料的燃烧(机动车尾气,燃烧)、挥发性有机物等。
(4)2012年2月,国务院同意发布新修订的《环境空气质量标准》增加了PM2.5监测指标。
室内空气污染:
指由于各种原因导致的室内空气中有害物质超标.进而影响人体健康的室内环境污染。有害物质包括甲醛、苯、氨、放射性物质等。
概念:
由一种物质生成两种或两种以上物质的反应
特征:
一变多
表达式:
A = B + C
初中常见的分解反应:
按产物种类多少分类:
一、加热分解的产物有两种
1.分解成两种单质
⑴气态氢化物的分解
碘化氢的分解2HI=H2↑+I2
⑵氯化银的分解
氯化银的分解2AgCl=2Ag+Cl2↑
⑶电解
电解水2H2O 2H2↑+O2↑
2H2↑+O2↑
2.分解成两种化合物
⑴不稳定盐类的分解
碳酸钙的高温分解CaCO3 CaO+CO2↑
CaO+CO2↑
⑵不稳定弱碱的分解
氢氧化铝受热分解2Al(OH)3=Al2O3+3H2O
⑶不稳定弱酸的分解
碳酸的分解H2CO3=H2O+CO2↑
⑷含结晶水的盐类的脱水
十水碳酸钠的风化Na2CO3·10H2O=Na2CO3+10H2O
3.分解成一种单质和一种化合物
⑴不太稳定的盐类的分解
氯酸钾的催化分解2KClO3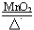 2KCl+3O2↑
2KCl+3O2↑
⑵不稳定酸的分解
次氯酸的分解2HClO=2HCl+O2
⑶双氧水的分解
受热(或以二氧化锰为催化剂)分解2H2O2=2H2O+O2
4.有机物的分解
甲烷的裂解2CH4=C2H2+3H2
二、加热分解的产物有三种
1.不稳定盐类的分解
⑴碳酸氢钠受热分解2NaHCO3=Na2CO3+CO2↑+H2O
⑵亚硫酸的酸式强碱盐受热分解
亚硫酸氢钠受热分解 2NaHSO3=Na2SO4+SO2↑+H2O
⑶铵盐的受热分解
碳酸铵受热分解
(NH4)2CO3=2NH3↑+H2O↑+CO2↑
⑷高锰酸钾受热分解
2KMnO4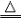 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
⑸硝酸盐的受热分解
硝酸银的受热分解2AgNO3=2Ag+2NO2↑+O2↑
2.硝酸的分解
4HNO3=4NO2+O2+2H2O
3.电解水溶液
⑴电解饱和食盐水
2NaCl+2H2O=2NaOH+H2↑+Cl2↑
按反应物种类进行分类:
1.酸的分解反应。
⑴含氧酸=非金属氧化物+水 如H2CO3=CO2↑+H2O,H2SO3=SO2↑+H2O
⑵某些含氧酸的分解比较特殊, 如
硝酸的分解: 4HNO3(浓)=4NO2↑+O2↑+2H2O,
次氯酸分解 2HClO=2HCl+O2↑
磷酸脱水 4H3PO4 (HPO3)4+4H2O↑ ;
(HPO3)4+4H2O↑ ;
2H3PO4 H4P2O7+H2O↑
H4P2O7+H2O↑
3H3PO4 H5P3O10+2H2O↑
H5P3O10+2H2O↑
2.碱的分解反应:
活泼金属的氢氧化物较难分解,难溶性碱一般都较易分解: 2Al(OH)3=Al2O3+3H2O, 2Fe(OH)3=Fe2O3+3H2O, Cu(OH)2=CuO十H2O。
3.盐的分解反应:
碳酸盐、硝酸盐、铵盐一般都较易分解,且反应表现出一定的规律性。
⑴碳酸盐的分解:
碳酸盐=金属氧化物十CO2↑ 如CaCO3 CaO+CO2↑,CuCO3
CaO+CO2↑,CuCO3 CuO+CO2↑
CuO+CO2↑
K2CO3、Na2CO3比较稳定,很难分解,而其酸式盐较易分解:
2NaHCO3=Na2CO3+CO2↑+H2O
Ca(HCO3)2=CaCO3+CO2↑+H2O
⑵硝酸盐的分解反应。硝酸盐受热均易分解,并放出氧气,其规律大体如下:
活动性强的金属(K、Ca、Na)硝酸盐=亚硝酸盐+O2↑:
如 2KNO3=2KNO2+O2↑。
处于活动性顺序表中间的金属(Mg、Cu等)的硝酸盐=金属氧化物+NO2↑+O2↑:
如2Mg(NO3)2=2MgO+4NO2↑+O2↑ 2Cu(NO3)2=2CuO+4NO2↑+O2↑
不活动金属(Hg、Ag、Au)的硝酸盐=金属+NO2↑+O2↑:
如 Hg(NO3)2=Hg+2NO2↑+O2↑; 2AgNO3=2Ag+2NO2↑+O2↑
⑶铵盐的分解反应。铵盐受热易分解,一般都有氨气放出:
如(NH4)2SO4=2NH3↑+H2SO4 ;NH4HCO3=NH3↑+CO2↑+H2O。
⑷其它盐类的分解反应
如 2KClO3=2KCl+3O2↑ 2KMnO4=K2MnO4+MnO2+O2↑
4.氧化物的分解反应:
非金属氧化物一般不容易发生分解反应 2H2O2=H2↑+O2↑
金属氧化物一般分解的规律是: 金属活动顺序表中,排在铜后的金属氧化物受热易分解:
如 2HgO=2Hg+O2↑,2Ag2O=4Ag+O2↑
活泼的金属氧化物,给它们熔化态通电流可使其分解:
如2Al2O3(熔化)=4Al+3O2↑
由一种物质生成两种或两种以上物质的反应
特征:
一变多
表达式:
A = B + C
初中常见的分解反应:
按产物种类多少分类:
一、加热分解的产物有两种
1.分解成两种单质
⑴气态氢化物的分解
碘化氢的分解2HI=H2↑+I2
⑵氯化银的分解
氯化银的分解2AgCl=2Ag+Cl2↑
⑶电解
电解水2H2O
 2H2↑+O2↑
2H2↑+O2↑2.分解成两种化合物
⑴不稳定盐类的分解
碳酸钙的高温分解CaCO3
 CaO+CO2↑
CaO+CO2↑ ⑵不稳定弱碱的分解
氢氧化铝受热分解2Al(OH)3=Al2O3+3H2O
⑶不稳定弱酸的分解
碳酸的分解H2CO3=H2O+CO2↑
⑷含结晶水的盐类的脱水
十水碳酸钠的风化Na2CO3·10H2O=Na2CO3+10H2O
3.分解成一种单质和一种化合物
⑴不太稳定的盐类的分解
氯酸钾的催化分解2KClO3
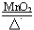 2KCl+3O2↑
2KCl+3O2↑⑵不稳定酸的分解
次氯酸的分解2HClO=2HCl+O2
⑶双氧水的分解
受热(或以二氧化锰为催化剂)分解2H2O2=2H2O+O2
4.有机物的分解
甲烷的裂解2CH4=C2H2+3H2
二、加热分解的产物有三种
1.不稳定盐类的分解
⑴碳酸氢钠受热分解2NaHCO3=Na2CO3+CO2↑+H2O
⑵亚硫酸的酸式强碱盐受热分解
亚硫酸氢钠受热分解 2NaHSO3=Na2SO4+SO2↑+H2O
⑶铵盐的受热分解
碳酸铵受热分解
(NH4)2CO3=2NH3↑+H2O↑+CO2↑
⑷高锰酸钾受热分解
2KMnO4
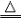 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑ ⑸硝酸盐的受热分解
硝酸银的受热分解2AgNO3=2Ag+2NO2↑+O2↑
2.硝酸的分解
4HNO3=4NO2+O2+2H2O
3.电解水溶液
⑴电解饱和食盐水
2NaCl+2H2O=2NaOH+H2↑+Cl2↑
按反应物种类进行分类:
1.酸的分解反应。
⑴含氧酸=非金属氧化物+水 如H2CO3=CO2↑+H2O,H2SO3=SO2↑+H2O
⑵某些含氧酸的分解比较特殊, 如
硝酸的分解: 4HNO3(浓)=4NO2↑+O2↑+2H2O,
次氯酸分解 2HClO=2HCl+O2↑
磷酸脱水 4H3PO4
 (HPO3)4+4H2O↑ ;
(HPO3)4+4H2O↑ ;2H3PO4
 H4P2O7+H2O↑
H4P2O7+H2O↑ 3H3PO4
 H5P3O10+2H2O↑
H5P3O10+2H2O↑ 2.碱的分解反应:
活泼金属的氢氧化物较难分解,难溶性碱一般都较易分解: 2Al(OH)3=Al2O3+3H2O, 2Fe(OH)3=Fe2O3+3H2O, Cu(OH)2=CuO十H2O。
3.盐的分解反应:
碳酸盐、硝酸盐、铵盐一般都较易分解,且反应表现出一定的规律性。
⑴碳酸盐的分解:
碳酸盐=金属氧化物十CO2↑ 如CaCO3
 CaO+CO2↑,CuCO3
CaO+CO2↑,CuCO3 CuO+CO2↑
CuO+CO2↑K2CO3、Na2CO3比较稳定,很难分解,而其酸式盐较易分解:
2NaHCO3=Na2CO3+CO2↑+H2O
Ca(HCO3)2=CaCO3+CO2↑+H2O
⑵硝酸盐的分解反应。硝酸盐受热均易分解,并放出氧气,其规律大体如下:
活动性强的金属(K、Ca、Na)硝酸盐=亚硝酸盐+O2↑:
如 2KNO3=2KNO2+O2↑。
处于活动性顺序表中间的金属(Mg、Cu等)的硝酸盐=金属氧化物+NO2↑+O2↑:
如2Mg(NO3)2=2MgO+4NO2↑+O2↑ 2Cu(NO3)2=2CuO+4NO2↑+O2↑
不活动金属(Hg、Ag、Au)的硝酸盐=金属+NO2↑+O2↑:
如 Hg(NO3)2=Hg+2NO2↑+O2↑; 2AgNO3=2Ag+2NO2↑+O2↑
⑶铵盐的分解反应。铵盐受热易分解,一般都有氨气放出:
如(NH4)2SO4=2NH3↑+H2SO4 ;NH4HCO3=NH3↑+CO2↑+H2O。
⑷其它盐类的分解反应
如 2KClO3=2KCl+3O2↑ 2KMnO4=K2MnO4+MnO2+O2↑
4.氧化物的分解反应:
非金属氧化物一般不容易发生分解反应 2H2O2=H2↑+O2↑
金属氧化物一般分解的规律是: 金属活动顺序表中,排在铜后的金属氧化物受热易分解:
如 2HgO=2Hg+O2↑,2Ag2O=4Ag+O2↑
活泼的金属氧化物,给它们熔化态通电流可使其分解:
如2Al2O3(熔化)=4Al+3O2↑
发现相似题
与“下列关于空气的说法中,错误的是[ ]A.氯酸钾和二氧化锰制氧...”考查相似的试题有:
- 属于稀有气体的是( )A.氢气B.氦气C.氮气D.氯气
- 到我省迪庆州梅里雪山旅游时,有的人常常会感到呼吸困难,这是因为空气成分中( )A.氧气的体积分数远大于2l%B.氮气的体积...
- 空气、水是人类赖以生存的自然资源.测定空气中氧气体积分数的实验装置如图所示.在集气瓶内加入少量的水,并五等分水面以上...
- 小明同学在用右图所示装置测量空气中氧气含量实验时,发现集气瓶中进入的水的体积小于瓶子容积的15,请你帮助他查找出可能导...
- 下列变化,与空气的成分无关的是( )A.敞口放置的石灰水表面出现一层白膜B.敞口放置的浓盐酸变稀C.酥脆的饼干置于空气中...
- 用教材上的装置测定空气中的氧气含量,实验后发现测得氧气的体积小于1/5,针对这一事实,你认为下列做法或想法不可取的是( ...
- 生活处处皆化学,下列做法不合理的是( )A.为使粮食不变质,在粮库内充入氮气B.爆竹的生产和销售统一管理C.为保持皮蛋香...
- (1)2011年3月,年产100万吨聚氯乙烯项目在清镇开工建设,这对贵阳市落实“工业强市”的战略起到了积极作用。聚氯乙烯是以氯乙烯...
- 下列反应中,属于分解反应的是[ ]A. 氧化钠+水→氢氧化钠B. 碱式碳酸铜氧化铜+水+二氧化碳C. 甲烷+氧气二氧化碳+水D. 镁...
- 下列说法正确的是[ ]A.氧化反应一定是化合反应B.没有颜色和气味的气体一定是空气C.盐水蒸发后变成盐和水蒸气,所以盐水蒸...