本试题 “下列做法或报道有科学依据的是( )A.高828米的迪拜塔使用大量的纯铁作建筑材料,因为纯铁的硬度大B.工人疏通天然气管道时,通入氮气后引起爆炸死伤二十多...” 主要考查您对粗盐的提纯
爆炸、自燃
金属的化学性质
一氧化碳的毒性
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 粗盐的提纯
- 爆炸、自燃
- 金属的化学性质
- 一氧化碳的毒性
粗盐提纯:
粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+,Mg2+,SO42-等。不溶性杂质可以用过滤的方法除去,可溶性杂质中的Ca2+,Mg2+,SO42-则可通过加入BaCl2、NaOH和Na2CO3溶液,生成沉淀而除去,也可加入BaCO3固体和NaOH溶液来除去。然后蒸发水分得到较纯净的精盐。
粗盐提纯实验:
1. 实验过程:
(1)溶解
(2)在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐。
(3)加入过量BaCl2(去除硫酸根离子)BaCl2+Na2SO4==BaSO4↓+2NaCl
(4)加入过量NaOH(去除镁离子)MgCl2+2NaOH==Mg(OH)2↓+2NaCl
(5)加入过量Na2CO3(去除钙离子及BaCl2中的钡离子)Na2CO3+CaCl2==CaCO3↓+2NaCl
(6)Na2CO3+BaCl2==BaCO3↓+2NaCl
(注:3,4两步可互换。)
(7)过滤
向滤液中加入适量HCl(除去过量NaOH,Na2CO3,可选择用pH试纸控制加入的量,或是直接蒸发)
(8)蒸发结晶
2. 实验步骤:
(1)溶解:
用托盘天平称取5克粗盐(精确到0.1克),用量筒量取10毫升水倒入烧杯里,
用药匙取一匙粗盐加入水中,观察发生的现象,用玻璃棒搅拌,并观察发生的现象。
接着再加入粗盐,边加边用玻璃棒搅拌,一直加到粗盐不再溶解时为止,观察溶液是否浑浊。
(2)过滤:
将滤纸折叠后用水润湿使其紧贴漏斗内壁并使滤纸上沿低于漏斗口,溶液液面低于滤纸上沿,
倾倒液体的烧杯口要紧靠玻璃棒,玻璃棒的末端紧靠有三层滤纸的一边,漏斗末端紧靠承接
滤液的烧杯的内壁。慢慢倾倒液体,待滤纸内无水时,仔细观察滤纸上的剩余物及滤液的颜色,
滤液仍浑浊时,应该再过滤一次。
(3)蒸发:
把得到的澄清滤液倒入蒸发皿,把蒸发皿放在铁架台的铁圈上,用酒精灯加热同时用玻璃棒
不断搅拌滤液,等到蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干。
(4)用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器,比较提纯前后食盐的状态
并计算精盐的产率。
(5)去除可溶性杂质:溶解,依次加入过BaCl2,NaOH,Na2CO3过滤。向滤液中加入适量HCl,
蒸发,结晶。
产率计算:
将提纯后的氯化钠与粗盐作比较,计算精盐的产率。
(误差分析:明显偏低:A.溶解时将粗盐一次全部倒入水中,立即过滤B.蒸发时,有一些液体、固体溅出。
偏高:提纯后的精盐尚未完全干燥就称其质量.粗盐中含有其他可溶性固体。)
元素变化:
反应前:NaCl、MgCl2、CaCl2、Na2SO4
加入BaCl2(过量)产生BaSO4沉淀溶液内还剩:NaCl、MgCl2、CaCl2、BaCl2
加入Na2CO3(过量)产生CaCO3沉淀和BaCO3沉淀溶液内还剩:NaCl、MgCl2、Na2CO3
加入NaOH(过量)产生Mg(OH)2沉淀溶液内还剩:NaCl、Na2CO3、NaOH
加入HCl(过量)产生CO2、H2O溶液内还剩:HCl、NaCl
蒸发后:NaCl
实验现象:
溶解:粗盐固体为灰色,加入水中所得液体呈浑浊状。
过滤:滤液是无色透明液体,滤纸上的残留物呈黑色。
蒸发:随着加热,蒸发皿中液体的量减少;当蒸发到一定程度时,蒸发皿底部有固体析出。蒸发得到的固体为白色。
过程中玻璃棒的作用:
(1)溶解时:搅拌,加速溶解
(2)过滤时:引流
(3)蒸发时:搅拌,使液体均匀受热,防止液体飞溅
粗盐中含有泥沙等不溶性杂质,以及可溶性杂质如:Ca2+,Mg2+,SO42-等。不溶性杂质可以用过滤的方法除去,可溶性杂质中的Ca2+,Mg2+,SO42-则可通过加入BaCl2、NaOH和Na2CO3溶液,生成沉淀而除去,也可加入BaCO3固体和NaOH溶液来除去。然后蒸发水分得到较纯净的精盐。
粗盐提纯实验:
1. 实验过程:
(1)溶解
(2)在天平上称量剩下的粗盐,计算在10毫升水中大约溶解了多少克粗盐。
(3)加入过量BaCl2(去除硫酸根离子)BaCl2+Na2SO4==BaSO4↓+2NaCl
(4)加入过量NaOH(去除镁离子)MgCl2+2NaOH==Mg(OH)2↓+2NaCl
(5)加入过量Na2CO3(去除钙离子及BaCl2中的钡离子)Na2CO3+CaCl2==CaCO3↓+2NaCl
(6)Na2CO3+BaCl2==BaCO3↓+2NaCl
(注:3,4两步可互换。)
(7)过滤
向滤液中加入适量HCl(除去过量NaOH,Na2CO3,可选择用pH试纸控制加入的量,或是直接蒸发)
(8)蒸发结晶
2. 实验步骤:
(1)溶解:
用托盘天平称取5克粗盐(精确到0.1克),用量筒量取10毫升水倒入烧杯里,
用药匙取一匙粗盐加入水中,观察发生的现象,用玻璃棒搅拌,并观察发生的现象。
接着再加入粗盐,边加边用玻璃棒搅拌,一直加到粗盐不再溶解时为止,观察溶液是否浑浊。
(2)过滤:
将滤纸折叠后用水润湿使其紧贴漏斗内壁并使滤纸上沿低于漏斗口,溶液液面低于滤纸上沿,
倾倒液体的烧杯口要紧靠玻璃棒,玻璃棒的末端紧靠有三层滤纸的一边,漏斗末端紧靠承接
滤液的烧杯的内壁。慢慢倾倒液体,待滤纸内无水时,仔细观察滤纸上的剩余物及滤液的颜色,
滤液仍浑浊时,应该再过滤一次。
(3)蒸发:
把得到的澄清滤液倒入蒸发皿,把蒸发皿放在铁架台的铁圈上,用酒精灯加热同时用玻璃棒
不断搅拌滤液,等到蒸发皿中出现较多量固体时,停止加热,利用蒸发皿的余热使滤液蒸干。
(4)用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器,比较提纯前后食盐的状态
并计算精盐的产率。
(5)去除可溶性杂质:溶解,依次加入过BaCl2,NaOH,Na2CO3过滤。向滤液中加入适量HCl,
蒸发,结晶。
产率计算:
将提纯后的氯化钠与粗盐作比较,计算精盐的产率。
(误差分析:明显偏低:A.溶解时将粗盐一次全部倒入水中,立即过滤B.蒸发时,有一些液体、固体溅出。
偏高:提纯后的精盐尚未完全干燥就称其质量.粗盐中含有其他可溶性固体。)
元素变化:
反应前:NaCl、MgCl2、CaCl2、Na2SO
加入BaCl2(过量)产生BaSO4沉淀溶液内还剩:NaCl、MgCl2、CaCl2、BaCl2
加入Na2CO3(过量)产生CaCO3沉淀和BaCO3沉淀溶液内还剩:NaCl、MgCl2、Na2CO3
加入NaOH(过量)产生Mg(OH)2沉淀溶液内还剩:NaCl、Na2CO3、NaOH
加入HCl(过量)产生CO2、H2O溶液内还剩:HCl、NaCl
蒸发后:NaCl
实验现象:
溶解:粗盐固体为灰色,加入水中所得液体呈浑浊状。
过滤:滤液是无色透明液体,滤纸上的残留物呈黑色。
蒸发:随着加热,蒸发皿中液体的量减少;当蒸发到一定程度时,蒸发皿底部有固体析出。蒸发得到的固体为白色。
过程中玻璃棒的作用:
(1)溶解时:搅拌,加速溶解
(2)过滤时:引流
(3)蒸发时:搅拌,使液体均匀受热,防止液体飞溅
自燃:
1. 概念:自燃是由缓慢氧化引起的自发燃烧。如果缓慢氧化产生的热量不能及时散失,就会越积越多,当温度升高到可燃物的着火点时,如果再遇到氧气就会引起自发的燃烧,这就是自燃。
爆炸:
1. 概念:通常说的爆炸指可燃物拒有限空间内急速燃烧,短时间内聚积大量的热量,使气体体积迅速膨胀引起的爆炸。
自燃:
露在地表的煤层,由于气候炎热,发生缓慢氧化反应而导致自燃。
贮存棉花、饲草的仓库,沾满机器油的破布、棉丝等堆积时间长了,通风不好有时就会自燃。在干燥的季节,森林也会自燃。
在坟地里出现“磷火”也是一种自燃现象。
人和动物机体里含磷的有机物腐败分解能生成磷化氢气体。这种气体着火点很低,接触空气就会自燃。在缺乏科学知识的时代,常把这种自燃现象说成是“鬼火”。
平时将白磷浸泡在冷水里,防止自燃。白磷的着火点低(40℃),可用它做自燃实验。取出少许白磷溶解在二硫化碳中,然后把溶液倒在滤纸上,待二硫化碳挥发后,白磷在滤纸上与空气中氧气充分接触就会自燃。
爆炸:
爆炸是我们日常生活中常见的观象,但有的爆炸仅仅是由物理变化引起的,如轮胎爆炸;有螳爆炸则是由化学变化引起的,如火药爆炸,汽油、液化气等燃料的爆炸等。其中,由化学变化引起的爆炸是学习的重点,这种类型的爆炸主要是由于:
①在有限的空间 (如炸弹)内,发生急速的燃烧,短时问聚积大量的热,使气体的体积迅速膨胀;
②氧气的浓度高,或者可燃物 (气体、粉尘)与氧气的接触面积很大,燃烧范围广,周围的空气迅速猛烈膨胀。防止这类爆炸的方法:通风,禁止烟火等。
燃烧,缓慢氧化,自燃,爆炸(由化学变化引起)的比较:
| 燃烧 | 缓慢氧化 | 自燃 | 爆炸 | |
| 概念 | 可燃物与氧气发生的一种发光放热的剧烈的氧化反应 | 缓慢进行的氧化反应 | 由缓慢氧化引起的自发燃烧 | 可燃物在有限空间内发生的急速燃烧 |
| 能量变化 | 放热明显 | 放出热量随时散失 | 放热明显 | 放热明显 |
| 温度 | 达到可燃物的着火点 | 未达到可燃物的着火点 | 达到可燃物的着火点 | 达到可燃物的着火点 |
| 是否发光 | 发光 | 无明显发光现象 | 发光 | 发光 |
| 联系 | 均属于氧化反应,均放出热量 | |||
易燃易爆物的安全知识:
(1)易燃物:一般来说,易燃物指的是那些易燃的气体和液体,容易燃烧、自燃或遇水可以燃烧的固体,以及一些可以引起其他物质燃烧的物质等。常见的有硫;磷、酒精,液化石油气、氢气、乙炔、沼气、石油产品、面粉、棉絮等。
(2)易爆物:指的是那受热或受到撞击时.容易发生爆炸的物质。
(3)一些与燃烧和爆炸有关的图标:

(4)再生产、运输、使用、储存易燃、易爆物时的注意事项:
①对厂房和仓库的要求:与周围建筑物间有足够的防火距离。车间,仓库要有防火、防爆、通风、静电除尘、消防等器材设备,严禁烟火,杜绝一切可能产生火花的因素。容器要求:要牢固、密封、警示标志明显且要注明物品名称、化学性质、注意事项。
③存放要求:单存、单放、远离火种:注意通风。
④运输要求:轻拿轻放、勿撞击。
⑤工作人员要求:严禁烟火、人走电断。
火灾自救及逃生策略:
(1)可燃性气体泄漏时的注意事项当室内天然气、液化石油气、煤气泄漏后室内充满可燃性气体.在此环境中打电话或打开换气扇开关,可能产生电火花,造成爆炸、所以应先关闭总阀、开窗通风,并在杜绝一切明火的同时,查找泄露的原因。
(2)火灾自救策略
①迅速找到安全通道;
②火灾时上层空气中氧气少,毒气浓度大,所以要匍匐前进:
③房间发生火灾时不能随时开门开窗,开门开窗会增加氧气量,使火势更加凶猛;
④火灾时,会产生大量浓烟,使人窒息,因此最好用湿布捂住口鼻;
⑤在山林中遇到火灾时,应逆风而跑,因为顺着风更容易被烧伤或发生危险。
爆炸极限:
(1)概念:可燃性气体在空气中达到一定浓度时,遇到明火会发生爆炸,人们把容易导致爆炸的空气中可燃性气体的体积分数范围,称为该气体的爆炸极限。
①当可燃性气体在混合气体中的含量高于爆炸极限的上限时,可燃性气体可以安静地燃烧;而低于爆炸极限的下限时,则无法燃烧。
②我们通常所说额可燃性气体检验纯度,其实就是检验可燃性气体有没有达到爆炸极限,只要超过爆炸极限的上限,可燃性气体就可以安静的燃烧。
(2)几种常见物质的爆炸极限
| 可燃物 | 爆炸极限 |
| 甲烷 | 5%-15% |
| 丙烷 | 2.2%-9.5% |
| 乙醇 | 3.4%-19% |
| 氢气 | 4.0%-75% |
| 一氧化碳 | 12.5%-74% |
| 液化气 | 2.0%-12% |
| 水煤气 | 7.0%-72% |
粉尘爆炸实验:
(1)实验装置及步骤
下面是模拟粉尘爆炸的一个实验:如下图所示,在无盖小塑料筒里放入干燥面粉,点燃蜡烛,用塑料盖盖住金属筒,迅速鼓入大量空气,不久,便会听到“砰”的一声,爆炸的气浪将金属筒的塑料盖掀起。
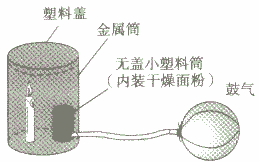
(2)现象:砰的一声响,伴随着一团火光产生,放热,塑料盖被掀起。
(3)分析:面粉被吹起,与空气充分接触,又被蜡烛点燃,在有限空间内发生急剧地燃烧,并让出大量热,产生的气浪将塑料盖掀起,说明可燃物的粉尘在有限的空间内急剧燃烧,能发生爆炸。
金属的化学性质:
常见金属能与氧气反应,也能与盐酸,硫酸及盐溶液反应。
常见金属的化学性质:
1.金属和氧气的反应
2.金属与酸的反应
3.金属与盐的反应
将锌片、铁丝、铜丝三种金属分别放入硫酸铜溶液、硝酸银溶液、氯化钠溶液中,观察现象
易错点:
一、(1)一般在金属活动性顺序表中排在氢前面的金属(也叫活泼金属)能置换出酸中的氢;排在氢后面的金属则不能,如铜、银与盐酸、稀硫酸都不反应。
(2)浓硫酸和硝酸与金属反应不生成氢气,因为它们有很强的氧化性,与金属反应不生成氢气。
(3)在金属活动性顺序表中排在最前面的金属如K、 Na活泼性太强,放入酸溶液中首先跟酸发生置换反应,过M的金属会继续跟水发生剧烈的反应。
(4)铁与非氧化性酸反应时,始终生成亚铁盐 (Fe2+)。
(5)金属与酸反应后溶液的质量增大。
二、
(1)在金属活动性顺序表中,位于前面的金属可以把位于其后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。相隔越远,反应越容易发生。
(2)金属与盐溶液的反应,盐必须能溶于水,不溶性的盐与金属不反应,如AgCl难溶于水,Fe和AgCl不反应。
(3)不能用活泼的金属K,Ca,Na,与盐溶液反应,因为K,Ca,Na。会先与H2O发生置换反应生成碱和氢气。
金属与酸的反应不一定属于置换反应:
置换反应是指一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。一般情况下,较活泼的金属跟酸发生的化学反应属于置换反应。但由于浓硫酸(或硝酸)具有强氧化性,金属与浓硫酸(或硝酸)反应时,生成物相对比较复杂。这类反应不属于置换反应。
铝和锌的抗腐蚀性:
1.铝制品具有很好的抗腐蚀性,是因为铝与空气中的氧气反应表面生成一种致密的氧化铝薄膜,对铝起防护作用。
2.锌与铝的抗腐蚀性相似,也是在金属表面会生成一层致密的氧化锌保护膜。
常见金属能与氧气反应,也能与盐酸,硫酸及盐溶液反应。
常见金属的化学性质:
1.金属和氧气的反应
| 金属 | 在空气中 | 在氧气中 | 方程式 |
| 镁 | 常温下表面逐渐变暗。点燃 剧烈燃烧,发出耀眼的白光, 生成白色固体 |
点燃,剧烈燃烧,发出耀 眼的白光,生成白色固体 |
2Mg+O2 2MgO 2MgO |
| 铝 | 常温下,铝表而变暗,生成一 层致密氧化膜,保护铝不再被腐蚀 |
点燃。剧烈燃烧,火星四射, 放出大量的热,生成白色固体 |
4Al+3O2 2Al2O3 2Al2O3 |
| 铁 | 持续加热发红,离火变冷 | 火星四射,放出大量的热, 生成黑色固体 |
3Fe+2O2 Fe3O4 Fe3O4 |
| 铜 | 加热,生成黑色物质,在潮湿的 空气中,生成铜绿而被腐蚀 |
加热,生成黑色固体 | 2Cu+O2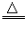 2CuO 2CuO |
| 金 | 即使在高温也不和氧气反应 | —— | |
| 结论 | 大多数金属都能喝氧气反应,但反应的难易程度和剧烈程度不同 | ||
2.金属与酸的反应
| 盐酸 | 稀硫酸 | 反应现象(两种酸中相同) | |
| 镁 | Mg+2HCl==MgCl2+H2↑ | Mg+H2SO4==MgSO4+H2↑ | 反应比较剧烈,产生大量 气泡,溶液仍为无色,生成 的气体能够燃烧,并且产 生淡蓝色火焰 |
| 铝 | 2Al+6HCl==2AlCl3+3H2↑ | 2Al+3H2SO4==Al2(SO4)+3H2↑ | |
| 锌 | Zn+2HCl==H2↑+ZnCl2 | Zn+H2SO4==ZnSO4+H2↑ | 反应缓慢,有气泡产生,溶 液由无色逐渐变为浅绿色, 生成的气体能够燃烧,并且 产生淡蓝色火焰 |
| 铁 | Fe+2HCl==FeCl2+H2↑ | Fe+H2SO4==FeSO4+H2↑ | |
| 铜 | 不反应 | 不反应 | 无 |
3.金属与盐的反应
将锌片、铁丝、铜丝三种金属分别放入硫酸铜溶液、硝酸银溶液、氯化钠溶液中,观察现象
| CuSO4溶液 | AgNO3溶液 | NaCl溶液 | |
| 锌 | 锌表面有一层红色金属析出,溶液由蓝色变为无色 Zn+CuSO4==ZnSO4+Cu |
锌表面有一层银白色金属析出 Zn+2AgNO3==Zn(NO3)2+2Ag |
无变化,不反应 |
| 铁 | 铁表面有一层红色金属析出,溶液由蓝色变为浅绿色 Fe+CuSO4==FeSO4+Cu |
铁表面有一层银白色金属析出,溶液由无色变为浅绿色 Fe+2AgNO3==Fe(NO3)2+2Ag |
无变化,不反应 |
| 铜 | 无变化,不反应 | 铜表面有一层银白色金属析出,溶液由无色变为蓝色 Cu+2AgNO3==Cu(NO3)2+2Ag |
无变化,不反应 |
易错点:
一、(1)一般在金属活动性顺序表中排在氢前面的金属(也叫活泼金属)能置换出酸中的氢;排在氢后面的金属则不能,如铜、银与盐酸、稀硫酸都不反应。
(2)浓硫酸和硝酸与金属反应不生成氢气,因为它们有很强的氧化性,与金属反应不生成氢气。
(3)在金属活动性顺序表中排在最前面的金属如K、 Na活泼性太强,放入酸溶液中首先跟酸发生置换反应,过M的金属会继续跟水发生剧烈的反应。
(4)铁与非氧化性酸反应时,始终生成亚铁盐 (Fe2+)。
(5)金属与酸反应后溶液的质量增大。
二、
(1)在金属活动性顺序表中,位于前面的金属可以把位于其后面的金属从它们的盐溶液中置换出来(K,Ca,Na除外)。相隔越远,反应越容易发生。
(2)金属与盐溶液的反应,盐必须能溶于水,不溶性的盐与金属不反应,如AgCl难溶于水,Fe和AgCl不反应。
(3)不能用活泼的金属K,Ca,Na,与盐溶液反应,因为K,Ca,Na。会先与H2O发生置换反应生成碱和氢气。
金属与酸的反应不一定属于置换反应:
置换反应是指一种单质和一种化合物反应生成另一种单质和另一种化合物的反应。一般情况下,较活泼的金属跟酸发生的化学反应属于置换反应。但由于浓硫酸(或硝酸)具有强氧化性,金属与浓硫酸(或硝酸)反应时,生成物相对比较复杂。这类反应不属于置换反应。
铝和锌的抗腐蚀性:
1.铝制品具有很好的抗腐蚀性,是因为铝与空气中的氧气反应表面生成一种致密的氧化铝薄膜,对铝起防护作用。
2.锌与铝的抗腐蚀性相似,也是在金属表面会生成一层致密的氧化锌保护膜。
一氧化碳的毒性:
一氧化碳进入人体之后会和血液中的血红蛋白结合,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。因此一氧化碳具有毒性。一氧化碳是无色、无臭、无味的气体,故易于忽略而致中毒。常见于家庭居室通风差的情况下,煤炉产生的煤气或液化气管道漏气或工业生产煤气以及矿井中的一氧化碳吸入而致中毒。
一氧化碳的解毒:
轻微中毒者,应吸入大量新鲜空气或进行人工呼吸。医疗上常用静脉注射亚甲基蓝进行解毒。
一氧化碳进入人体之后会和血液中的血红蛋白结合,进而使血红蛋白不能与氧气结合,从而引起机体组织出现缺氧,导致人体窒息死亡。因此一氧化碳具有毒性。一氧化碳是无色、无臭、无味的气体,故易于忽略而致中毒。常见于家庭居室通风差的情况下,煤炉产生的煤气或液化气管道漏气或工业生产煤气以及矿井中的一氧化碳吸入而致中毒。
一氧化碳的解毒:
轻微中毒者,应吸入大量新鲜空气或进行人工呼吸。医疗上常用静脉注射亚甲基蓝进行解毒。
发现相似题
与“下列做法或报道有科学依据的是( )A.高828米的迪拜塔使用大...”考查相似的试题有:
- 下图中的甲~丁是初中化学常见的四种不同类别的物质,相邻两种物质可发生反应生成A~D四种物质(部分生成物已略去)。其中乙是...
- 下列鉴定物质的方法错误的是( ) 待鉴别物质鉴别方法A硬水、软水加肥皂水,搅拌,观察产生泡沫的多少B氧气、空气用带火星的...
- 下列图标中,属于消防安全标志的是A. B. C. D.
- 豆浆机由于快捷方便而进入了千家万户.请根据如图所示回答相关问题:(1)豆浆机的制作材料中属于金属材料的是______(填图中...
- 表中列出几种金属的熔点,据此判断以下说法不正确的是( )物质名称汞金铜铁钨武德合金熔点/℃-38.8106410831535341070A.“真...
- 下边五环图中的每个环代表初中化学中常见的一种物质,两环相交表示两者之间能相互反应.下列符合题意的是( )A.(1)Fe,(...
- 下列描述中,属于金属化学性质的是[ ]A.铜是紫红色固体B.汞在常温下呈液态C.铝能与酸反应D.钠的质地较软
- 选用铜、银、金作为钱币,从化学角度看,主要是由于它们[ ]A.硬度适当B.化学性质不活泼C.密度适当D.相应元素在地壳里的含...
- 冬天使用燃气热水器时,造成煤气中毒的气体是( )A.CH4B.CO2C.COD.SO2
- 下列对化学知识的归纳中不正确的是( )A.化学巨匠及贡献张青莲-测量相对原子质量拉瓦锡-研究了空气的成分B.生产生活中安全...