本试题 “氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答下列问题:Ⅰ.把氯气通入紫色石蕊溶液中,可以观察到的现象是:______...” 主要考查您对氯气
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氯气
氯气:
①化学式:Cl2
②氯元素在周期表中的位置:第三周期ⅦA族
③氯原子的电子式: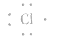
④氯的原子结构示意图: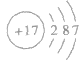
⑤氯原子的外围电子排布式:
⑥化学键类型:非极性共价键
⑦氯分子的电子式:
⑧氯分子的结构式:
氯气的物理性质和化学性质:
(1)物理性质:黄绿色,有刺激性气味,有毒,密度比空气大,能溶于水(1:2)。
(2)化学性质:氯气(Cl2)是双原子分子,原子的最外层有七个电子,是典型的非金属元素,单质是强氧化剂。
①氯气与金属反应: 2Na+Cl2
 2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2
2NaCl(反应剧烈,产生大量白烟) 2Fe+3Cl2 2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2
2FeCl3(反应剧烈,产生大量棕褐色烟,溶于水成黄色溶液) Cu+Cl2 CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。
CuCl2(反应剧烈,产生大量棕色的烟,溶于水成蓝色或绿色溶液)氯气能与绝大数金属都能发生反应,表明氯气是一种活泼的非金属单质。 ②与非金属的反应 H2+Cl2
 2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2
2HCl(纯净的氢气在氯气中安静的燃烧,芒白色火焰,在瓶口处有白雾产生)H2+Cl2 2HCl(发生爆炸) 2P+3Cl2
2HCl(发生爆炸) 2P+3Cl2 2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。
2PCl3(液态) PCl3+Cl2==PCl5(固态)磷在氯气中剧烈燃烧,产生大量的烟、雾。雾是PCl3,烟是PCl5。氯气能有很多非金属单质反应,如S、C、Si等。 ③与碱反应 Cl2+2NaOH==NaCl+NaClO+H2O 2Cl2+2Ca(OH)2==CaCl2+Ca(ClO)2+2H2O
④与某些还原性物质反应:Cl2+2FeCl2===2FeCl3 Cl2+SO2+2H2O==2HCl+H2SO4
⑤有机反应(参与有机反应的取代和加成反应)
CH4+Cl2→CH3Cl+HCl
CH3Cl+Cl2→CH2Cl2+HCl
CH2Cl2+Cl2→CHCl3+HCl
CHCl3+Cl2→CCl4+HCl
Cl2+CH2=CH2→CH2Cl-CH2Cl(加成反应)
⑥与水反应 Cl2+H2O
 HCl+HClO
HCl+HClO 发现相似题
与“氯气是一种重要的化工原料,在工农业生产、生活中有着重要的...”考查相似的试题有:
- 下列物质能使干燥的蓝色石蕊试纸先变红后退色的是( )①氯气 ②液氯 ③新制氯水 ④敞口放置的久置氯水 ⑤盐酸 ⑥用盐酸酸化的漂白...
- 放在敞口容器中的下列溶液,久置后溶液中溶质的浓度会变大的是()A.浓硫酸B.氢氧化钠C.浓盐酸D.氯化钠
- 氯是富集在海水中的元素。下列有关氯气的说法不正确的是[ ]A.氯气是无色无味的气体B.氯气有毒C.氯气可用于自来水的消毒D....
- 下列气体中,无色无味无毒的是[ ]A.SO2B.CH4C.NOD.Cl2
- 某混合气体G可能含有CO、CO2、SO2、H2O等气体,用a.无水CuSO4,b.澄清石灰水,c.灼热CuO,d.碱石灰,e.酸性品红溶液,f.酸性...
- 下列关于氯气的说法错误的是A.有刺激性气味B.有毒C.密度比空气大 D.红棕色
- 下列物质间发生化学反应时,在不同情况下生成物都相同的是( )A.Na与O2B.P和Cl2C.Cu和HNO3D.H2和O2
- 多数自来水是采用氯气消毒的,为检验自来水中Cl–的存在,最好选用下列物质中的 ( )A.石蕊试液B.四氯化碳C.氢氧化钠溶液D....
- 下列溶液中不存在氯离子的是A.氯水B.氯化氢溶液C.漂白粉溶液D.氯酸钾溶液
- 氯气是一种化学性质很活泼的非金属单质,它具有较强的氧化性,下列叙述中不正确的是A.灼热的铜丝在Cl2中剧烈地燃烧,产生棕...