本试题 “科学家预测,氨有望取代氢能,成为重要的新一代绿色能源。下列有关说法不正确的是[ ]A.液氨作为清洁能源的反应原理是4NH3+5O24NO+6H2OB.液氨具有腐蚀性和毒...” 主要考查您对氨气
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氨气
氨:
NH3的电子式为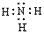 ,结构式为
,结构式为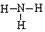 ,氨分子的结构为三角锥形,N原子位于锥顶,三个H原子位于锥底,键角107°18′,是极性分子。 分子结构为:
,氨分子的结构为三角锥形,N原子位于锥顶,三个H原子位于锥底,键角107°18′,是极性分子。 分子结构为: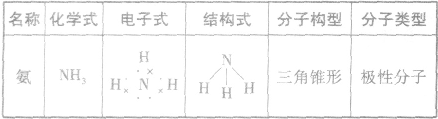
氨的物理性质和化学性质:
1.物理性质:
氨是无色、有刺激性气味的气体,比空气轻;氨易液化,在常压下冷却或常温下加压,气态氨转化为无色的液态氨,同时放出大量热。液态氨气化时要吸收大量的热,使周围的温度急剧下降;氨气极易溶于水,在常温、常压下,1体积水中能溶解约700体积的氨气(因此,氨气可进行喷泉实验);氨对人的眼、鼻、喉等粘膜有刺激作用,若不慎接触过多的氨而出现病症,要及时吸入新鲜空气和水蒸气,并用大量水冲洗眼睛。
2.化学性质:
(1)与水反应, ,氨的水溶液叫做氨水。在氨水中所含的微粒有:
,氨的水溶液叫做氨水。在氨水中所含的微粒有:
 氨水具有碱的通性,如能使无色酚酞溶液变红。
氨水具有碱的通性,如能使无色酚酞溶液变红。
(2)与酸反应生成铵盐反应实质为:
反应原理拓展NH3分子中N原子有一对孤电子,能够跟有空轨道的H+形成配位键: 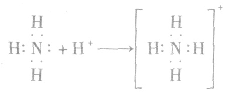
(3)具有还原性  (工业制HNO3的基础反应)
(工业制HNO3的基础反应) (Cl2过量)
(Cl2过量) (NH3过量,可用于检验Cl2瓶是否漏气)
(NH3过量,可用于检验Cl2瓶是否漏气)  (实验室制N2)
(实验室制N2)
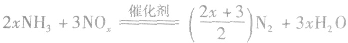 (治理氮氧化物污染)
(治理氮氧化物污染)
(4)与CO2反应制尿素 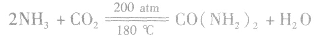
(5)配合反应
 的比较:
的比较:
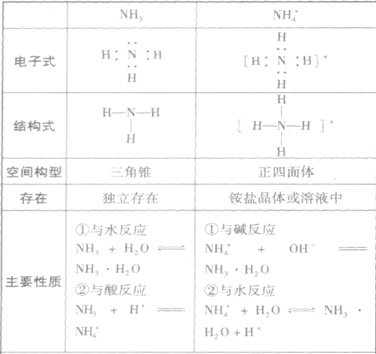
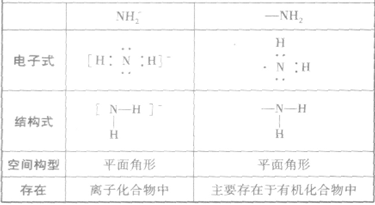
氨的结构与性质的关系总结:

氨的用途:
(1)氨是氮肥工业及制造硝酸、铵盐、纯碱等的重要原料。
(2)氨也是有机合成工业(如制尿素、合成纤维、染料等)上的常用原料。
(3)氨还可用作制冷剂。
对实验室制氨气常见问题的解释:
l.制取氨气时为什么用的铵盐一般是氯化铵而不是硝铵、硫铵或碳铵实验室制氨气用 固体混合反应,加热时反应速率显著增大。因为
固体混合反应,加热时反应速率显著增大。因为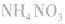 在加热时可能发生爆炸性的分解反应:
在加热时可能发生爆炸性的分解反应: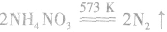
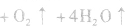 ,若用硝铵代替,在制氨气过程中可能会发生危险;因为碳铵受热极易分解出CO2:,使生成的NH3中混有较多CO2杂质,故不用碳铵;若用硫铵,由于反应时生成
,若用硝铵代替,在制氨气过程中可能会发生危险;因为碳铵受热极易分解出CO2:,使生成的NH3中混有较多CO2杂质,故不用碳铵;若用硫铵,由于反应时生成 ,易使反应混合物结块,产生的氨气不易逸出。故制NH3时选用
,易使反应混合物结块,产生的氨气不易逸出。故制NH3时选用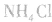 。
。
2.不用铵盐与强碱反应能否制取氨气能。
①加热浓度在20%以上的浓氨水,若浓度不够可加人适量固体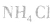 和生石灰(CaO)或烧碱:
和生石灰(CaO)或烧碱: 
②将浓氨水滴入盛有固体烧碱或生石灰(CaO)的烧瓶中,使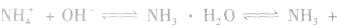
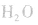 平衡右移,放出
平衡右移,放出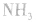 ,且NaOH、CaO溶于水均放热,可降低
,且NaOH、CaO溶于水均放热,可降低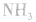 ,在水中的溶解度。
,在水中的溶解度。
③将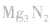 溶于水或使尿素在碱性条件下水解。
溶于水或使尿素在碱性条件下水解。 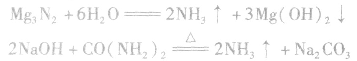
3.为什么制NH3用Ca(OH)2而不用NaOH ①固体NaOH易吸湿结块,不易与铵盐混合充分而反应;②在加热条件下,NaOH易腐蚀玻璃仪器。
4.制NH3的装置有哪些注意事项
①收集装置和发生装置的试管和导管必须是干燥的,因为氨气易溶于水;
②发生装置的试管口略向下倾斜,以免生成的水倒流使试管炸裂;
③导管应插入收集装置的底部,以排尽装置中的空气;
④收集NH3的试管口塞一团棉花,作用是防止NH3与空气形成对流,使收集的NH3较纯,还可防止NH3逸散到空气中。
5.用什么方法收集NH3只能用向下排空气法,因为NH3极易溶于水,密度又比空气小。
6.怎样收集干燥的NH3将NH3通过盛有碱石灰或固体NaOH的干燥管,但不能选用浓 、无水
、无水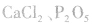 等作干燥剂,因为它们均能与NH3发生反应。
等作干燥剂,因为它们均能与NH3发生反应。
7.怎样检验NH3已充满试管把湿润的红色石蕊试纸放在试管口处,若试纸变蓝,则NH3已充满;把蘸有浓盐酸的玻璃棒接近试管口,若产生大量白烟,则NH3已充满。
与“科学家预测,氨有望取代氢能,成为重要的新一代绿色能源。下...”考查相似的试题有:
- 下列工业生产的反应原理错误的是( )A.高炉炼铁:Fe2O3+3CO高温2Fe+3CO2B.氨的氧化:4NH3+5O2催化剂△4NO+6H2OC.煅烧硫铁...
- A、B、C、D为中学化学中常见的四种气体单质,在一定条件下,B可以分别和A、C、D化合生成甲、乙、丙,C和D化合生成化合物丁。...
- 下列反应说明氨气既有还原性,又有碱性的是[ ]A.4NH3+5O2=4NO+6H2OB.3Cl2+8NH3=N2+6NH4ClC.3CuO+2NH3=3Cu+ N2+3H2OD.NH3+...
- 已知A、B、C是中学化学的常见物质,它们在一定条件下有如下转化关系:⑴若A能使湿润的红色石蕊试纸变蓝;C为红棕色气体。则A转...
- 下列描述不正确的是( )A.二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生产硝酸B.液氨汽化时要吸收大量的热,...
- 某化学兴趣小组欲制取氨气和氯化氢气体并完成喷泉实验(图中夹持装置均已略去)。(1)写出实验室制取氨气的化学方程式:____...
- 现有下列四种物质:① SO2②NH3③Na2SO4溶液 ④Fe(OH)3胶体。其中加入氯化钡溶液产生白色沉淀的是______(填序号,下同),能使品...
- 有A、B、C三种气体,A气体在一定条件下能与O2反应生成B;B不溶于水,但易与O2反应生成C;A、C气体皆易溶于水,所得的溶液可以...
- 氢、氮、氧三种元素可以分别两两组成如氮氧化物、氮氢化物和氢氧化物等,科学家们已经研究和利用其特殊性质开发其特有的功能...
- 下列反应中,相关示意图象错误的是( )ABCD将二氧化硫通入到一定量氯水中将氨水滴入到一定量氯化铝溶液中常温下将铜粉加入到...