本试题 “不定项选择下列四幅图涉及到不同的物理知识,其中说法正确的是( )A.图甲:普朗克通过研究黑体辐射提出能量子的概念,成为量子力学的奠基人之一B.图乙:玻...” 主要考查您对光的衍射
能量量子化
原子的核式结构模型:α粒子散射实验
玻尔的原子理论
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 光的衍射
- 能量量子化
- 原子的核式结构模型:α粒子散射实验
- 玻尔的原子理论
光的衍射:
1.定义:当光照射到小孔或障碍物上时,光离开直线路径绕到孔或障碍物的阴影里去的现象,叫做光的衍射现象
2.明显衍射条件:障碍物或小孔的尺寸跟光的波长相差不多.甚至比光的波长还要小
3.形成原因:光的衍射是相干光波叠加的结果,当光源发出的光照射到小孔或障碍物上时,小孔处可以看成许多点光源,障碍物的边缘也可看成许多点光源(惠更斯原理)。这些点光源是相干光源,发出的光相干涉,在光屏上形成明暗相间的条纹
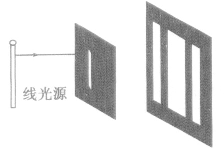
衍射图样及条纹特征:
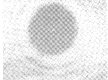
| 单缝衍射 | 圆孔衍射 | 圆板衍射 |
 |
 |
 |
| ①单缝衍射条纹的分布是不均匀的,中央亮条纹与邻边的亮条纹相比有明显的不同。用单色光照射单缝时,光屏上出现亮、暗相间的衍射条纹,中央亮条纹最宽最亮。用白光照射单缝时,中间是白色亮条纹,两边是彩色条纹,其中最靠近中间的色光是紫光,最远离中间的色光是红光。 ②中央亮条纹的宽度及条纹间距跟入射光的波长及单缝宽度有关,入射光波长越大,单缝越窄,中央亮条纹的宽度及条纹间距就越大。 ③缝变窄,通过的光能变少,而光能分布的范围变宽,所以亮纹的亮度降低 |
①衍射图样中,中央亮圆的亮度最大,外面是亮、暗相间的圆环,但外围亮环的亮度小,用不同的光照射时得到的图样也不一样,如果用单色光照射时,中间为亮圆,外面是亮度越来越暗的亮环。如果用白光照射时,中间亮圆为白色,周围是彩色圆环。 ②中央是大且亮度最大的圆形亮斑,周围分布着明暗相间的同心圆环,且越靠外,圆形亮条纹的亮度越弱,宽度越小。 ③只有圆孔足够小时,才能得到明显的衍射图样。在圆孔由较大直径逐渐减小的过程中,光屏依次得到几种不同的现象——圆形亮斑(光的直线传播)、光源的像(小孔成像)、明暗相间的圆环(衍射图样)、完全黑暗。 ④用不同色光照射圆孔时,得到的衍射图样的大小和位置不同,波长越大,中央圆形亮斑的直径越大。 ⑤白光的圆孔衍射图样中,中央是大且亮的白色光斑,周围是彩色同心圆环。 ⑥圆孔越小,中央亮斑的直径越大,同时亮度越弱 |
①圆板阴影区的中央有个亮斑——泊松亮斑。 ②圆板阴影区的周围有明暗相问的圆形衍射条纹 ③亮环或暗环的间距随半径的增大而减小,即越向外条纹越窄 |
光的干涉和衍射的比较:

能量量子化:
1、黑体辐射:固体或液体,在任何温度下都在发射各种波长的电磁波,这种由于物体中的分子、原子受到激发而发射电磁波的现象称为热辐射。
2、黑体能全部吸收各种波长的电磁波而不发生反射的物体,称为绝对黑体,简称黑体。
3、黑体辐射实验:黑体热辐射的强度与波长的关系:随着温度的升高,一方面,各种波长的辐射强度都有增加,另一方面,辐射强度的极大值向波长较短的方向移动。
4、能量子:1900年,德国物理学家普朗克提出能量量子化假说:辐射黑体分子、原子的振动可看作谐振子,这些谐振子可以发射和吸收辐射能。但是这些谐振子只能处于某些分立的状态,在这些状态中,谐振子的能量并不象经典物理学所允许的可具有任意值。相应的能量是某一最小能量ε(称为能量子)的整数倍,即:ε,1ε,2ε,3ε,... nε,n为正整数,称为量子数。
对于频率为υ的谐振子最小能量为ε=hυ,这个最小能量值,就叫做能量子。
1、黑体辐射:固体或液体,在任何温度下都在发射各种波长的电磁波,这种由于物体中的分子、原子受到激发而发射电磁波的现象称为热辐射。
2、黑体能全部吸收各种波长的电磁波而不发生反射的物体,称为绝对黑体,简称黑体。
3、黑体辐射实验:黑体热辐射的强度与波长的关系:随着温度的升高,一方面,各种波长的辐射强度都有增加,另一方面,辐射强度的极大值向波长较短的方向移动。
4、能量子:1900年,德国物理学家普朗克提出能量量子化假说:辐射黑体分子、原子的振动可看作谐振子,这些谐振子可以发射和吸收辐射能。但是这些谐振子只能处于某些分立的状态,在这些状态中,谐振子的能量并不象经典物理学所允许的可具有任意值。相应的能量是某一最小能量ε(称为能量子)的整数倍,即:ε,1ε,2ε,3ε,... nε,n为正整数,称为量子数。
对于频率为υ的谐振子最小能量为ε=hυ,这个最小能量值,就叫做能量子。
α粒子散射实验:
是用α粒子轰击金箔,结果是绝大多数α粒子穿过金箔后基本上仍沿原来的方向前进,但是有少数α粒子发生了较大的偏转。这说明原子的正电荷和质量一定集中在一个很小的核上。
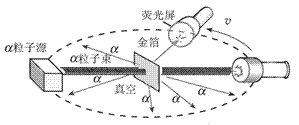
是用α粒子轰击金箔,结果是绝大多数α粒子穿过金箔后基本上仍沿原来的方向前进,但是有少数α粒子发生了较大的偏转。这说明原子的正电荷和质量一定集中在一个很小的核上。

汤姆孙的原子结构模型:
| 模型理论 | 原子是一个球体,正电荷均匀分布在整个球内,而电子像枣糕里的枣儿那样镶嵌在原子里,电子的总电荷量和正电荷的电荷量相等 |
| 模型比例 | 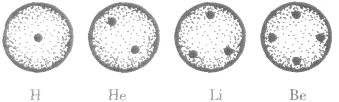 |
| 模型的应用 |
原子呈现电中性的原因是原子内正电荷与电子的总电荷数值相等;原子能够发光的原因是电子在原子内振动;不同原子发光频率不同的原因是不同原子内电子的振动频率不同等 |
| 模型的否定 | 不能解释α粒子散射现象被否定 |
玻尔的原子理论:
| 经典理论的困难 | 原子的稳定性 | 电子做加速运动应该辐射电磁波,逐渐减小能量和轨道半径,最终落入原子核,原子是不稳定的,与事实不符 |
| 原子光谱的分立性 | 电子绕核运行辐射频率应等于电子绕核运行频率,由于运行轨道的减小,辐射电磁波频率应不断变化而形成连续光谱,这与原子光谱一明线光谱不符(固定的若干种频率) | |
| 玻尔理论基础 | 实验基础 | 氢原子光谱的分立特征 |
| 理论基础 | 普朗克关于黑体辐射的量子论与爱因斯坦的光子说 | |
| 波尔理论内容 | 量子化假设 | ①电子的轨道是量子化的。电子运行轨道的半径不是任意的,只有半径的大小符合一定条件的轨道才是可能的。电子在这些轨道上绕核的转动是稳定的,不产生电磁辐射 ②原子的能量是量子化的。这些量子化的能量值叫做能级。原子中这些具有确定能量的稳定状态称为定态。能量最低的状态叫做基态,其他的状态叫做激发态 |
| 频率条件 | 当电子从能量较高的定态轨道(Em)跃迁到能量较低的定态轨道(En)时,会放出能量为hv的光子,这个光子的能量由前后两个能级的能量差决定,即hv=Em一En | |
| 对光谱的解释 | 原子光谱的分立性 | 通常情况下,原子处于基态,基态是稳定的,处于激发态的原子是不稳定的。原子从高能态向低能态跃迁时放出的光子的能量等于前后两个能级之差。由于原子的能级是分立的,所以放出的光子的能量也是分立的。因此原子的发射光谱只有一些分立的亮线 |
| 特征谱线 | 由于不同的原子具有不同的结构,能级各不相同,因此辐射(或吸收)的光子频率也不同,这就是不同元素的原子具有不同的特征谱线的原因 | |
| 氢原子光谱线系 | 玻尔理论不但成功地解释了氢光谱的巴耳末系,而且对当时已发现的氢光谱的另一线系——帕邢系(在近红外区)也能很好地解释。它是电子从n=4、5、6等能级向n=3 能级跃迁时辐射出来的。此外,玻尔理论还预言了当时尚未发现的氢原子的其他光谱线系,这些线系后来相继被发现,也都跟玻尔理论的预言相符 |
玻尔的原子理论的成功与局限:
玻尔的原子理论第一次将量子观引入原子领域,提出定态和跃迁的概念,成功地解释了氢原子光谱规律,但玻尔引入的量子化观点并不完善。在量子力学中,核外电子并没有确定的轨道,玻尔的电子轨道只不过是电子出现概率较大的地方。把电子的概率分布用图像表示时,用小黑点的稠密程度代表概率的大小,其结果如同电子在原子核周围形成的云雾,称为“电子云
发现相似题
与“不定项选择下列四幅图涉及到不同的物理知识,其中说法正确的...”考查相似的试题有:
- 利用如图所示装置,可以在光屏上观察到明暗相间的条纹,这是光的______现象,若保持单缝到光屏的距离不变,调节狭缝的缝宽,...
- 有以下说法,其中正确的是( )A.在“探究单摆的周期与摆长的关系”实验中,为减小偶然误差,应测出单摆作n次全振动的时间t,...
- 下列说法中正确的是[ ]A.光传播时,若遇到的障碍物的尺寸比光的波长大很多,衍射现象十分明显,此时不能认为光沿直线传播B....
- 日出和日落时,太阳看起来特别红,关于其原因的说法正确的是 ( )A.红光沿直线传播B.红光的波长最长C.空气分子对红光散射得最...
- 不定项选择关于下列四幅图中所涉及物理知识的论述中,正确的是( )A.甲图中的海市蜃楼是光的色散现象引起的B.乙图中的泊松...
- 在α粒子散射实验中,当α粒子穿过金箔时,下列理解正确的是[ ]A.与金原子核相距较远的α粒子,可能发生大角度偏转B.与金原子...
- 汤姆生通过研究阴极射线发现了电子,并提出了枣糕模型,为证实枣糕模型是否正确,卢瑟福做了用α粒子打击金箔的实验,下图是在...
- 下列说法中正确的是( )A.α、β、γ三种射线,照射到锌板上都会使之带电B.在地球大气层外观察到的太阳光谱是连续谱C.查德威克...
- 下列说法中正确的是( ) A.氢原子由较高能级跃迁到较低能级时,能量减小 B.氢原子从n=3的激发态跃迁到基态时,有可能辐射...
- 氢原子处于基态时,原子的能量为,问:(1)氢原子在n =4的定态时,可放出几种频率的光?其中最小频率等于多少Hz?(2)若要...