本试题 “某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.所用试剂:样品、pH试纸...” 主要考查您对测定物质组成、成分含量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 测定物质组成、成分含量
定量实验介绍:

燃烧法测定氨基酸的组成:
实验室用燃烧法测定某种氨基酸(CxHyOzNp)的分子组成。取Wg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2。现按下图所示装置进行实验。

①实验开始时,首先要通入一段时间的氧气,目的是排除体系中的N2。
②D装置的作用是吸收未反应的O2,保证最终收集的气体是N2。
③读取N2体积时,应注意:量筒内液面与广口瓶中的液面相持平视线与凹液面最低处相切。
④实验中测得N2的体积为VmL(已折算为标准状况)。为确定此氨基酸的分子式,还需要的有关数据为生成二氧化碳气体的质量、生成水的质量、氨基酸的相对分子质量
用氨气还原氧化铜的方法测定铜的近似相对原子质量:
实验室用氨气还原氧化铜的方法测定铜的近似相对原子质量,反应的化学方程式为:2NH3+3CuO
 N2+3Cu+3H2O
N2+3Cu+3H2O(1)如果选用测定反应物CuO和生成物H2O的质量[m(CuO)、m(H2O)]时,请用下列仪器设计一个简单的实验方案。
装置图:
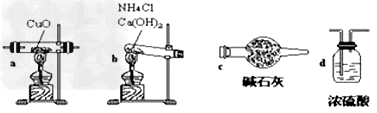
①连接顺序为:bcacd
②d中浓硫酸的作用是吸收未反应的氨、防止空气中水分进入;实验完毕时观察到a中的现象是固体由黑色转变为红色;
③Cu的相对原子质量的表达式
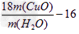
发现相似题
与“某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量...”考查相似的试题有:
- 用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2·xH2O)。有如下操作已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+...
- 某白色粉末可能含有氯化钙、硫酸钠、硝酸钡、碳酸钾中的一种或几种.把该粉末放入足量的水中,充分搅拌,仍然有白色物质不能...
- 铁在冷的浓硫酸中能发生钝化.某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体.请你协...
- 铝粉是铝热剂的主要成分之一, 常用铝锭制得的铝粉中含有少量的Al2O3和SiO2,用如图所示的装置(甲、乙管用橡皮管连接可上下...
- 某小组同学将一定浓度Na2CO3溶液滴入CuSO4溶液中发现生成了蓝色沉淀.甲同学认为沉淀是CuCO3;乙同学认为沉淀是CuCO3和Cu(OH...
- 硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化...
- 测定硫酸铜晶体(CuSO4·5H2O)里结晶水的含量,实验步骤为:①研磨②称量空坩埚和装有试样的坩埚的质量③加热④冷却⑤称量⑥重复③至...
- 下表是一组各10.0克,不纯的碳酸盐(M2CO3)的样品,与足量稀盐酸反应产生二氧化碳气体的体积(已换算成标准状况下的体积)和...
- 铝镁合金现已成为轮船制造、化工生产等行业的重要原料.现有一块铝镁合金,欲测定其中镁的质量分数,几位同学分别称取3.9克样...
- 三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探...