本试题 “碳和碳的化合物广泛的存在于我们的生活中。(1)根据下列反应的能量变化示意图,2C(s)+O2(g) =2CO(g) △H= 。(2)在体积为2L的密闭容器中,充人1 mol CO2和3m...” 主要考查您对化学反应速率的定义、公式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应速率的定义、公式
化学反应速率:
1.定义:化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
2.表示方法:在容积不变的反应器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。即: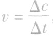
3.单位:mol·L-1·s-1或mol·L-1·min-1等。
4.注意:
(1)化学反应速率是指一段时间内的平均速率,而不是瞬时速率;通常前一段时间的平均反应速率要快于后一段时间的平均反应速率,反应速率均取正值,即v>0。
(2)在一定温度下,固体和纯液体物质单位体积的物质的量保持不变,即物质的量浓度为常数,因此在表示化学反应速率时,不代入固体或纯液体物质的浓度。浓度是指气体或溶液的浓度。
(3)同一个化学反应在相同的条件下、在同一段时间内,用不同物质表示反应速率时,数值可能相同也可能不同,但表达的意义都相同,即反应的快慢程度是一样的。
(4)在同一反应巾用不同的物质来表示反应速率时,其数值之比等于化学方程式中各物质的化学计量数之比.
如化学反应: ,
,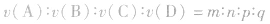 ,所以
,所以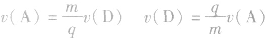
发现相似题
与“碳和碳的化合物广泛的存在于我们的生活中。(1)根据下列反应...”考查相似的试题有:
- T℃时,向10L的密闭容器中同时充入6mol H2和2mol N2,2min末测得生成NH31.2mol,前2min内用N2表示的平均反应速率是______,H2...
- 在3L密闭容器中充入2molSO2和一定量O2,反应生成SO3气体,当进行到6min时,测得n(SO2)=0.4mol,若反应只进行到3min时,容器内...
- 反应3A(g) + B(g) ="=" 2C(g)在三种不同的条件下进行反应,在同一时间内,测得的反应速率用不同的物质表示为:①vA="=1mol/L·min"...
- Ⅰ.某探究小组用HNO3与大理石反应过程中固体质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol...
- 下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快是A.v(H2)="=0.1" mol/(L·min)B.v(N2)==0.1mol/(L·min)C.v...
- 将2 mol X和2 mol Y充入2 L密闭容器中发生如下反应:X(g)+3Y(g)2Z(g)+aQ(g);ΔH=bkJ/mol。达到平衡时生成0.8 mol Z,测得Q的...
- 已知一氧化碳与水蒸气的反应为:CO(g)+H2O (g)CO2(g)+H2(g) ,800℃时,在容积为2.0L的密闭容器中充入2.0mol CO(g)和3.0mol ...
- 对可逆反应4NH3(g)+5O2(g)4NO(g)+6H2O(g),下列叙述正确的是( )A.平衡时,v正(O2)=v逆(O2)必成立B.关系式5v...
- 反应4A(g)+5B(g)=4C(g)+6D(g)在0.5L密闭容器中进行,30s内A减少了0.90mol,则此反应的速率可表示为( )A.v(B)=0.075mol/(...
- 仅改变下列一个条件,通过提高活化分子的百分数来提高反应速率的是A.加热B.加压C.降温D.加大反应物浓度