本试题 “在一定温度下,向一个5L的密闭容器中,通入2 mol N2和8 mol H2及固体催化剂,使之反应。已知:N2(g)+3H2(g)2NH3(g) ΔH=-92.2 kJ·mol-1。平衡时容器内气体...” 主要考查您对化学平衡的有关计算
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学平衡的有关计算
化学平衡计算的一般思路和方法:
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g) pC(g)+ qD(g)
pC(g)+ qD(g)
(1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
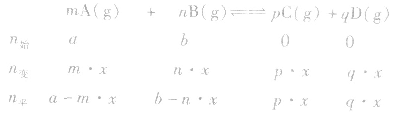
则有:

(2)对于反应物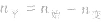 ,对于生成物
,对于生成物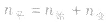
(3)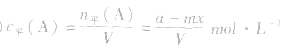
(4)A的转化率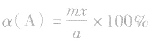
(5)平衡时A的体积(物质的量)分数
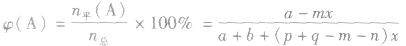
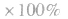
(6)
(7)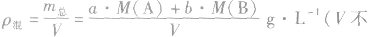
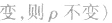
(8)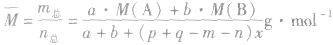
有天化学平衡的计算一般涉及各组分的物质的量、浓度、转化率、百分含量,气体混合物的密度、平均摩尔质量、压强等。通常的思路是写出反应方程式,列出相关量(起始量、变化量、平衡量),确定各量之间的火系,列出比例式或等式或依据平衡常数求解,这种思路和方法通常称为“三段式法”、如恒温恒压下的反应mA(g)+nB(g)
 pC(g)+ qD(g)
pC(g)+ qD(g) (1)令A、B的起始物质的量分别为amol,bmol 达到平衡后,A的消耗量为m·xmol,容器容积为VL。
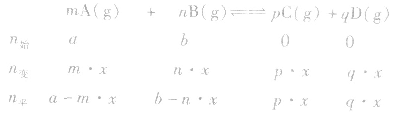
则有:

(2)对于反应物
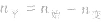 ,对于生成物
,对于生成物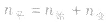
(3)
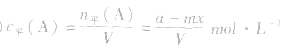
(4)A的转化率
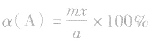
(5)平衡时A的体积(物质的量)分数
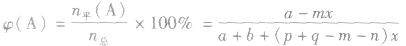
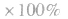
(6)

(7)
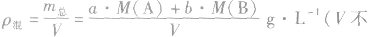
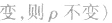
(8)
发现相似题
与“在一定温度下,向一个5L的密闭容器中,通入2 mol N2和8 mol H...”考查相似的试题有:
- (6分)在温度为830°K时,下列可逆反应具有某些特殊性质:CO+H2OH2+CO2若起始浓度[CO]为2mol/L、[H2O]=3mol/L,反应达到平衡...
- (14分)煤炭气化可以提高燃料的利用率,又可以合成新型能源。(1)煤炭气化时发生的反应为:C(s)+H2O(g)H2(g)+CO(g...
- 已知:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H=-41kJ/mol相同温度下,在体积相同的两个恒温密闭容器中,加入一定量的反应物发生...
- A.加入催化剂可以提高单位时间氨的产量B.高压有利于氨的合成反应C. 500℃高温比室温更有利于合成氨的反应D.恒温恒容下,在...
- (14分)合成氨对工、农业生产和国防都有重要意义。已知:N2(g)+3H2(g)2NH3(g);△H= -92.4 kJ·mol-1,请回答:(1)合...
- 在一定条件下,对于反应mA(g)+nB(g)cC(g)+dD(g),C物质的浓度(c%)与温度、压强的关系如图所示,下列判断正确的是 ( )A.△H...
- Ⅰ.恒温恒压下,在一体积可变的密闭容器中发生下列反应:4AC(g)+2BC2(g)4AC2(g)+B2(g),在上述条件下,向容器中充入AC和BC2各1 m...
- (6分)在500℃容积为2升的密闭容器中充入SO2和O2,其中SO2的浓度为1mol/L,经10秒后,达到平衡,2SO2(g)+O2(g)2SO3(g),此时...
- (12分)830K时,在密闭容器中发生下列可逆反应:CO(g)+H2O(g)CO2(g)+H2(g) △H<0 ,试回答下列问题:(1)若起始时...
- 在已达平衡的可逆反应2SO2+O22SO3体系中,加入一定量的18O2,足够长时间后,在_______________物质中存在18O原子。