本试题 “当今世界上最重要的三大矿物燃料是:______、______、______生铁和钢都是______的合金,以赤铁矿为原料冶炼生铁时______ 是还原剂.” 主要考查您对化石燃料
合金
金属的冶炼(铁的冶炼)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化石燃料
- 合金
- 金属的冶炼(铁的冶炼)
概念:
化石燃料是由古代动植物的遗骸经过一系列复杂变化而形成的。化石燃料包括煤(工业的粮食),石油(工业的血液)和天然气,是不可再生能源。
煤:
①煤是固体燃料,其最大的缺点是燃烧速率慢,利朋效率低,且不适用于多数运输业作动力源,还会导致严重的大气污染。从资源、经济与环境三方面综合考虑,适宜在煤产地搞热电联产,提高煤炭转换成电能的比重.住城市发展煤气或液化燃料。煤的综合利用煤是我国主要的化石能源,占90%以上,煤的综合利用措施主要有下列三条:
a.煤的气化:目前主要是煤在高温下与水蒸气的反应。产物为燃料气,又可作化工原料。主要产品有CO、CH4、H2等。
b.煤的焦化:也称煤的干馏,是在隔绝空气的条件下加强热.使组成煤的物质发生分解反应。主要产品及用途:焦炭:金属冶炼;煤焦油:重要的化工原料;焦炉气:含有CO、CH4、H2等,既可作燃料又是重要的化工原料。
c. 煤的液化:煤发生化学反应,分裂为小分子,利用催化剂向小分子中加入氯元素.得到与石油产品成分相近的燃料油,是一项人造石油的技术。
②煤气:
a.煤气的形成:煤气作为一种生活燃料,在一些城市被使用.煤气通常情况下是利用煤与水蒸气在高温条件反应生成的:C+H2O CO+H:煤气的主要成分是CO,但同时含有H2、CH4等其他可燃性气体
CO+H:煤气的主要成分是CO,但同时含有H2、CH4等其他可燃性气体
b.煤气中报警物质的特性:由于煤气的主要成分CO是一种无色、无味的有毒气体,当煤气泄漏时不易察觉,会危害人体健康甚至危及生命。为了安全起见,通常在煤气中加入一些持殊的物质,如乙硫醇(C2H5SH)。乙硫醇具有特殊刺激性气味,当煤气泄漏时,可以使人很快警觉,并马上采取措施,防止发生爆炸、火灾和中毒事故;同时,乙硫醇在煤气燃烧过称中可以充分燃烧不仪煤气.其他可燃性气体如天然气、液化石油气中通常也加入少量报警物质。
石油的综合利用:
①石油是由多种物质组成的混合物,没有同定的组成和性质,根据组成石油的各组分的沸点不同,可从石油中分离出不同的燃料,如汽油、煤油、液化石油气等,
②石油分馏产品及用途
溶剂油——溶剂
汽油—一汽车燃料
航空煤油一一飞机燃料
柴油一—拖拉机、轮船燃料
润滑油一一润滑剂
石蜡——蜡烛
沥青——筑路
石油不仅是优质的能量来源,还是宝贵的化工资源。使石油中的大分子断裂为小分子.小分子重新组合成大分子,从而把石油转化为工农业、医疗、化工等产品,因此把石油称怍“工业的血液”。石油化学工业不同于石油分离,石油化学工业是石油发生复杂的反应,从而生成各种产品,是化学变化。
天然气:
天然气的主要成分是甲烷,主要含碳、氢两种元素。天然气里的甲烷是在隔绝空气的情况下,主要由植物残体分解而生成的。有石油的地方,一般就有天然气。天然气是一种重要的气体燃料。但其贮藏量是有限的。
①甲烷的组成
甲烷是由碳、氢两种元素组成的化合物,其化学式为CH4,是一种最简单的有机物,其中含氢元素的质量分数为25%,是氢元素含量最高的有机物。
②甲烷的性质
a. 物理性质:无色,无味的气体,极难溶于水,它的密度比空气小。
b. 化学性质——可燃性
纯净的甲烷在空气中能安静地燃烧在火焰上方罩一冷而干燥的小烧杯,然后再换一个内壁有石灰水的小烧杯。
现象:烧杯内壁有水珠生成,烧杯内壁的石灰水变浑浊。
结论:甲烷中含有碳元素和氢元素,是由碳和氢两种元素组成的化合物,化学式为CH4。
化学方程式:CH4+O2 CO2+H2O
CO2+H2O
c. 当甲烷与氧气或空气混合后,点燃就有发生爆炸的危险(按体积计算爆炸极限为5%—15%),所以在煤矿的矿井里必须采取通风,严禁烟火等安全措施,以防甲烷和空气等混合发生爆炸。
煤,石油,天然气的区别
化石燃料燃烧与环境的关系:
①化石燃料燃烧产生的物质
化石燃料煤、石油和天然气都是含碳元素的物质.其中还含硫元素等杂质。这些燃料燃烧时,会产生二氧化硫等污染空气的气体,燃料燃烧不充分,会产生一氧化碳和碳粒,加上未燃烧的碳氢化合物,如果直接排放到空气中必然对空气造成污染化石燃料燃烧时排放出的物质有:
a.一氧化碳:
b.碳氢化合物;
c.碳粒和尘粒;
d.二氧化碳
②煤燃烧产生的有害物质
由于煤所含元素有C、H、N、S、O等几种,所以煤燃烧时会排放出二氧化硫、氮的氧化物等.这些气体溶于水会形成酸雨,酸雨会对森林、雕像、建筑物等造成腐蚀。当煤未充分燃烧时,会产生一氧化碳,一氧化碳是夺气的污染物。煤在燃烧时,会散出固体小颗粒(未燃烧的碳粒),造成对空气的粉尘污染。家庭里用煤炉烧煤时,常常会闻到一股激性气味,并看到炉口上方蓝色火焰、这种刺激气昧是烧煤时产生的二氧化硫的气味,蓝色火焰主要是生成的一氧化碳燃烧而产生的。二氧化碳的大量排放,超过自然界的消耗能力,就会引起温室效应,会使大气变暖,陆地减少。
③减少煤燃烧污染的措施
a.燃烧低硫优质煤,或是采用燃料脱硫技术.减少SO2的排放;
b.尽量使燃料完全燃烧;
c.减少化石燃料的使用,开发新能源:
d.植树造林;
e.变分散供热为集中供热。
④汽车用燃料燃烧对空气的影响及减少空气污染的措施
化石燃料的使用与开发:
现有的化石燃料是有限的,而且是不可再生的,每种化石燃料都确有用尽的时候。下表是我同1998年探明的化石燃料储量及产量和使用年限
从表中数据可以看出,节约能源是完全有必要的,也是十分重要的
节约能源,充分利用能源,使燃料充分燃烧,可从以下两个方面着手:
①燃烧时要有足够的空气;
②燃料与空气要有足够大的接触面积,充足的空气才能使燃料尽可能完全燃烧,与空气充分接触才能使其反应快,对能量的利用损失小,
化石燃料是由古代动植物的遗骸经过一系列复杂变化而形成的。化石燃料包括煤(工业的粮食),石油(工业的血液)和天然气,是不可再生能源。
煤:
①煤是固体燃料,其最大的缺点是燃烧速率慢,利朋效率低,且不适用于多数运输业作动力源,还会导致严重的大气污染。从资源、经济与环境三方面综合考虑,适宜在煤产地搞热电联产,提高煤炭转换成电能的比重.住城市发展煤气或液化燃料。煤的综合利用煤是我国主要的化石能源,占90%以上,煤的综合利用措施主要有下列三条:
a.煤的气化:目前主要是煤在高温下与水蒸气的反应。产物为燃料气,又可作化工原料。主要产品有CO、CH4、H2等。
b.煤的焦化:也称煤的干馏,是在隔绝空气的条件下加强热.使组成煤的物质发生分解反应。主要产品及用途:焦炭:金属冶炼;煤焦油:重要的化工原料;焦炉气:含有CO、CH4、H2等,既可作燃料又是重要的化工原料。
c. 煤的液化:煤发生化学反应,分裂为小分子,利用催化剂向小分子中加入氯元素.得到与石油产品成分相近的燃料油,是一项人造石油的技术。
②煤气:
a.煤气的形成:煤气作为一种生活燃料,在一些城市被使用.煤气通常情况下是利用煤与水蒸气在高温条件反应生成的:C+H2O
 CO+H:煤气的主要成分是CO,但同时含有H2、CH4等其他可燃性气体
CO+H:煤气的主要成分是CO,但同时含有H2、CH4等其他可燃性气体 b.煤气中报警物质的特性:由于煤气的主要成分CO是一种无色、无味的有毒气体,当煤气泄漏时不易察觉,会危害人体健康甚至危及生命。为了安全起见,通常在煤气中加入一些持殊的物质,如乙硫醇(C2H5SH)。乙硫醇具有特殊刺激性气味,当煤气泄漏时,可以使人很快警觉,并马上采取措施,防止发生爆炸、火灾和中毒事故;同时,乙硫醇在煤气燃烧过称中可以充分燃烧不仪煤气.其他可燃性气体如天然气、液化石油气中通常也加入少量报警物质。
石油的综合利用:
①石油是由多种物质组成的混合物,没有同定的组成和性质,根据组成石油的各组分的沸点不同,可从石油中分离出不同的燃料,如汽油、煤油、液化石油气等,
②石油分馏产品及用途
溶剂油——溶剂
汽油—一汽车燃料
航空煤油一一飞机燃料
柴油一—拖拉机、轮船燃料
润滑油一一润滑剂
石蜡——蜡烛
沥青——筑路
石油不仅是优质的能量来源,还是宝贵的化工资源。使石油中的大分子断裂为小分子.小分子重新组合成大分子,从而把石油转化为工农业、医疗、化工等产品,因此把石油称怍“工业的血液”。石油化学工业不同于石油分离,石油化学工业是石油发生复杂的反应,从而生成各种产品,是化学变化。
天然气:
天然气的主要成分是甲烷,主要含碳、氢两种元素。天然气里的甲烷是在隔绝空气的情况下,主要由植物残体分解而生成的。有石油的地方,一般就有天然气。天然气是一种重要的气体燃料。但其贮藏量是有限的。
①甲烷的组成
甲烷是由碳、氢两种元素组成的化合物,其化学式为CH4,是一种最简单的有机物,其中含氢元素的质量分数为25%,是氢元素含量最高的有机物。
②甲烷的性质
a. 物理性质:无色,无味的气体,极难溶于水,它的密度比空气小。
b. 化学性质——可燃性
纯净的甲烷在空气中能安静地燃烧在火焰上方罩一冷而干燥的小烧杯,然后再换一个内壁有石灰水的小烧杯。
现象:烧杯内壁有水珠生成,烧杯内壁的石灰水变浑浊。
结论:甲烷中含有碳元素和氢元素,是由碳和氢两种元素组成的化合物,化学式为CH4。
化学方程式:CH4+O2
 CO2+H2O
CO2+H2Oc. 当甲烷与氧气或空气混合后,点燃就有发生爆炸的危险(按体积计算爆炸极限为5%—15%),所以在煤矿的矿井里必须采取通风,严禁烟火等安全措施,以防甲烷和空气等混合发生爆炸。
煤,石油,天然气的区别
| 煤 | 石油 | 天然气 | |
| 形成 | 古代植物被埋在地下经过一系列复杂变化而形成 | 古代植物遗骸在地壳中经过复杂变化而形成 | |
| 元素组成 | 主要含C;少量含:H、N、S、O等 | 主要含C、H,少量含S、N、O | 主要含C、H,主要成分是CH4 |
| 类别 | 混合物(由有机物和无机物组成) | 混合物(多种有机物) | 混合物 |
| 形态 | 黑色固体,有光泽,人称“黑色金子”,无固定的熔点,沸点,具有可燃性 | 粘稠液体,黑色或棕色,不溶于水,密度比水小,无固定的熔点,沸点 | 无色无味气体,密度比空气小,极难溶于水 |
| 性质 | 煤 焦炭,煤焦油、煤气等 焦炭,煤焦油、煤气等 |
石油 溶剂油,汽油,航空煤油,煤油,柴油等 溶剂油,汽油,航空煤油,煤油,柴油等 |
易燃烧,产生明亮的蓝色火焰,化学方程式为CH4+2O2 CO2+2H2O CO2+2H2O |
化石燃料燃烧与环境的关系:
①化石燃料燃烧产生的物质
化石燃料煤、石油和天然气都是含碳元素的物质.其中还含硫元素等杂质。这些燃料燃烧时,会产生二氧化硫等污染空气的气体,燃料燃烧不充分,会产生一氧化碳和碳粒,加上未燃烧的碳氢化合物,如果直接排放到空气中必然对空气造成污染化石燃料燃烧时排放出的物质有:
a.一氧化碳:
b.碳氢化合物;
c.碳粒和尘粒;
d.二氧化碳
②煤燃烧产生的有害物质
由于煤所含元素有C、H、N、S、O等几种,所以煤燃烧时会排放出二氧化硫、氮的氧化物等.这些气体溶于水会形成酸雨,酸雨会对森林、雕像、建筑物等造成腐蚀。当煤未充分燃烧时,会产生一氧化碳,一氧化碳是夺气的污染物。煤在燃烧时,会散出固体小颗粒(未燃烧的碳粒),造成对空气的粉尘污染。家庭里用煤炉烧煤时,常常会闻到一股激性气味,并看到炉口上方蓝色火焰、这种刺激气昧是烧煤时产生的二氧化硫的气味,蓝色火焰主要是生成的一氧化碳燃烧而产生的。二氧化碳的大量排放,超过自然界的消耗能力,就会引起温室效应,会使大气变暖,陆地减少。
③减少煤燃烧污染的措施
a.燃烧低硫优质煤,或是采用燃料脱硫技术.减少SO2的排放;
b.尽量使燃料完全燃烧;
c.减少化石燃料的使用,开发新能源:
d.植树造林;
e.变分散供热为集中供热。
④汽车用燃料燃烧对空气的影响及减少空气污染的措施
| 燃料燃烧对空气的影响 | 减少空气污染的措施 | |
| 汽车用燃料的燃烧 | 汽车使用的燃料 (汽油或柴油)燃烧产生的尾气中,主要污染物有一氧化碳、未燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘等 | ①改进发动机的燃烧方式,使汽油或柴油充分燃烧;②使用催化净化装置,使有害气体转化为无害物质;④使用无铅汽油。禁止含铅物喷排放,同时在管理上加入检测尾气的力度等 |
化石燃料的使用与开发:
现有的化石燃料是有限的,而且是不可再生的,每种化石燃料都确有用尽的时候。下表是我同1998年探明的化石燃料储量及产量和使用年限
| 探明储量 | 年产量 | 使用年限 | |
| 石油 | 32.7亿吨 | 1.6亿 | 约20年 |
| 天然气 | 1.37×104亿立方米 | 217亿立方米 | 约63年 |
| 煤 | 1145亿吨 | 12.4亿 | 约92年 |
节约能源,充分利用能源,使燃料充分燃烧,可从以下两个方面着手:
①燃烧时要有足够的空气;
②燃料与空气要有足够大的接触面积,充足的空气才能使燃料尽可能完全燃烧,与空气充分接触才能使其反应快,对能量的利用损失小,
合金的概念:
合金是在金属中加热熔合某些金属或非金属形成的具有金属特性的物质。
①合金可以是金属与金属或金属与非金属的混合物,不一定全部由金属组成。
②合金具有金属特性,如导电性、导热性、延展性等。
③合金是几种成分熔合在一起形成的,发生的是物理变化,不是化学变化;合金不是几种成分简单地混合而成的。
④合金中各成分仍保持自己的性质。
合金与组成它们的金属的性质比较:
金属熔合了其他金属或非金属后,不仅组成上发生了变化,其内部结构也发生了改变,从而引起性质的变化。因而合金比纯金属具有更广泛的用途。 纯金属与合金性质的比较:
①合金一般比其组分金属的颜色更鲜艳。
②合金的硬度一般应工组成它的金属。
③合金的熔点一般低于成它的金属。
④合金的抗腐蚀能力一般强工组成它的金属。
⑤合金的导电性、导热隆能一般差于组成它的金属。
生铁和钢的比较:
知识点拨:
①生铁和熟铁:生铁是指含碳债在 2%一4.3%之间的铁合金,熟铁是用生铁精炼而成的较纯的铁,含碳量低于0.02%。
②生铁与铸铁:铸铁是生铁中的一种,是指可用来铸造的生铁,通常指球墨铸铁。
③碳素钢的性能与含碳址有关,含碳量越高,硬度越大,但韧性越差;含碳量越低,韧性越好,但硬度越小。
④纯铁与日常生活中铁的颜色差异日常生活,我们接触的铁一般不是纯铁,而是一些铁的氧化物或含铁的混合物,故我们常见的铁的颜色是黑色的,但它并不是纯铁的颜色,纯铁的颜色是银白色的。
应用广泛的合金:
(1)铁合金:铁合金包括生铁和钢,生铁和钢的主要成分是铁,钢与生铁的各种性能不同,主要是由于二者的含碳量不同。
生铁与钢的种类
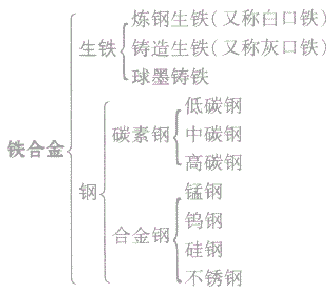
(2)生铁与钢:
生铁的含碳量为2%—4.3%
钢的含碳量为0.03%—2%
(3)钛和钛合金:钛和钛合金被认为是21世纪的重要金属材料。
①性质:优异的耐腐蚀性,对海水、空气和若干腐蚀介质都稳定,可塑性好,强度大,密度小,又称亲生物金属;
②用途:喷气发动机、飞机.机身、人造卫星外壳、火箭壳体、医学补形、人造骨、海水淡化设备、海轮和舰艇的外壳等。
合金是在金属中加热熔合某些金属或非金属形成的具有金属特性的物质。
①合金可以是金属与金属或金属与非金属的混合物,不一定全部由金属组成。
②合金具有金属特性,如导电性、导热性、延展性等。
③合金是几种成分熔合在一起形成的,发生的是物理变化,不是化学变化;合金不是几种成分简单地混合而成的。
④合金中各成分仍保持自己的性质。
合金与组成它们的金属的性质比较:
金属熔合了其他金属或非金属后,不仅组成上发生了变化,其内部结构也发生了改变,从而引起性质的变化。因而合金比纯金属具有更广泛的用途。 纯金属与合金性质的比较:
①合金一般比其组分金属的颜色更鲜艳。
②合金的硬度一般应工组成它的金属。
③合金的熔点一般低于成它的金属。
④合金的抗腐蚀能力一般强工组成它的金属。
⑤合金的导电性、导热隆能一般差于组成它的金属。
生铁和钢的比较:
| 含碳量 | 2%—4% | 0.03%—2% |
| 其他元素 | Si、Mn、S、P(少量) | Si、Mn等 |
| 机械性能 | 硬而脆,无韧性 | 坚硬,韧性大,塑性好,有弹性 |
| 机械加工性质 | 可铸不可锻 | 可铸,可锻,可压延 |
| 分类 | 白口铁,灰口铁,球墨铸铁 | 碳素钢,合金钢 |
知识点拨:
①生铁和熟铁:生铁是指含碳债在 2%一4.3%之间的铁合金,熟铁是用生铁精炼而成的较纯的铁,含碳量低于0.02%。
②生铁与铸铁:铸铁是生铁中的一种,是指可用来铸造的生铁,通常指球墨铸铁。
③碳素钢的性能与含碳址有关,含碳量越高,硬度越大,但韧性越差;含碳量越低,韧性越好,但硬度越小。
④纯铁与日常生活中铁的颜色差异日常生活,我们接触的铁一般不是纯铁,而是一些铁的氧化物或含铁的混合物,故我们常见的铁的颜色是黑色的,但它并不是纯铁的颜色,纯铁的颜色是银白色的。
应用广泛的合金:
(1)铁合金:铁合金包括生铁和钢,生铁和钢的主要成分是铁,钢与生铁的各种性能不同,主要是由于二者的含碳量不同。
生铁与钢的种类

(2)生铁与钢:
生铁的含碳量为2%—4.3%
钢的含碳量为0.03%—2%
(3)钛和钛合金:钛和钛合金被认为是21世纪的重要金属材料。
①性质:优异的耐腐蚀性,对海水、空气和若干腐蚀介质都稳定,可塑性好,强度大,密度小,又称亲生物金属;
②用途:喷气发动机、飞机.机身、人造卫星外壳、火箭壳体、医学补形、人造骨、海水淡化设备、海轮和舰艇的外壳等。
金属冶炼:
金属冶炼是把金属从化合态变为游离态的过程
矿石
①工业上能用来提炼金属的矿物叫做矿石。
②常见的矿石赤铁矿(Fe2O3)、黄铁矿(FeS2)、褐铁矿(Fe2O3·xH2O)、水铝石(Al2O3·H2O)、菱铁矿(主要成分是FeCO3)、磁铁矿(Fe3O4)、方铅矿(PbS)、孔雀石 [Cu2(OH)2CO3]、赤铜矿(Cu2O)、铝土矿(主要成分是Al2O3)、黄铜矿(主要成分是CuFeS2)、辉铜矿(主要成分是Cu2S)。
铁的冶炼
①原理:把铁矿石冶炼成铁是一个复杂的过程,其主要的反应原理是:
在高温下,利用还原剂一氧化碳把铁从铁矿石里还原出来,其反应的化学方程式是: Fe2O3+3CO 2Fe+3CO2
2Fe+3CO2
②炼铁的原料及作用:
铁矿石:提供原料
焦炭:提供能量,产生还原剂
石灰石:将矿石中的二氧化硅转变为炉渣。
③设备:高炉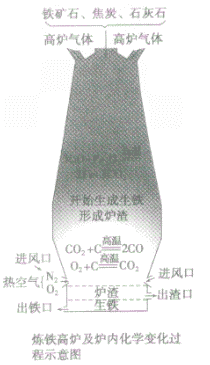
④高炉内有关反应:
a.产生CO提供能量:C+O2 CO2;CO2+C
CO2;CO2+C 2CO
2CO
b.在高温下用CO将Fe从Fe2O3中还原出来:3CO+ Fe2O3 2Fe + 3CO2
2Fe + 3CO2
c.用石灰石将矿石中的SiO2转变为炉渣除去。
CaCO3 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2 CaSiO3
CaSiO3
⑤产品:生铁
炼铁高炉中出铁口低于出渣口的原因:
炼铁高炉中出铁口与出渣口的高低取决于铁水和炉渣的密度〔铁水的密度大于炉渣的密度)。
金属的冶炼方法:
①热分解法(适用于Hg,Ag不活泼的金属的冶炼,加热使其氧化物分解) 如:
2HgO=Hg+O2↑
②热还原法(适用于金属活动性顺序表中,Zn- Cu金属的冶炼)
a.用H2作还原剂(优点:制得金属纯度高,污染小) 如:Fe3O4+4H2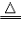 3Fe+4H2O
3Fe+4H2O
b.用焦炭、一氧化碳作还原剂(易混入杂质,污染大气,适合工业化大规模生产) 如:
炼铁的反应方程式为Fe2O3+3CO 2Fe +3CO2
2Fe +3CO2
炼锌的反应万程式为2ZnO+C 2Zn+CO2↑
2Zn+CO2↑
c.用Al作还原剂(铝热剂用来焊接铁轨) 如:
8Al+3Fe3O4 9Fe+4Al2O3
9Fe+4Al2O3
d.电解法(适用于活泼金属Na,Mg等的冶炼) 如:
2NaCl(熔融) 2Na+Cl2↑ ;MgCl2(熔融)
2Na+Cl2↑ ;MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
e.湿法冶金(从溶液中通过化学反应来获取金属) 如:
Fe+CuSO4==Cu+FeSO4
金属冶炼是把金属从化合态变为游离态的过程
矿石
①工业上能用来提炼金属的矿物叫做矿石。
②常见的矿石赤铁矿(Fe2O3)、黄铁矿(FeS2)、褐铁矿(Fe2O3·xH2O)、水铝石(Al2O3·H2O)、菱铁矿(主要成分是FeCO3)、磁铁矿(Fe3O4)、方铅矿(PbS)、孔雀石 [Cu2(OH)2CO3]、赤铜矿(Cu2O)、铝土矿(主要成分是Al2O3)、黄铜矿(主要成分是CuFeS2)、辉铜矿(主要成分是Cu2S)。
铁的冶炼
①原理:把铁矿石冶炼成铁是一个复杂的过程,其主要的反应原理是:
在高温下,利用还原剂一氧化碳把铁从铁矿石里还原出来,其反应的化学方程式是: Fe2O3+3CO
 2Fe+3CO2
2Fe+3CO2 ②炼铁的原料及作用:
铁矿石:提供原料
焦炭:提供能量,产生还原剂
石灰石:将矿石中的二氧化硅转变为炉渣。
③设备:高炉

④高炉内有关反应:
a.产生CO提供能量:C+O2
 CO2;CO2+C
CO2;CO2+C 2CO
2COb.在高温下用CO将Fe从Fe2O3中还原出来:3CO+ Fe2O3
 2Fe + 3CO2
2Fe + 3CO2 c.用石灰石将矿石中的SiO2转变为炉渣除去。
CaCO3
 CaO+CO2↑,CaO+SiO2
CaO+CO2↑,CaO+SiO2 CaSiO3
CaSiO3⑤产品:生铁
炼铁高炉中出铁口低于出渣口的原因:
炼铁高炉中出铁口与出渣口的高低取决于铁水和炉渣的密度〔铁水的密度大于炉渣的密度)。
金属的冶炼方法:
①热分解法(适用于Hg,Ag不活泼的金属的冶炼,加热使其氧化物分解) 如:
2HgO=Hg+O2↑
②热还原法(适用于金属活动性顺序表中,Zn- Cu金属的冶炼)
a.用H2作还原剂(优点:制得金属纯度高,污染小) 如:Fe3O4+4H2
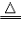 3Fe+4H2O
3Fe+4H2O b.用焦炭、一氧化碳作还原剂(易混入杂质,污染大气,适合工业化大规模生产) 如:
炼铁的反应方程式为Fe2O3+3CO
 2Fe +3CO2
2Fe +3CO2炼锌的反应万程式为2ZnO+C
 2Zn+CO2↑
2Zn+CO2↑ c.用Al作还原剂(铝热剂用来焊接铁轨) 如:
8Al+3Fe3O4
 9Fe+4Al2O3
9Fe+4Al2O3 d.电解法(适用于活泼金属Na,Mg等的冶炼) 如:
2NaCl(熔融)
 2Na+Cl2↑ ;MgCl2(熔融)
2Na+Cl2↑ ;MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑ e.湿法冶金(从溶液中通过化学反应来获取金属) 如:
Fe+CuSO4==Cu+FeSO4
发现相似题
与“当今世界上最重要的三大矿物燃料是:______、______、______...”考查相似的试题有:
- 化学就在我们身边,它与我们的生活息息相关,请从①熟石灰 ②碳酸钠 ③天然气④硝酸钾 ⑤纤维素⑥维生素D ⑦盐酸 ⑧硫酸 这八种物质中...
- 通过化学学习,你是否已经体会到化学就在我们的身边?例如我们初步了解了氢气、一氧化碳、二氧化碳和甲烷等气体的一些重要性...
- 化学就在我们身边,它与我们的生活息息相关.现有下列七种物质:A.聚乙烯B.金刚石C.液氮D.尿素E.盐酸F.醋酸G.石油.请...
- 如果说“龙塔”让人们感受到了哈尔滨的“高度”,那么地铁的正式开通又让人们感受到了哈尔滨的“速度”,下列有关说法错误的是A.作...
- 下列有关铁的说法错误的是[ ]A.地壳中铁元素含量排在第四位B.在铁制品表面镀锌可防锈C.用铁矿石与焦炭在高炉内炼钢D.生铁...
- 生活中所用到的这些物质不属于合金的是[ ]A.不锈钢B. 塑料瓶C. 硬铝D. 锰钢
- 钢铁是人类生活和生产中重要的材料.下列关于钢铁的说法错误的是( )A.生铁和钢是含碳量不同的铁的两种合金B.工业上冶炼钢...
- 下列说法错误的是( )A.钢比生铁的使用价值更高,用途更广泛,是由于钢的性能硬而韧,生铁硬而脆,但含铁量都达到了96%以上...
- 化学就在我们身边,它与我们的生活息息相关.(1)在“生石灰、明矾、钛合金、维生素A”中,选择适当物质填空:①净化水时可作絮...
- 下图是某同学设计的模拟工业炼铁原理的实验装置图.请根据小资料提供的信息和下列要求回答有关问题.(1)写出工业炼铁的化学...