本试题 “下列叙述正确的是( )A.常温常压下,5.6LNH3的物质的量为0.25molB.0.5molH2的质量为1g,体积为11.2LC.40gNaOH溶于1L水中,得到的溶液物质的量浓度为lmol•...” 主要考查您对相对分子质量
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 相对分子质量
定义:
相对分子质量就是化学式中各原子的相对原子质量的总和,符号为Mr。如化学式为AmBn的物质的相对分子质量Mr=A的相对原子质量×m+B的相对原子质量×n。
易错易混点:
①化学式中原子团右下角的数字表示其个数(但BaSO4中的4表示氧原子的个数.不表示原子团 SO42-的个数),计算时先求一个原子团的相对质量,再乘以其个数。如Ca(OH)2的相对分子质量=40+(1+16)× 2=74;
②化学式中的圆点,如“CuSO4·5H2O”中的“·” 表示和,不表示积。即CuSO4·5H2O的相对分子质量CuSO4的相对分子质量+H2O的相对分子量×5=160+18×5=250;
③相对分子质量的单位为1,书写时省略不写;
④计算多个相同分子的相对分子质量总和时,应先求出化学式的相对分子质量再乘以前面的系数,如2KClO,的相对分子质量=2×(39+35.5+16×3) =245;
⑤若已知化合物中某原子的相对原子质量A和原了个数n及其质量分数x%,则化合物的相对分子质量=
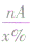
发现相似题
与“下列叙述正确的是( )A.常温常压下,5.6LNH3的物质的量为0....”考查相似的试题有:
- 柠檬酸(C6H8O7)是目前化学清洗中用得较广的有机酸,为无色半透明晶体,无臭、味极酸,易溶于水和乙醇,水溶液显酸性。下列...
- 生活中常见的甜味剂有蔗糖、糖精、阿巴斯甜、木糖醇、安赛蜜等,但目前最甜的甜味剂是纽甜.已知纽甜的化学式为C20H30N2O5,...
- 维生素C(化学式为C6H8O6)对人体皮肤和牙龈的健康有重要作用,缺乏维生素C会引起坏血病.经研究表明,青少年每天都需要摄入6...
- 奥运会“祥云”火炬燃烧时,火炬中的可燃物为X,其燃烧的主要反应为:5O2+ X3CO2+ 4H2O。下列有关X的说法不正确的是[ ]A.X的化...
- 今年9月29日,“天宫一号”成功发射,“天宫一号”在升天前加注的火箭燃料主要是偏二甲肼(C2H8N2)和四氧化二氮(N2O4),下列有...
- 氯化铵是一种常见的化学肥料,请根据题给信息回答:(1)氯化铵(NH4Cl)的相对分子质量是______;氮元素与氢元素的质量比为_...
- 某钢铁厂用含杂质19%的赤铁矿冶炼生铁,求8000kg这种矿石可冶炼出含杂质3.5%的生铁多少千克?
- 有相对分子质量为100的某无水盐X,若50g此无水盐能和36g水结合成结晶水合物,则该结晶水合物的化学式为[ ]A. X·10H2OB. X·2H2...
- 化学式为H2R2O3的物质,其相对分子质量为114,则R的相对原子质量为( )A.32gB.64gC.32D.64
- 北京奥运会“祥云”火炬采用的燃料是丙烷(分子结构模型如图),下列关于丙烷分子的说法正确的是[ ]A.丙烷分子由碳和氢分子组...