本试题 “二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具有优良的环保性能.Ⅰ.工业制备二甲醚的生产流程如下:催化反应室中(压力2.0~10.0Mpa,温度230...” 主要考查您对熵;熵变
化学平衡常数
一次电池
二次电池
燃料电池
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 熵;熵变
- 化学平衡常数
- 一次电池
- 二次电池
- 燃料电池
在一定温度和压强下,无需外界帮助就能自动进行的过程叫做自发过程;在一定温度和压强下,无需外界帮助就可以自发进行到显著程度的化学反应叫自发反应。
化学反应方向的判据:
1.焓变对反应方向的影响:
△H<0 的化学反应也能自发进行。但有些△H>0的化学反应也能自发进行,也就是说,焓变是与化学反应能否自发进行有关的一个重要因素,但不是唯一的因素:
2.熵与熵变:
熵是用于描述体系混乱度的物理量,以符号S表示。熵值越大,体系的混乱度越大。
在一定条件下,不同物质的熵值不同;对同一物质来说,S(g)>S(l)>S(s),S(aq)>S(s)。
物质发生化学反应后熵值也发生变化,这个熵值的变化叫做反应的熵变,以符号△S表示,单位是
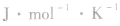 。
。△S=生成物总熵一反应物总熵
若△S为正值,表示反应过程中熵值增大,称为熵增过程;若△S为负值,表示反应过程中熵值减小,称为熵减过程。在与外界隔离的体系中,自发过程将导致体系的熵值增大,这个原理也叫做熵增原理。
3.熵变对反应方向的影响:
△S>0有利于化学反应的自发进行,有些△S>0 的化学反应在常温下不能自发进行,但在较高温度下可以自发进行,有些△S<0的化学反应也能自发进行。总之,熵变是与化学反应能否自发进行有关的一个重要因素,但不是唯一的因素。
4.焓变与熵变对反应方向的共同影响:
在温度和压强一定的条件下,化学反应的方向是反应的焓变和熵变共同影响的结果,反应方向的判据是
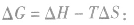
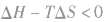 反应能自发进行
反应能自发进行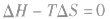 反应达到平衡状态
反应达到平衡状态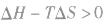 反应不能自发进行
反应不能自发进行在一定温度下,可逆反应无论从正反应开始,还是从逆反应开始,也不管反应物起始浓度大小,最后都达到平衡,这时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值是个常数,用K表示,这个常数叫化学平衡常数。
化学表平衡达式:
对于可逆反应mA(g)+nB(g)
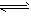 pC(g)+qD(g)来说,化学平衡表达式:
pC(g)+qD(g)来说,化学平衡表达式: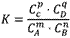
化学平衡常数的意义:
①表示该反应在一定温度下,达到平衡时进行的程度,K值越大,正反应进行的越彻底,对反应物而言转化率越高。
②某一温度下的K′与K比较能够判断反应进行的方向
K′>K,反应正向进行;K′<K,反应逆向进行;K′=K,反应处于平衡状态
(3)化学平衡常数与浓度、压强、催化剂无关,与温度有关,在使用时必须指明温度。
(4)在计算平衡常数时,必须是平衡状态时的浓度。
(5)对于固体或纯液体而言,其浓度为定值,可以不列入其中。
(6)化学平衡常数是指某一具体反应的平衡常数,若反应方向改变,则平衡常数改变,且互为倒数关系。如:在一定温度下,
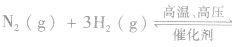


化学平衡常数的应用:
1.K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,反应物转化率越大;反之,正向反应进行的程度就越小,反应物转化率就越小,即平衡常数的大小可以衡量反应进行的程度,判断平衡移动的方向,进行平衡的相关计算。
2.若用浓度商(任意状态的生成物浓度幂之积与反应物浓度幂之积的比值,符号为Qc)与K比较,可判断可逆反应是否达到平衡状态和反应进行的方向。
3.利用K值可判断反应的热效应若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
4.计算转化率及浓度依据起始浓度(或平衡浓度)和平衡常数可以计算平衡浓度(或起始浓度),从而计算反应物的转化率。
电源:
化学电源化学电源是能够实际应用的原电池,化学电池是将化学能转变成电能的装置,它包括一次电池、二次电池和燃料电池等几大类。
一次电池:
(1)普通锌锰干电池构造简单,价格便宜,但放电时间短,放电后电压下降较快。
负极:
正极: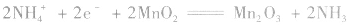
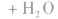
总反应式: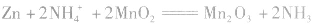
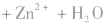
(2)碱性锌锰电池比普通锌锰干电池性能优越,比能量和可储存时间均有提高,适用于大电流和连续放电。负极是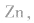 正极是
正极是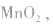 电解质是
电解质是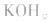
负极: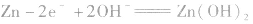
正极:
总反应式: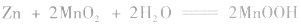
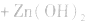
(3)锂电池
用金属锂作负极,石墨作止极,电解质溶液由四氯化铝锂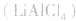 溶解在亚硫酰氯
溶解在亚硫酰氯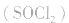 组成。
组成。
负极:
正极:
总反应式: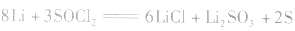
(4)锌银电池
负极是Zn,正极是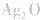 ,电解质是KOH。
,电解质是KOH。
负极: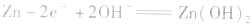
正极: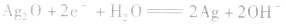
总反应式:
这种电池比能量大,电压稳定,储存时间长,适宜小电流连续放电,常制成纽扣式微型电池,广泛用于电子手表、照相机、计算器和其他微型电子仪器。
(1)蓄电池:蓄电池是可以反复使用、放电后可以充电使活性物质复原、以便再重新放电的电池,也称二次电池。其广泛用于汽车、发电站、火箭等部门。由所用电解质的酸碱性质不同分为酸性蓄电池和碱性蓄电池。
①酸性铅蓄电池铅蓄电池由一组充满海绵状金属铅的铅锑合金格板做负极,由另一组充满二氧化铝的铅锑合金格板做正极,两组格板相间浸泡在电解质稀硫酸中,放电时,电极反应为:
负极:Pb+SO42-=PbSO4+2e- 正极:PbO2+SO42-十4H++2e-=PbSO4+2H2O
总反应:Pb+PbO2+2H2SO4=2PbSO4十2H2O
放电后,正负极板上都沉积有一层PbSO4,放电到一定程度之后又必须进行充电,充电时用一个电压略高于蓄电池电压的直流电源与蓄电池相接,将负极上的PbSO4还原成Pb,而将正极上的PbSO4氧化成PbO2,
充电时发生放电时的逆反应:阴极:PbSO4+2e-=Pb+SO42-阳极:PbSO4+2H2O=PbO2+SO42-+4H++2e- 总反应:2PbSO4+2H2O=Pb+PbO2+H2SO4
②碱性蓄电池日常生活中用的充电电池就属于这类。它的体积、电压都和干电池差不多,携带方便,使用寿命比铅蓄电池长得多,使用信当可以反复充放电上千次,但价格比较贵。商品电池中有镍-镉(Ni-Cd)和镍一铁(Ni-Fe)两类,它们的电池反应是:
Cd+2NiO(OH)+2H2O
 2Ni(OH)2+Cd(OH)2
2Ni(OH)2+Cd(OH)2 Fe+2NaO(OH)+2H2O
 2Ni(OH)2+Fe(OH)2
2Ni(OH)2+Fe(OH)2 反应是在碱性条件下进行的,所以叫碱性蓄电池。
(2)银锌蓄电池 银锌电池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源。目前,有一种类似干电池的充电电池,它实际是一种银锌蓄电池,电解液为KOH溶液。 常见的钮扣电池也是银锌电池,它用不锈钢制成一个由正极壳和负极盖组成的小圆盒,盒内靠正极盒一端充由Ag2O和少量石墨组成的正极活性材料,负极盖一端填充锌汞合金作负极活性材料,电解质溶液为KOH浓溶液,溶液两边用羧甲基纤维素作隔膜,将电极与电解质溶液隔开。
负极:Zn+2OH--2e-=Zn(OH)2
正极:Ag2O+H2O+2e-=2Ag+2OH-?
银锌电池跟铅蓄电池一样,在使用一段时间后就要充电,充电过程表示如下:
阳极:2Ag+2OH--2e-=Ag2O+H2O
阴极:Zn(OH)2+2e-=Zn+2OH-?
总反应式:Zn+Ag2O+H2O
 Zn(OH)2+2Ag
Zn(OH)2+2Ag 一粒钮扣电池的电压达1.59V,安装在电子表里可使用两年之久。
燃料电池:
燃料电池是一种连续地将燃料和氧化剂的化学能直接转化成电能的化学电池。
(1)氧氧燃料电池以氢气为燃料(作负极),以氧气为氧化剂(作正极),可用酸性电解质(如稀H2SO4),也可用碱性电解质(如KOH)。
①若电解质是酸性的,在电极反应式中不能出现OH-。
负极:
正极: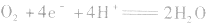
总反应式:
②若电解质是碱性的,在电极反应式中不能出现H+。
负极: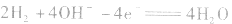
正极: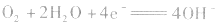
总反应式:
(2)甲烷一氧气燃料电池
若将金属铂片插入KOH溶液中作电极,在两极上分别通入甲烷和氧气。
负极: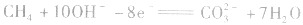
正极: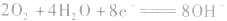
总反应式:
新型化学电源的考查及解题指导:
近几年高考试题中出现的新型电池,有“氢镍电池”“高铁电池”“锌一锰碱性电池”、我国首创的“海洋电池”“燃料电池”(如新型细菌燃料电池、CO燃料电池)、“锂离子电池”“银锌电池~纽扣电池”等。这些电池一般具有高能环保、经久耐用、电压稳定、比能量 (单位质量释放的能量)高等特点。取材于这些知识点的试题,由于题材广、信息新、陌生度大,所以,大多数考生认为这类试题难度大,而难在何处又十分迷茫。实际上这些题目主要考查的是学生对信息的迁移应用能力。具体有以下几个考查角度:
1.新型电池“放电”时正、负极的判断

2.新型电池“放电”时,电极反应式的书写首先根据电池反应分析物质得失电子情况,然后再考虑电极反应生成的物质是否跟电解质溶液巾的离子发生反应;对于较复杂的电极反应,可以利用总反幢方程式减去较简单一极的电极反应式,从而得到较复杂一极的电极反应式。
3.新型电池“充电”时阴、阳极的判断首先明确原电池放电时的正、负极,再根据充电时,阳极接正极、阴极接负极的原理进行分析。
4.新型电池充、放电时,电解质溶液中离子移动方向的判断首先分清电池是放电还是充电;再判断正、负极或阴、阳极,进而可确定离子的移动方向。
与“二甲醚(CH3OCH3)被称为21世纪的新型能源,它清洁、高效、具...”考查相似的试题有:
- 已知反应CO(g)=C(s)+1/2O2(g)的△H>0.设△H和△S都不随温度而变,下列说法中正确的是( ) A.任何温度下都是非自发变化...
- 密闭容器中,反应xA(g)+yB(g)zC(g)达平衡时,A的浓度为0.5mol/L,若保持温度不变,将容器的容积扩大到原来的2倍,达新平衡时A...
- 在某密闭容器中充入HI气体发生反应:2HI(g)H2(g)+I2(g) △H
- 下列有关平衡常数(K、Ka、Kw、Ksp)的说法中错误的是A.若各平衡常数(K、Ka、Kw、Ksp)的值发生变化,则平衡一定发生移动B...
- 下图是恒温下化学反应“A(g)+B(g)C(g)”的反应速率随反应时间变化的示意图,下列叙述与示意图符合的是( )A.平衡态Ⅰ与平衡态...
- 可逆反应H2(g) + I2(g)2HI(g)达到平衡的标志是A.H2、I2、HI的浓度相等B.H2、I2、HI的浓度之比为1:1:2C.混合气体的平均相...
- 一定温度下,在一密闭容器中加入1molPCl5,发生反应PCl5(g)PCl3(g)+Cl2(g)充分反应平衡后,测得PCl5的分解率为a%, 此时,再向密...
- 对于一定不能自发进行的反应来说,反应后体系的A.混乱度减少,而能量增加B.混乱度增大,而能量降低C.混乱度减少,而能量降...
- 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极)。下列说法中正确的是( )A.电池...
- 阿波罗号宇宙飞船上使用的氢氧燃料电池,其电池反应为:2H2+O2=2H2O ,电解质溶液为KOH溶液,反应保持在较高温度,使H2O蒸...