本试题 “下来实验方法和操作有误的是[ ]A.检验有机物中是否含有卤素元素可用铜丝燃烧法B.用纸上层析法分离和检验墨水的成分,为了看到色斑,只有有色离子的检验才可...” 主要考查您对渗析
层析
其他物质的检验
其他物质的制备(硫酸铜晶体、铁红等)
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 渗析
- 层析
- 其他物质的检验
- 其他物质的制备(硫酸铜晶体、铁红等)
渗析:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 渗析 | 胶体提纯、精制 | 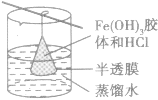 |
除去Fe(OH)3胶体中的HCl | 要不断更换烧杯中的水或改用流动水,以提高渗析效果 |
层析:
利用各组分物理性质的不同,将多组分混合物进行分离及测定的方法。
利用各组分物理性质的不同,将多组分混合物进行分离及测定的方法。
其他物质的检验:
1.有机物的检验
(1)在有机物检验时,需特别知道的物质性质:
①溶解性:有机物均能溶于有机溶剂,能溶于水的有机物为:低级醇、醛、酸。
②密度:比水小:烃、苯及同系物、酯、油脂;比水大:CCl4、溴苯、硝基苯。
③有毒:苯、硝基苯、甲醇、甲醛。
(2)常见有机物或官能团的检验

2.卤代烃中卤元素的检验:与氢氧化钠加热反应后取上层反应完全的清夜,再加入稀硝酸酸化的硝酸银溶液,观察沉淀颜色,白色的是氯离子,淡黄色的是溴离子,黄色的是碘离子
3.淀粉水解产物的检验:用稀硫酸作为催化剂,水解后先加NaOH来中和硫酸酸性,然后再分出一部分加足量碘酒,若变蓝,则仍含有淀粉,未完全水解;反之则已经完全水解;另一部分加土伦试剂或者菲林试剂,检验葡萄糖,若有银镜生成,或者有砖红色沉淀生成,则说明含有还原糖,水解已经发生,反之则没有发生水解。
1.有机物的检验
(1)在有机物检验时,需特别知道的物质性质:
①溶解性:有机物均能溶于有机溶剂,能溶于水的有机物为:低级醇、醛、酸。
②密度:比水小:烃、苯及同系物、酯、油脂;比水大:CCl4、溴苯、硝基苯。
③有毒:苯、硝基苯、甲醇、甲醛。
(2)常见有机物或官能团的检验

2.卤代烃中卤元素的检验:与氢氧化钠加热反应后取上层反应完全的清夜,再加入稀硝酸酸化的硝酸银溶液,观察沉淀颜色,白色的是氯离子,淡黄色的是溴离子,黄色的是碘离子
3.淀粉水解产物的检验:用稀硫酸作为催化剂,水解后先加NaOH来中和硫酸酸性,然后再分出一部分加足量碘酒,若变蓝,则仍含有淀粉,未完全水解;反之则已经完全水解;另一部分加土伦试剂或者菲林试剂,检验葡萄糖,若有银镜生成,或者有砖红色沉淀生成,则说明含有还原糖,水解已经发生,反之则没有发生水解。
实验室制取甲烷(CH4):
(1)反应原理:CH3COONa+NaOH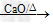 CH4+Na2CO3
CH4+Na2CO3
(2)发生装置:固+固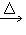 气
气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法/向下排空气法
(5)尾气处理:无
(6)检验方法:①点燃,淡蓝色火焰,燃烧产物是H2O和CO2
实验室制取一氧化氮(NO):
(1)反应原理:3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法
(5)尾气处理:收集法(塑料袋)
(6)检验方法:无色气体,暴露于空气中立即变为红棕色
实验室制取二氧化氮(NO2):
(1)反应原理:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:碱液吸收 (3NO2+H2O==2HNO3+NO;NO+NO2+2NaOH===2NaNO2+H2O)
实验室制取氯化氢(HCl):
(1)反应原理:2NaCl+H2SO4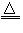 Na2SO4+2HCl?
Na2SO4+2HCl?
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:水(防倒吸装置)
(6)检验方法:①能使湿润的蓝色石蕊试纸变红 ②靠近浓氨水冒白烟
五水硫酸铜的制备:
(1)实验原理:铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到硫酸铜: Cu+2HNO3+H2SO4====CuSO4+2NO2+2H2O 未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在0~100℃范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。
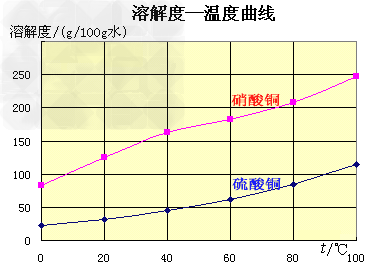
(2)实验步骤
①称量1.5g铜屑,灼烧至表面呈现黑色,冷却;
②加5.5mL3mol/L硫酸,2.5mL浓硝酸,反应平稳后水浴加热,补加2.5mL3mol/L硫酸,0.5mL浓硝酸;
③铜近于完全溶解后,趁热倾滗法分离;
④水浴加热,蒸发浓缩至结晶膜出现;
⑤冷却、过滤;
⑥粗产品以1.2mL水/g的比例,加热溶于水,趁热过滤;
⑦滤液冷却、过滤、晾干,得到纯净的硫酸铜晶体。
⑧称重,计算产率。
实验室制取硫化氢(H2S):
(1)反应原理:FeS+2HCl→H2S↑+FeCl2
(2)发生装置:固+液→气(启普发生器)
(3)净化方法:饱和NaHS(除HCl),固体CaCl2(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:CuSO4溶液或碱液吸收(H2S+2NaOH==Na2S+H2O或H2S+NaOH==NaHS+H2O)
(6)检验方法:①湿润的蓝色石蕊试纸变红 ②湿润的醋酸试纸黑
(1)反应原理:CH3COONa+NaOH
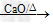 CH4+Na2CO3
CH4+Na2CO3(2)发生装置:固+固
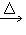 气
气 (3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法/向下排空气法
(5)尾气处理:无
(6)检验方法:①点燃,淡蓝色火焰,燃烧产物是H2O和CO2
实验室制取一氧化氮(NO):
(1)反应原理:3Cu+8HNO3(稀)==3Cu(NO3)2+2NO↑+4H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:排水集气法
(5)尾气处理:收集法(塑料袋)
(6)检验方法:无色气体,暴露于空气中立即变为红棕色
实验室制取二氧化氮(NO2):
(1)反应原理:Cu+4HNO3(浓)==Cu(NO3)2+2NO2↑+2H2O
(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:碱液吸收 (3NO2+H2O==2HNO3+NO;NO+NO2+2NaOH===2NaNO2+H2O)
实验室制取氯化氢(HCl):
(1)反应原理:2NaCl+H2SO4
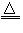 Na2SO4+2HCl?
Na2SO4+2HCl?(2)发生装置:固+液→气
(3)净化方法:浓硫酸(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:水(防倒吸装置)
(6)检验方法:①能使湿润的蓝色石蕊试纸变红 ②靠近浓氨水冒白烟
五水硫酸铜的制备:
(1)实验原理:铜是不活泼金属,不能直接和稀硫酸发生反应制备硫酸铜,必须加入氧化剂。在浓硝酸和稀硫酸的混合液中,浓硝酸将铜氧化成Cu2+,Cu2+与SO42-结合得到硫酸铜: Cu+2HNO3+H2SO4====CuSO4+2NO2+2H2O 未反应的铜屑(不溶性杂质)用倾滗法除去。利用硝酸铜的溶解度在0~100℃范围内均大于硫酸铜溶解度的性质,溶液经蒸发浓缩析出硫酸铜,经过滤与可溶性杂质硝酸铜分离,得到粗产品。硫酸铜的溶解度随温度升高而增大,可用重结晶法提纯。在粗产品硫酸铜中,加适量水,加热成饱和溶液,趁热过滤除去不溶性杂质。滤液冷却,析出硫酸铜,过滤,与可溶性杂质分离,得到纯的硫酸铜。


(2)实验步骤
①称量1.5g铜屑,灼烧至表面呈现黑色,冷却;
②加5.5mL3mol/L硫酸,2.5mL浓硝酸,反应平稳后水浴加热,补加2.5mL3mol/L硫酸,0.5mL浓硝酸;
③铜近于完全溶解后,趁热倾滗法分离;
④水浴加热,蒸发浓缩至结晶膜出现;
⑤冷却、过滤;
⑥粗产品以1.2mL水/g的比例,加热溶于水,趁热过滤;
⑦滤液冷却、过滤、晾干,得到纯净的硫酸铜晶体。
⑧称重,计算产率。
实验室制取硫化氢(H2S):
(1)反应原理:FeS+2HCl→H2S↑+FeCl2
(2)发生装置:固+液→气(启普发生器)
(3)净化方法:饱和NaHS(除HCl),固体CaCl2(除水蒸气)
(4)收集方法:向上排空气法
(5)尾气处理:CuSO4溶液或碱液吸收(H2S+2NaOH==Na2S+H2O或H2S+NaOH==NaHS+H2O)
(6)检验方法:①湿润的蓝色石蕊试纸变红 ②湿润的醋酸试纸黑
发现相似题
与“下来实验方法和操作有误的是[ ]A.检验有机物中是否含有卤素...”考查相似的试题有:
- 为了鉴定溴乙烷中溴元素的存在,试分析①~⑤的各步实验,其中操作顺序合理的是[ ]① 加入AgNO3溶液 ② 加入NaOH溶液 ③ 加热 ④ 用...
- 黄铁矿(FeS2)燃烧产生的SO2通过下列工艺过程既能制得H2SO4,又能制得H2。(1)该过程中能循环利用的物质为 。(2)在该过程...
- 在实验室进行下列有关物质的制备流程中,理论上正确、操作上可行且经济上合理的是[ ]A.CCOCO2Na2CO3B.CuCu(NO3)2溶液Cu(OH)...
- (14分)某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO42CaSO4+2Cl2↑+2...
- 医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用二水合氯化钙工艺流程为:已知...
- 实验室制取下列气体时,其发生装置相同的一组是A.C2H4和O2B.CO2和 Cl2C.NH3和O2D.Cl2和H2
- (10分)二氧化锰是制造锌锰干电池的基本原料,普通锌锰干电池的电池反应式为:2MnO2+Zn+2H2O=2MnOOH+Zn(OH)2。工业上以软锰...
- 孔雀石的主要成分为Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuCl2·3H2O及CaCO3的步骤如下:为解决有...
- 可用图示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)请填空:(1)试管a中需要加入浓硫酸、冰醋酸和乙醇各2mL,正确的计...
- 实验室制取下列气体时,与实验室取氨气的气体发生装置相同的是A.CO2B.H2C.Cl2D.O2