本试题 “Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH4Cl混合溶液.(1)该电池的负极材料是______.电池工作时,电子流向______(填“正极”或“负极”)...” 主要考查您对原电池原理的应用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 原电池原理的应用
(1)根据形成原电池判断金属的活动性根据活泼金属为负极,不活泼金属为正极,可通过组成原电池判断金属活动性。
(2)形成原电池可以加快反应速率纯锌与稀H2SO4反应速率较慢,当加入CuSO4溶液以后,反应速率加快,因为Zn+Cu2+=Cu+Zn2+析出的Cu与Zn接触,在稀H2SO4中形成原电池,加快反应速率。
(3)根据原电池原理可以判断电池的正负极、电解质溶液、判断溶液pH的变化
(4)根据原电池原理可以保护金属不被腐蚀
(5)判断金属腐蚀程度的快慢
原电池原理的应用:
1.比较不同金属的活动性强弱
根据原电池原理可知,在原电池反应过程中,一般活动性强的金属作负极,而活动性弱的金属(或能导电的非金属)作正极。
若有两种金属A和B,用导线将A和B连接后,插入到稀硫酸中,一段时间后,若观察到A极溶解,而B 极上有气体放出,说明在原电池工作过程中,A被氧化成阳离子而失去电子作负极,B作正极,则金属A的金属活动性比B强。
2.加快氧化还原反应的速率
因为形成原电池后,产生电位差,使电子的运动速率加快,从而使反应速率增大,如Zn与稀H2SO4反应制氧气时,可向溶液中滴加少量CuSO4溶液,形成Cu—Zn原电池,加快反应速率 3.用于金属的防护要保护一个铁制闸门,可用导线将其与一锌块相连,使锌作原电池的负极,铁制闸门作正极。
4.设计制作化学电源设计原电池时要紧扣构成原电池的条件。
(1)首先要将已知氧化还原反应拆分为两个半反应:
(2)然后根据原电池的电极反应特点,结合两个半反应找出正、负极材料(一般负极就是失电子的物质,正极用比负极活泼性差的金属或导电的非金属)及电解质溶液:
①电解质溶液的选择电解质溶液一般要能够与负极发生反应,或者能与电极产物发生反应。但如果两个半反应分别在两个容器中进行(中间连接盐桥),左右两个容器中的电解质溶液应选择与电极材料相同的阳离子。如在铜一锌一硫酸铜构成的原电池中,负极金属锌浸泡在含有 Zn2+“的电解质溶液中,而正极铜浸泡在含有Cu2+的溶液中.
②电极材料的选择在原电池中,选择较活泼的金属或还原性较强的物质作为负极,较不活泼的金属或能导电的非金属或氧化性较强的物质作为正极。一般,原电池的负极能够与电解质溶液反应,容易失去电子,因此负极一般是活泼的金属材料(也可以是还原性较强的非金属材料如H2、CH4等)。
(3)举例根据以下反应设计原电池: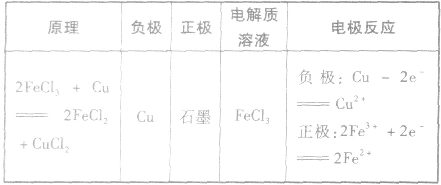
与“Zn-MnO2干电池应用广泛,其示意图如下,电解质溶液是ZnCl2-NH...”考查相似的试题有:
- 银锌电池(钮扣式电池)的两个电极分别是由氧化银与少量石墨组成的活性材料和锌汞合金构成,电解质为氢氧化钾溶液,电极反应...
- 将质量相等的铁片和铜片用导线相连浸入500mL硫酸铜溶液中构成如下图的装置:(以下均假设反应过程中溶液体积不变)。(1)铁...
- 选择适宜的材料和试剂设计一个原电池,完成下列反应:Zn+CuSO4=ZnSO4+Cu(1)画出装置图,并标明各部分材料名称。(2)负极材料 ,正...
- 如图所示装置,均盛有等体积等浓度的稀硫酸,工作相同的时间后测得均通过n mol e-。下列叙述错误的是(不考虑溶液体积的变化)A...
- 如图所示Cu-Zn原电池,下列叙述正确的是A.锌为负极,发生氧化反应B.氢离子在负极得电子C.铜为负极,铜片上有气泡产生D....
- 关于右图所示的原电池,下列说法正确的是A.电子从铜电极通过电流计流向锌电极B.盐桥中的阳离子向硫酸铜溶液中迁移C.锌电极...
- 下列关于下图所示装置的叙述,不正确的是( )A.该装置是利用氧化还原反应将化学能转化成电能B.铁片质量逐渐减少,碳棒上有...
- 锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如下图所示,其中两极区间的隔膜只允许Li+通过。电...
- 现在电池的种类非常多,且由电池造成的污染越来越严重,下列电池不会造成环境污染是A.锂电池B.锌锰电池C.氢氧燃料电池D....
- 从理论上分析,关于Fe—CuSO4溶液—Cu原电池的叙述正确的是A.铜极为负极B.电子从铜沿导线转移到铁C.铁表面析出金属铜D.总反...