本试题 “已知25℃时部分弱电解质的电离平衡常数数据如表所示:化学式CH3COOHH2CO3HClO电离平衡常数Ka=1.8×10-5Kal=4.3×10-7Ka2=5.6×10-11Ka=3.0×10-8 回答下列...” 主要考查您对弱电解质电离的影响因素
弱电解质的电离度
弱电解质的电离
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 弱电解质电离的影响因素
- 弱电解质的电离度
- 弱电解质的电离
电离平衡的影响因素:
(1)温度:由于弱电解质的电离是吸热过程,故升高温度,将使弱电解质的电离平衡向电离方向移动。
(2)浓度:对于同一弱电解质来说,浓度越小,离子相互碰撞结合成分子的机会越小,弱电解质的电离程度就越大。因此,加水稀释溶液会使弱电解质的电离平衡向电离的方向移动,电离程度增大,电离出的离子的总量增加,但离子浓度是减小的。
(3)同离子效应:加入与弱电解质具有相同的离子的强电解质则抑制弱电解质的电离。
(4)化学反应:在弱电解质溶液中加入能与弱电解质电离产生的某种离子反应的物质,可促进弱电解质的电离。
以醋酸归纳为例:
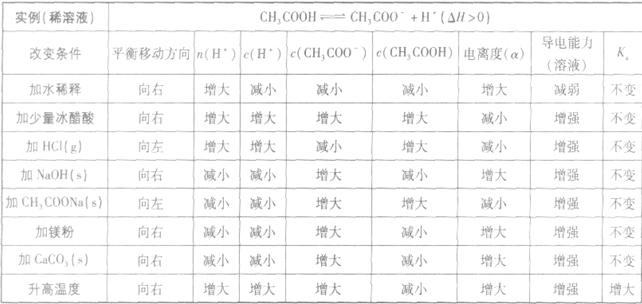
(1)温度:由于弱电解质的电离是吸热过程,故升高温度,将使弱电解质的电离平衡向电离方向移动。
(2)浓度:对于同一弱电解质来说,浓度越小,离子相互碰撞结合成分子的机会越小,弱电解质的电离程度就越大。因此,加水稀释溶液会使弱电解质的电离平衡向电离的方向移动,电离程度增大,电离出的离子的总量增加,但离子浓度是减小的。
(3)同离子效应:加入与弱电解质具有相同的离子的强电解质则抑制弱电解质的电离。
(4)化学反应:在弱电解质溶液中加入能与弱电解质电离产生的某种离子反应的物质,可促进弱电解质的电离。
以醋酸归纳为例:

电离度:
溶液中已电离的分子数占弱电解质分子总数的百分比称为电离度。
溶液中已电离的分子数占弱电解质分子总数的百分比称为电离度。
定义:
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:
(2)动: 的动态平衡
的动态平衡
(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
在一定温度、浓度的条件下,弱电解质在溶液中电离成离子的速率与离子结合成分子的速率相等时,电离过程就到了电离平衡状态,叫弱电解质的电离平衡。

电离平衡的特征:
(1)等:

(2)动:
 的动态平衡
的动态平衡(3)定:条件一定,分子与离子浓度一定。
(4)变:条件改变,平衡破坏,发生移动。
发现相似题
与“已知25℃时部分弱电解质的电离平衡常数数据如表所示:化学式CH...”考查相似的试题有:
- (8分)醋酸是我们很熟悉的一种有机物。(1)生活中可使用醋酸除暖瓶中的水垢,由此说明醋酸具有的性质是 。A.挥发性B.酸性...
- 下列叙述正确的是[ ]A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)B.两种醋酸溶液的物质的量浓度分别为c1...
- 醋酸溶液中存在电离平衡:CH3COOHH++CH3COO-,下列叙述不正确的是[ ]A.CH3COOH溶液中离子浓度的关系满足:c(H+)=c(OH-...
- 部分弱酸的电离平衡常数如下表:弱酸HCOOHHCNH2CO3电离平衡常数(25℃)K=1.77×10-4K=4.9×10-10K1=4.2×10-7K2=5.6×10-11 下列...
- 已知苯酚钠溶液中通入二氧化碳,充分反应后只能生成苯酚和碳酸氢钠;而偏铝酸钠溶液中通入二氧化碳时,可生成氢氧化铝和碳酸...
- 已知:①25℃时弱电解质电离平衡数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Kap(CaF2)=1...
- pH=11的x、y两种碱溶液各5mL,分别稀释至500mL,其pH与溶液体积(V)的关系如图所示。下列说法正确的是( )。A.稀释后x溶液中水...
- 能说明醋酸是弱电解质的事实是( )A.醋酸水溶液能使湿润的蓝色石蕊试纸变红B.醋酸和碳酸钠溶液反应放出二氧化碳C.c(H+)...
- 少量二氧化碳通入NaCN溶液中,发生如下反应:CO2+ H2O + CN-=HCO3-+ HCN。以下说法正确的是(温度均为25℃)A.电离常数:K(HC...
- 有关下列两种溶液的说法中,①:0.1mo1•L-1CH3COONa溶液 ②:0.1mo1•L-1CH3COOH溶液.正确的是( )A.相同温度下,溶液中水的...