本试题 “某课外小组为研究钢铁制品生锈的条件,进行了研究性学习.(1)他们准备了以下实验用品:刚洗净的四只试管、3枚铁钉、植物油、久置的蒸馏水、镊子、滤纸,还...” 主要考查您对金属的锈蚀与防护
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 金属的锈蚀与防护
金属锈蚀:
金属材料受周围介质的作用而损坏,称为金属腐蚀。金属的锈蚀是最常见的腐蚀形态。腐蚀时,在金属的界面上发生了化学或电化学多相反应,使金属转入氧化(离子)状态。这会显著降低金属材料的强度、塑性、韧性等力学性能,破坏金属构件的几何形状,增加零件间的磨损,恶化电学和光学等物理性能,缩短设备的使用寿命,甚至造成火灾、爆炸等灾难性事故。
铁生锈条件的探究
易错点:
①探究铁生锈的条件时采用经煮沸后迅速冷却的蒸馏水,目的是赶走水中溶解的氧气;再加上植物油用来隔绝空气。
②环境中的某些物质会加快铁的锈蚀,如与酸、食盐溶液等接触的铁制品比钢铁生锈更快。
③铁生锈的过程。实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程(缓慢氧化)。反应过程相当复杂,最终生成物铁锈是一种混合物。铁锈(主要成分是Fe2O3·H2O)为红色,疏松多孔,不能阻碍内层的铁继续与氧气、水等反应,因此铁制品可以全部锈蚀。
④许多金属都易生“锈”,但“锈”的结构不同,成分不同。铜在潮湿的空气中也能生“锈”,铜锈即铜绿,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],是铜与水、氧气、二氧化碳共同作用的产物。
金属制品的防锈原理及方法:
(1)防锈原理根据铁的锈蚀条件不难推断出防止铁生锈的方法是使铁制品隔绝空气或隔绝水。
(2)防锈方法:
①保持铁制品表面洁净和干燥,如菜刀不用时擦干放置。
②在钢铁表面覆盖保护膜、如车、船表而涂油漆。
③在钢铁表而镀一层其他金属,如水龙头表面镀铬、镀锌。
④用化学方法使钢铁表面形成致密的保护膜,如烤蓝。
⑤改善金属的结构,如将钢铁制成不锈钢
(3)除锈方法
物理方法:用砂纸打磨,用刀刮。
化学方法:用酸清洗(酸不能过量),发生的反应为:Fe2O3+6HCl==2FeCl3+3H2O或Fe2O3+3H2SO4==Fe2(SO4)3+3H2O。
金属材料受周围介质的作用而损坏,称为金属腐蚀。金属的锈蚀是最常见的腐蚀形态。腐蚀时,在金属的界面上发生了化学或电化学多相反应,使金属转入氧化(离子)状态。这会显著降低金属材料的强度、塑性、韧性等力学性能,破坏金属构件的几何形状,增加零件间的磨损,恶化电学和光学等物理性能,缩短设备的使用寿命,甚至造成火灾、爆炸等灾难性事故。
铁生锈条件的探究
| 实验装置 | 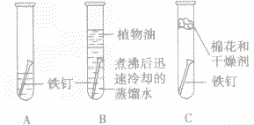 |
| 实验现象 | 几天后观察A试管中铁钉生锈,在水面附近锈蚀 严重,B,C试管中的铁钉没有生锈 |
| 实验分析 | A试管中的铁钉同时跟水、空气(或氧气)接触而生锈; B试管中的铁钉只与水接触不生锈; C 试管中的铁钉只与干燥的空气(或氧气)接触不生锈 |
| 实验结论 | 铁生锈的条件是与水、空气(或氧气)同时接触 |
易错点:
①探究铁生锈的条件时采用经煮沸后迅速冷却的蒸馏水,目的是赶走水中溶解的氧气;再加上植物油用来隔绝空气。
②环境中的某些物质会加快铁的锈蚀,如与酸、食盐溶液等接触的铁制品比钢铁生锈更快。
③铁生锈的过程。实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程(缓慢氧化)。反应过程相当复杂,最终生成物铁锈是一种混合物。铁锈(主要成分是Fe2O3·H2O)为红色,疏松多孔,不能阻碍内层的铁继续与氧气、水等反应,因此铁制品可以全部锈蚀。
④许多金属都易生“锈”,但“锈”的结构不同,成分不同。铜在潮湿的空气中也能生“锈”,铜锈即铜绿,其主要成分为碱式碳酸铜[Cu2(OH)2CO3],是铜与水、氧气、二氧化碳共同作用的产物。
金属制品的防锈原理及方法:
(1)防锈原理根据铁的锈蚀条件不难推断出防止铁生锈的方法是使铁制品隔绝空气或隔绝水。
(2)防锈方法:
①保持铁制品表面洁净和干燥,如菜刀不用时擦干放置。
②在钢铁表面覆盖保护膜、如车、船表而涂油漆。
③在钢铁表而镀一层其他金属,如水龙头表面镀铬、镀锌。
④用化学方法使钢铁表面形成致密的保护膜,如烤蓝。
⑤改善金属的结构,如将钢铁制成不锈钢
(3)除锈方法
物理方法:用砂纸打磨,用刀刮。
化学方法:用酸清洗(酸不能过量),发生的反应为:Fe2O3+6HCl==2FeCl3+3H2O或Fe2O3+3H2SO4==Fe2(SO4)3+3H2O。
发现相似题
与“某课外小组为研究钢铁制品生锈的条件,进行了研究性学习.(1...”考查相似的试题有:
- 全世界每年生锈的钢铁约占钢铁总产量的1/4,铁锈的主要成分是 ,请写出防止钢铁锈蚀的一种方法 ;某同学想从铁锈中回收铁,查...
- 在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的防锈措施中,不属于覆盖保护膜的是A.擦拭保持洁净与干燥B...
- 某同学研究铁在什么条件下容易生锈时,设计了如图实验,放置一周后,发现水下的铁钉都生锈了,由此他得出了结论:铁生锈只与...
- 2010年4月14日青海玉树地区发生7.1级强地震,遇难人数2187人,失踪80人,受伤12135人.(1)地震发生后,全国各地为灾区紧急...
- 结合日常生活中的实例,写出防止铁制品生锈的两种具体做法:①______;②______.
- 下列实验方案合理的是( )A.用点燃的方法除去CO2中混有少量的COB.制备NaOH溶液是将饱和的Na2CO3溶液与适量的石灰水混合C....
- 在下列各种情况下,埋在地下的铸铁输气管道被腐蚀速度最慢的是( )A.在潮湿、疏松、透气的土壤中B.在呈酸性的潮湿土壤中C...
- (1)苯是一种强烈的至癌物,是新装修房子的室内污染物之一.其燃烧的化学方程式为:2X+15O2 点燃 . 12CO2+6H2O,则X的化学式...
- 生铁是含碳量为 的铁合金,在工业上一般用铁矿石、焦炭,石灰石等原料来炼铁,炼铁的化学反应方程式是
- 依据所学的化学知识回答:(1)下列措施错误的是_________(填序号);①油锅不慎着火,立即盖上锅盖;②酸或碱溶液溅入眼睛里...