本试题 “氧气、水、二氧化碳是我们身边重要的物质。(1)上述物质中能供给呼吸的是 ;可用于灭火的是 。(2)A、B都是研究物质组成的实验。B实验中负极得到的气体是 ;A...” 主要考查您对常见污染的来源、危害及治理
电解水实验
空气中氧气含量的测定
氧气的用途
化学反应方程式的书写
二氧化碳的用途
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 常见污染的来源、危害及治理
- 电解水实验
- 空气中氧气含量的测定
- 氧气的用途
- 化学反应方程式的书写
- 二氧化碳的用途
影响环境的因素:
1.化石燃料燃烧对环境的影响
(1)化石燃料充分燃烧的条件及意义
①条件
a.充分接触氧气(或空气);b.提高氧气的浓度
②意义燃料燃烧若不充分,不仅使燃料燃烧产生的热量少、浪费资源.同时会产牛大量的CO等有害气体,污染空气。
(2)煤燃烧产生的危害及防治
①煤燃烧时的危害主要有两个方面
a.煤大量燃烧时生成的CO2易造成温室效应;
b.煤燃烧时生成的SO2、NO2等溶于水生成酸,随雨水降落,形成酸雨。
②防治
a.煤炭脱硫后燃烧;
b.将煤炭进行综合利用:
c.使用清洁能源;
d.尾气进行处理达标后排放等。
(3)汽车尾气对环境的影响及防治
①汽车用的燃料是汽油或柴油,它们燃烧会产生氧化碳、氮的氧化物、未燃烧的碳氢化合物、含铅化合物、烟尘等,合称尾气。这些废气排到空气中,会对空气造成污染,损害人体健康。
②为减少汽车尾气对空气的污染,需采取:
a.改进发动机的燃烧方式,使燃烧充分;
b.使用催化净化装置,使有害气体转化为无害气体;
c.使用无铅汽油,禁止含铅物质排放;
d.加大检测汽车尾气的力度,禁止未达到环保标准的汽车上路;
e.改用压缩天然气或液化石油气或乙醇汽油作燃料。
2.化肥、农药对环境的影响
(1)化肥、农约对环境的危害
①化肥 污染大气(有NH3等不良气体放出) ;污染水体(使水中N、P含节升高,富营养化) ;破坏土壤(使土壤酸化、板结)
污染大气(有NH3等不良气体放出) ;污染水体(使水中N、P含节升高,富营养化) ;破坏土壤(使土壤酸化、板结)
②农药的危害:农药本身是有毒物质,在消除病虫害的同时也带来了对自然环境的污染和对人体健康的危害。
(2)合理使用化肥与农药化肥的施用要以尽量小的投入,尽量小的对环境的影响来保持尽量高的农产品产量和保障食品品质,是我国持续农业生产的主要内容。
在施用农药时,要根据有害生物的发生,发展规律,对症下药、适时用药,并按照观定的施用量、深度、次数合理混用农约和交替使用不同炎型的农药,以便充分发挥不同农药的特性,以最少量的农约获得最高的防治效果,同时又延缓或防止抗药性的产生呢,从而减少对农产品和环境的污染。
3. 其他因素
固体废弃物。工业废水,生活污水都会对环境造成影响。
环境污染和防治:
1. 水污染及防治
(1)水体污染来源
①工业污染:座水、废渣、废气《工业“三反”》。
②农业污染:化肥、农药的不合理使川。
③生活污染:含磷洗涤剂的大量使用、生活污水的任意排放等。
(2)防治措施
①工业上:通过应用新技术、新工艺减少污染物的产生,同时对污染的水体作处理使之符合排放标准。
②农业上:提们使川农家肥,合理使用化肥和农药。
③生活污水也应逐步实现欲中处理和排放。
2. 空气污染及防治
(1)空气污染物及来源:
二氧化硫:含硫燃料的燃烧
二氧化氮:汽车飞机等的尾气
一氧化碳:汽车尾气,含碳燃料的不完全燃烧
可吸入颗粒物:汽车尾气、建筑、生活等城市垃圾扩散
(2)空气污染的防治措施:
①消除污染源
②治理废气
③加强空气质量检测
④植树造林,种草
3.土壤污染及防治
(1)土壤污染的原因及危害
①土壤污染的污染源:农业生产上大量施用化肥、农药;固体废弃物如塑料薄膜;大气中的有害气体和有毒废气随雨水降落污染土壤;污水中的重金属或有毒有害物质污染土壤。
②危害:土壤污染导致严重的直接经济损失—— 农作物的污染、减产;土壤污染破坏土壤正常的生态平衡;土壤污染危害人体健康。
(2)土壤污染的防治防治土壤污染,要以生态农业建设为基础,做到以下几点:
①推广科学测土配方施肥,减少化肥使用量;
②开展农业病虫害综合防治技术,减少农药用量:
③提倡和普及使用有机肥:
④加强工业废弃物及垃圾的管理;
⑤加强对土壤的检验监测力度,制定和完善相关法规。
4.白色污染及防治
白色污染是由难降解的塑料造成的污染,而不是由白色垃圾造成的污染。
(1)白色污染的产生白色污染是指塑料废弃物给环境带来的污染。日常生活中人们使用的塑料购物袋、塑料食品包装、聚苯乙烯一次性泡沫快餐饭盒,还有农村大量使用的家用薄膜等,这些塑料均可产生白色污染。
(2)白色污染的危害塑料使用后丢弃在环境中很难降解,长期堆积会破坏土壤,污染地下水,危害海洋生物的生存,并且如果焚烧含氯塑料会产生有毒的氯化氢气体,从而对空气造成污染。
(3)消除白色污染的措施要解决白色污染问题,应该从以下几个方面入手:
①减少使用不必要的塑料制品,如用布袋代替塑料袋等;
②重复使用某些塑料制品,如塑料袋、塑料盒等;
③使用一些新型的、可降解的塑料,如微生物降解塑料和光降解塑料等。
④回收各种废弃塑料。
5. 三大环境问题
酸雨:
正常情况下,由于雨水中溶有空气中的CO2,故雨水的pH<7而酸雨通常指pH<5.6的雨水。煤燃烧时会排放出NO2、SO2等污染物,这些气体溶于雨水中,会形成酸雨。
(1)酸雨的危害
①使土壤酸化,肥力降低,有毒物质毒害农作物体系,杀死根毛,导敛农作物发育不良或死亡。
②酸雨杀死水中的浮游牛物,减少鱼类食物来源,破坏水生生态系统。
③酸雨污染河流、湖泊和地下水,直接或间接危害人体健康
④酸雨对森林的危害更不容忽视,酸雨淋洗植物表面,直接伤害或通过土壤间接伤害植物,促进森林衰亡。
⑤酸雨对金属、石料、水泥、木材等建筑材料均有很强的腐蚀作用,因而对铁轨、桥梁、房屋等均会造成严重损害。
(2)酸雨的防治
①尽最少用含硫燃料;
②含硫燃料经脱硫后再使用;
③除去烟气中的有害气体再排放;
④开发利用新能源。
臭氧空洞:
(1)1985年,英同科学家首次发现南极上空出现臭氧空洞。
(2)成因:人类存生产生活中向大气排放的氟氯代烃等化学物质与臭氧发生化学反应,使臭氧含量降低,大气巾的臭氧总量明显减少,存南北两极上空下降幅度最大。在南极上空.约有2000多平方千米的区域为臭氧稀薄区,科学家们形象地称之为“臭氧空洞”。
(3)危害:臭氧有吸收太阳紫外线辐射的特性,臭氧层保护地球上的生物免受紫外线的伤害。由于臭氧层巾臭氧的减少,照射到地面的紫外线增强,对地球生物圈中的生态系统和各种牛物,包括人类,都会产生不利影响。
①对人类健康的影响
a.增加皮肤癌患者人数:臭氧减少1%,皮肤癌患者人数增加4%一6%;
b.损害眼晴.增加白内障患者人数;
c.削弱免疫力+增加传染病患者人数。
②对生态系统的影响
a.农产品减产及品质下降;
b.减少渔业产量;
c.破坏森林。
(4)保护臭氧层,防止臭氧减少
①禁止使用氟利昂。
②加大宣传力度,联合国大会通过会议决定,自1985 年开始,每年的9月16日为“吲际保护臭氧层日”
温室效应:
(1)温室效应:大气中的二氧化碳气体能像温室的玻璃或塑料薄膜那样,使地面吸收的太阳光的热量不易散失.从而使全球变暖,这种现象叫温室效应。
(2)温室效应的产生
①由于人类消耗的能源急剧增加,向空气中排放了大量的二氧化碳;森林遭到破坏,使二氧化碳的吸收量减小,从而造成大气中二氧化碳的含量不断上升
②臭氧(O3)、甲烷(CH4)、氟氯代烃等也能产生温室效应。
(3)危害
①两极冰川融化,海平面上升淹没部分沿海城市,
②土地沙漠化,农业减产。
(4)防治措施
①减少使用煤、行油、天然气等化石燃料
②开发新能源,利用太阳能、风能、地热能等
③大力植树造林,严禁乱砍滥伐。
知识拓展:
1. 光化学烟雾
光化学烟雾是一种刺激性的综红色的混合型烟雾,其组成比较复杂,主要是臭氧,此外还有氮的氧化物和过氧酰基硝酸酯、高活性游离基及某些醛类和酮类等。这些物质并非某一个污染源直接排放的原始污染物质,而是由氮的氧化物和碳氢化合物等一次污染物在阳光照射下,发生光化学反应而形成的二次污染物。经过研究发现,氮的氧化物和碳氢化合物是汽车尾气的主要成分。 1970年日本东京一个区受光化学烟雾的毒害,使两万人患眼痛病,正在操场上活动的某校学生,突然害红眼和喉痛,并相继有人昏倒。1971年这种危害已扩散到神奈川县、千叶县等地。
2. 富营养化污染
富营养化污染主要指水流缓慢、更新期长的地表水体,接纳大量氮、磷、有机碳等植物营养素引起的藻类浮游生物急剧增殖的水体污染。自然界湖泊存在着富营养化现象,由贫营养一富营养一沼泽一干地,但速率很慢;而人为污染所致的富营养化,速率很快。特别是在海湾地区。在水温、盐度、日照、降雨、地形、地貌、地质等合适的条件下,细胞中含有红色色素的甲藻或者其他浮游生物大量繁殖,并在上升流的影响下聚积出现,海洋学家称为“赤潮”;如在地下水巾积累,则可称为“肥水”。富营养污染物质的来源是广泛而大量的,有生活污水(有机质、洗涤剂)、农业(化肥、农药)与工业废水、垃圾等。富营养化的显著危害有:
①促使湖泊老化;
②破坏水产资源,日本仅布磨滩1972年赤潮一次死鱼1428万尾;
③危害水源,亚硝酸盐、亚硼酸盐对人畜都有害。
3. 重金属污染
密度在5kg/m3以上的金属统称为重金属,如金、银、铜、钳、锌、镍、钴、镉、铬和汞等。从环境污染方而昕说的蓖金膳,实际卜主要是指永、镉、铅、铬以及类金属砷等生物毒性显著的重金属,也指具有一定毒性的一般再金属如锌、铜、钻、镍、锡等。目前最引人注意的是汞、镉、铬等重金属随废水排出时,即使浓度很小,也可能造成污染。由重金属造成的环境污染称为重金属污染。
电解就是将两根金属或碳棒(即电极)放在要分解的物质(电解质)中,然后接上电源,使电流通过液体。化合物的阳离子移到带负电的电极(阴极),阴离子移到带正电的电极(阳极),化合物分为二极。
电解过程
用电使化合物分解的过程就叫电解过程。
水(H2O)被电解生成电解水。电流通过水(H2O)时,氢气在阴极形成,氧气则在阳极形成。带正电荷的离子向阴极移动,溶于水中的矿物质钙、镁、钾、钠……带正电荷的离子,便在阴极形成,就是我们所喝的碱性水;而带负电的离子,在阴极生成。
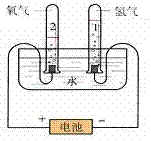
电解水实验:
1.实验装置图:
2.表达式:
水
 氢气+氧气
氢气+氧气2H2O
 2H2↑+O2↑
2H2↑+O2↑3.实验现象:
(1)通电后两电极上都有气泡产生;
(2)与电源正极相连接的一端产生的气体比连接负极一端产生的气体少,
接负极一端玻璃管中气体的体积是接正极一端玻璃管内气体体积的2倍。
4.产物检验
(1)正极一端的气体能使带火星的木条复燃,证明气体是氧气。
(2)负极一端的气体能燃烧,并看到微弱的淡蓝色火焰(或听到爆鸣声),
证明气体是氢气。
5.实验结论:
(1)水是由氢元素和氧元素组成的。
(2)1个水分子由2个氢原子和1个氧原子构成。
(3)化学变化中,分子可以再分,原子不可以再分。
6.注意事项:
(1)实验前在水中加入少量的氢氧化钠或者稀硫酸,可增强水的导电性,
加快反应速率。
(2)实验开始时产生的氧气和氢气的体积会小于1:2,是因为氢气难溶于水,
氧气不易溶于水,开始产生的氧气有一部分溶于水,实验时间越长,
其比值越接近1:2。
电解水记忆口诀:
水中通入直流电,正氧负氢会出现;氢二氧一体积比,任何时候都不变。
空气中氧气含量的测定实验是初中化学的一个重要实验,同时也是历年各地中考命题的热点。近年来在课本实验的基础上进行拓展、创新,旨在考查同学们的实验探究能力及创新思维能力已成为中考命题的趋势。
空气中氧气含量的测定实验:
| 原理 | 利用红磷在空气中燃烧,将瓶内氧气消耗掉,生成五氧化二磷固体,使空气内压强减少,在大气压作用下,进入容器内水的体积即为减少的氧气的体积。4P + 5O2 2P2O5 2P2O5 |
| 装置 | 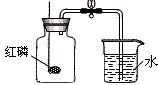 |
| 步骤 | ①连接装置,检查装置气密性 ②把集气瓶的容积分成5等份,做好记号。 ③用止水夹夹紧胶管。 ④在燃烧匙内放入过量的红磷。 ⑤点燃燃烧匙中的红磷,立即伸入集气瓶中,把塞子塞紧 ⑥待红磷熄灭并冷却后,打开止水阀 |
| 现象 | ①集气瓶中有大量的白烟生成,并放出热量 ②打开止水夹,烧杯中的水倒流到集气瓶中,并上升到约1/5处 |
| 结论 | 空气中氧气的体积分数约为1/5。 |
实验中的注意事项:
1.测定空气中氧气的体积分数时,所用物质应满足的条件:
①此物质能够在空气中中燃烧,不能用铁丝代替,铁丝在空气中不能燃烧
②此物质在空气中燃烧的时只能消耗氧气,不能消耗其他气体。不能选用镁代替红磷,因为镁不仅与空气中的氧气反应,还和二氧化碳反应。
③此物质在空气中燃烧时只能生成固体,而不能生成气体,一般不用木炭,硫代替红磷。
2.实验失败与成功的原因:
①装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
②实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
③实验完毕,待容器冷却至室温后,再打开止水夹,观察进水的体积,避免因温度高,气体膨胀,使测定结果低于1/5.
空气中氧气含量测定实验的改进:
1.测定原理:
(1)红磷(白磷)在密闭的容器中燃烧,消耗氧气,生成白色固体五氧化二磷。密闭容器内压强减小,大气压将水压入容器,通过测定容器中的水的量测定氧气在空气中的含量。
(2)利用金属与氧气反应,消耗密闭容器中的氧气使密闭容器内压强减小,在大气压的作用下,推动刻度器上的活塞移动,测出氧气体积。
2.装置
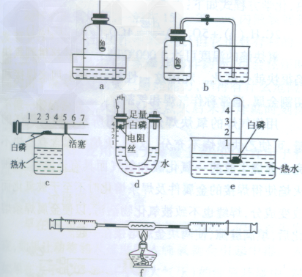
3.实验现象
(1)红磷(白磷)燃烧,产生大量白烟
(2)a中睡眠上升约占钟罩内空气体积的1/5
b中进入集气瓶中水的体积约占集气瓶液面以上容积的1/5
c中活塞移动到4处
d中U形管左侧液面上升至刻度1处
e中试管中液面上升至刻度1处
f中右侧的活塞会左移
4.结论
空气中氧气体积约占空气总体积的1/5
5.注意事项
(1)实验中红磷要过量,以消耗容器内全部氧气,否则会使测定结果低于1/5.
(2)装置不漏气是本实验成功的关键,所以实验前应检查装置的气密性。如果气密性不好,外界空气会进入容器,使测定结果低于1/5。
(3)不能用硫、木炭、铁丝等代替红磷(白磷)。因为硫或木炭燃烧后产生的气体会弥补反应所消耗的氧气,导致测得的体积不准确,而细铁丝在空气中难以燃烧,氧气体积几乎不变,因此密闭空气内水面不上升。
(4)导气管要夹紧,燃烧匙放入集气瓶时要迅速,防止空气受热膨胀,从导气管或集气瓶逸出,导致进入水的体积增多,使实验结果偏高。
用途作用:
1. 冶炼工艺 在炼钢过程中吹以高纯度氧气,氧便和碳及磷、硫、硅等起氧化反应,这不但降低了钢的含碳量,还有利于清除磷、硫、硅等杂质。而且氧化过程中产生的热量足以维持炼钢过程所需的温度,因此,吹氧不但缩短了冶炼时间,同时提高了钢的质量。高炉炼铁时,提高鼓风中的氧浓度可以降焦比,提高产量。在有色金属冶炼中,采用富氧也可以缩短冶炼时间提高产量。
2. 化学工业
在生产合成氨时,氧气主要用于原料气的氧化,以强化工艺过程,提高化肥产量。再例如,重油的高温裂化,以及煤粉的气化等。
3. 国防工业
液氧是现代火箭最好的助燃剂,在超音速飞机中也需要液氧作氧化剂,可燃物质浸渍液氧后具有强烈的爆炸性,可制作液氧炸药。
4. 医疗保健
供给呼吸:用于缺氧、低氧或无氧环境,例如:潜水作业、登山运动、高空飞行、宇宙航行、医疗抢救等时。
5. 其它方面
如:它本身作为助燃剂与乙炔、丙烷等可燃气体配合使用,达到焊割金属的作用,各行各业中,特别是机械企业里用途很广,作为切割之用也很方便,是首选的一种切割方法。
过度吸氧负作用:
早在19世纪中叶,英国科学家保尔·伯特首先发现,如果让动物呼吸纯氧会引起中毒,人类也同样。氧气瓶氧气瓶人如果在大于0.05MPa(半个大气压)的纯氧环境中,对所有的细胞都有毒害作用,吸入时间过长,就可能发生“氧中毒”。肺部毛细管屏障被破坏,导致肺水肿、肺淤血和出血,严重影响呼吸功能,进而使各脏器缺氧而发生损害。在0.1MPa(1个大气压)的纯氧环境中,人只能存活24小时,就会发生肺炎,最终导致呼吸衰竭、窒息而死。人在0.2MPa(2个大气压)高压纯氧环境中,最多可停留1.5小时~2小时,超过了会引起脑中毒,生命节奏紊乱,精神错乱,记忆丧失。如加入0.3MPa(3个大气压)甚至更高的氧,人会在数分钟内发生脑细胞变性坏死,抽搐昏迷,导致死亡。
此外,过量吸氧还会促进生命衰老。进入人体的氧与细胞中的氧化酶发生反应,可生成过氧化氢,进而变成脂褐素。这种脂褐素是加速细胞衰老的有害物质,它堆积在心肌,使心肌细胞老化,心功能减退;堆积在血管壁上,造成血管老化和硬化;堆积在肝脏,削弱肝功能;堆积在大脑,引起智力下降,记忆力衰退,人变得痴呆;堆积在皮肤上,形成老年斑。
缺氧和富氧对人体的影响:
氧气浓度(%体积)---征兆(大气压力下)
100%---致命/6分钟;
50%---致命/4-5分钟经治疗可痊愈
>23.5%---富氧,有强烈爆炸危险
20.9%---氧气浓度正常
19.5%---氧气最小允许浓度
15-19%---降低工作效率,并可导致头部、肺部和循环系统问题
10-12%---呼吸急促,判断力丧失,嘴唇发紫
8-10%---智力丧失,昏厥,无意识,脸色苍白,嘴唇发紫,恶心呕吐
6-8%---8分钟;
4-6%---40秒内抽搐,呼吸停止,死亡
一是必须以客观事实为基础,绝不能凭空设想、主观臆造事实上不存在的物质和化学反应;
二是遵循质量守恒定律,即方程式两边各种原子的种类和数目必须相等。
书写化学方程式的具体步骤:
(1)写:根据实验事实写出反应物和生成物的化学式。反应物在左,生成物在右,中间用横线连接,如: H2+O2——H2O,H2O——H2+O2。
(2)配:根据反应前后原子的种类和数目不变的原则,在反应物和生成物的化学式前配上适当的化学计量数,使各种元素的原子个数在反应前后相等,然后将横线变成等号。配平后,化学式前的化学计量数之比应是最简整数比,如:2H2+O2=2H2O,2H2O= 2H2+O2。
(3)注:注明反应条件【如点燃、加热(常用“△”表示)、光照、通电等〕和生成物的状态(气体用“↑”。沉淀用“↓”。)。如:2H2+O2
 2H2O,2H2O
2H2O,2H2O 2H2↑+O2↑。
2H2↑+O2↑。 化学计量数:
化学计量数指配平化学方程式后,化学式前面的数字。在化学方程式中,各化学式前的化学计量数之比应是最简整数比,计数量为1时,一般不写出。
书学化学方程式的常见错误:
| 常见错误 | 违背规律 |
| 写错物质的化学式 | 客观事实 |
| 臆造生成物或事实上不存在的化学反应 | |
| 写错或漏泄反应条件 | |
| 化学方程式没有配平 | 质量守恒 |
| 漏标多标“↑”、“↓”符号 | —— |
书写化学方程式时条件和气体、沉淀符号的使用:
(1).“△”的使用
①“△”是表示加热的符号,它所表示的温度一般泛指用酒精灯加热的温度。
②如果一个反应在酒精灯加热的条件下能发生,书写化学方程式时就用“△”,如:2KMnO4
 K2MnO4+MnO2+O2↑。
K2MnO4+MnO2+O2↑。 ③如果一个反应需要的温度高于用酒精灯加热的温度,一般用“高温”表示;如:CaCO3
 CaO+ CO2↑
CaO+ CO2↑(2)“↑”的使用
①“↑”表示生成物是气态,只能出现在等号的右边。
②当反应物为固体、液体,且生成的气体能从反应体系中逸出来,气体化学式后应该加“↑”。如Fe+ 2HCl==FeCl2+H2↑。
③当反应物是溶液时,生成的气体容易溶于水而不能从反应体系中逸出来,则不用“↑”,如:H2SO4+ BaCl2==FeCl2+2HCl
④只有生成物在该反应的温度下为气态,才能使用“↑”。
⑤若反应物中有气态物质,则生成的气体不用标 “↑”。如:C+O2
 CO2
CO2 (3)“↓”使用
①“↓”表示难溶性固体生成物,只能出现在等号的右边
②当反应在溶液中进行,有沉淀生成时,用 “↓”,如:AgNO3+HCl==AgCl↓+HNO3
③当反应不在溶液中进行,尽管生成物有不溶性固体,也不用标“↓”,如:2Cu+O2
 2CuO
2CuO ④反应在溶液中进行,若反应物中有难溶性物质,生成物中的难溶性物质后面也不用标“↓”。如:Fe +CuSO4==FeSO4+Cu.
化学方程式中“↑”和“↓”的应用:
①“↑”或“↓”是生成物状态符号,无论反应物是气体还是固体,都不能标“↑”或“↓”;
②若反应在溶液中进行且生成物中有沉淀,则使用“↓”;若不在溶液中进行,无论生成物中是否有固体或难溶物,都不使用“↓”;
③常温下,若反应物中无气体,生成物中有气体.
提取信息书写化学方程式的方法:
书写信息型化学方程式是中考热点,题目涉及社会、生产、生活、科技等各个领域,充分体现了化学学科的重要性,并考查了同学们接受信息、分析问题和解决问题的能力。解答这类题日的关键是掌握好化学方程式的书写步骤,可按两步进行:首先正确书写反应物和生成物的化学式,并注明反应条件及生成物状态;第二步就是化学方程式的配平。
1.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
2.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
3.工业制纯碱和尿素,是一种重要的化工原料
4.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气
二氧化碳中毒:
二氧化碳中毒是人吸入高浓度的二氧化碳所出现的昏迷及脑缺氧情况,一般大气中二氧化碳含量超过1%时,人即有轻度中毒反应;当超过3%时,开始出现呼吸困难;超过6%时,就会重度中毒甚至死亡。
(1)征状
中毒主要征状有:头痛、头愫晕、耳鸣、气急、胸闷、乏力、心跳加快,面颊发绀、烦躁、谵妄、呼吸困难,如情况持续,就会出现嗜睡、淡漠、昏迷、反射消失、瞳孔散大、大小便失禁、血压下降甚至死亡。
(2)补救
打开门窗、通风孔,抢救者才可进入。将病人救出后,在空气新鲜处进行人工呼吸,心脏按摩,吸氧(避免高压、高流量、高浓度给氧,以免呼吸中枢更为抑制),开始1~2L/分,随病人呼吸好转逐渐增大给氧量(4--5L/分),以至采用高压氧治疗。(最好是纯氧)
吸入兴奋剂:多种兴奋剂交替、联合使用,如洛贝林、山梗菜碱等。
防止脑和肺水肿:应用脱水剂、激素,限制液量和速度,吸入钠的份量亦应限制。
对症治疗:给予多种维生素、细胞色素C、能量合剂、高渗糖,以防感染。
抢救同时要留意有没有其他有毒气体存在,如一氧化碳等。
与“氧气、水、二氧化碳是我们身边重要的物质。(1)上述物质中能供...”考查相似的试题有:
- 能源和环境有着密切的联系.下列能源会对环境造成污染的是( )A.氢能B.太阳能C.石油D.风能
- 下列各组中的环境问题与治理措施无关的是 ABCD环境问题温室效应土地沙漠化酸雨蓝藻爆发治理措施减少使用化石燃料植树造林回收...
- 下列有关“化学与生活”的说法中,正确的是[ ]A.铝合金比铁制品耐腐蚀是因为铝的化学性质不如铁活泼B.用焚烧的方法处理废弃的...
- 与北京奥运相比,上海世博会将扩大各类新能源车的运用,约1000辆新能源汽车将为世博服务。其中,约500辆车为超级电容车、纯电...
- 下列有关实验现象的描述正确的是A.铁丝在空气中燃烧时火星四射,有黑色四氧化三铁固体生成B.铁钉与稀盐酸反应后溶液由无色...
- 健康的鸡所产的蛋有害细菌很少,一般是在贮藏、加功中受到污染,微生物通过气孔或孔隙进入蛋内,而导致鸡蛋腐败变质.鸡蛋的...
- 请写出实验室制取O2的化学方程式______(任写一个),该反应属于______反应(选填“化合”、“分解”、“置换”、“复分解”).
- 下列化学方程式符合题意且书写正确的是( )A.用氢氧化钠溶液检验二氧化碳:CO2+2NaOH═Na2CO3+H2OB.军事上用红磷作烟幕弹:...
- (1)原子数相同、核外电子总数也相同的粒子(分子或离子)互称为等电子体,等电子体往往具有相同的结构和相似的性质,写出下...
- 按要求选择适当的物质,用其前面的字母填空.A.肥皂水 B.干冰 C.洗洁精 D.食醋(1)人工降雨可使用______. (2)除去水...