本试题 “下列叙述正确的是[ ]A.Li在氧气中燃烧主要生成Li2O2B.将SO2通入BaCl2溶液中可生成BaSO3沉淀C.将CO2通入次氯酸钙溶液中可生成次氯酸D.由于铝在常温下不能与氧...” 主要考查您对单质铝
61. 其它金属及化合物(锌、锰、钙、金等)
二氧化硫
碳单质及化合物
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 单质铝
- 61. 其它金属及化合物(锌、锰、钙、金等)
- 二氧化硫
- 碳单质及化合物
铝的主要性质:
- 物理性质:
铝是银白色,具有金属光泽的固体,硬度较小,具有良好的导电性、导热性和延展性。 - 化学性质:
活泼金属,具有较强的还原性;常温下铝在浓硫酸和浓硝酸中发生钝化;既可以与酸反应又可以与碱反应。
(1)与氧气反应: (纯氧中发出耀眼的白光)
(纯氧中发出耀眼的白光)
(2)与Cl2 、S 、N2反应: (Al2S3在溶液中完全双水解)
(Al2S3在溶液中完全双水解)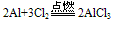
 (AlN与水反应生成Al(OH)3和NH3↑)
(AlN与水反应生成Al(OH)3和NH3↑)
(3)与水反应: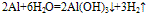
(4)与酸反应: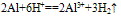
(5)与碱的反应:
(6)铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe - 铝的用途
纯铝制作导线,铝合金用于制造飞机、汽车、生活用品等。
铝的特殊性质:
铝既能与酸反应,也能与强碱反应。
铝与酸反应:铝与浓硫酸在常温下发生钝化,2Al+6HCl==2AlCl3+3H2↑
铝与碱反应:2Al+2NaOH+2H2O==2NaAlO2+3H2↑
铝热反应:
铝热法是一种利用铝的还原性获得高熔点金属单质的方法。此种反应被称为铝热反应。
可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3、V2O5等)或非金属氧化物(如SiO2等)在高热条件下发生的反应。
铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应,
其中镁条为引燃剂,氯酸钾为助燃剂。
其装置如下图所示: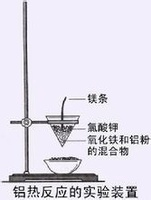
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,然后便可得到Al为8,Fe为9。
镁铝的化学性质比较:
| 单质 | 镁 | 铝 |
| 与非金属反应 | 2Mg+O2=(点燃)=2MgO (发出耀眼白光) Mg+Cl2=(点燃)=MgCl2 3Mg+N2=(点燃)=Mg3N2 |
4Al+3O2=(加热)=2Al2O3 2Al+3Cl2=(加热)=2AlCl3 2Al+3S=(加热)=Al2S3 |
| 与沸水反应 | Mg+2H2O=(加热)=Mg(OH)2+H2↑ | 不反应 |
| 与酸反应 | Mg+2H+==Mg2++H2↑ 与稀硝酸反应生成Mg(NO3)2、NOx(或者N2、NH4NO3)、H2O |
2Al+6H+==2Al3++3H2↑ 在冷的浓硝酸或浓硫酸中钝化 |
| 与氧化物反应 | 2Mg+CO2=(点燃)=2MgO+C (剧烈燃烧,生成白色粉末和黑色固体) |
2Al+Fe2O3=(高温)=2Fe+Al2O3(铝热反应) |
| 与盐溶液反应 | Mg+2NH4++2H2O==Mg2++2NH3·H2O+H2↑ Mg+Cu2+==Mg2++Cu |
2Al+3Hg2+=2Al3++3Hg |
| 与强碱反应 | 不反应 | 2Al+2OH-+2H2O==2AlO2-+3H2↑ |
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,底下便可得到Al为8,Fe为9。
铝与酸、碱反应的计算技巧:
铝与酸、碱反应的实质都是 ,
, ,所以根据得失电子守恒可知:
,所以根据得失电子守恒可知: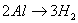 ,利用此关系可以方便地进行有关计算。
,利用此关系可以方便地进行有关计算。
铝与酸或碱溶液反应生成H2的量的计算:
Al是我们中学阶段学习的唯一既与H+反应也与OH-反应的金属,它与酸、碱反应既有相同点,也有不同点。
相同点:Al均被氧化成+3价,所以1molAl不论与H+还是与OH-反应均生成3gH2。
不同点:1molAl与H+反应消耗3molH+,而与OH-反应只消耗1molOH-,所以含有等物质的量的NaOH溶液和HCl溶液分别与足量的铝反应时生成的氢气的物质的量之比为3∶1。

“铝三角”关系:
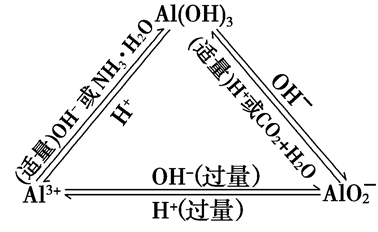
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
钝化:
铝、铁在常温下与浓硫酸发生钝化,钝化不是不反应,而是被氧化成一层致密的氧化物薄膜,恰恰说明金属的活泼性。
锌的单质及化合物:
①单质锌:
物理性质:锌化学符号是Zn,它的原子序数是30。锌是一种蓝白色金属。密度为7.14克/立方厘米,熔点为419.5℃。在室温下,性较脆;100~150℃时,变软;超过200℃后,又变脆。锌的化学性质活泼,在常温下的空气中,表面生成一层薄而致密的碱式碳酸锌膜,可阻止进一步氧化。当温度达到225℃后,锌氧化激烈。燃烧时,发出蓝绿色火焰。锌易溶于酸,也易从溶液中置换金、银、铜等。锌的氧化膜熔点高,但金属锌熔点却很低,所以在酒精灯上加热锌片,锌片熔化变软,却不落下,正是因为氧化膜的作用。锌是第四常见的金属,仅次于铁、铝及铜。
化学性质:2Zn+O2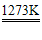 2ZnO Zn+X2
2ZnO Zn+X2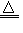 ZnX2(X=F、Cl、Br、I) 3Zn+2P
ZnX2(X=F、Cl、Br、I) 3Zn+2P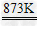 Zn3P2 Zn+S
Zn3P2 Zn+S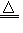 ZnS
ZnS
②氢氧化锌 Zn2++2NaOH==Zn(OH)2+2Na+ Zn(OH)2+2H+==Zn2++H2O Zn(OH)2+2OH-==[Zn(OH)4]2- Zn(OH)2+4NH3+2NH4+==[Zn(NH3)4]2++2H2O Zn(OH)2==ZnO+H2O
[Zn(NH3)4]2++2OH-==Zn(OH)2+4NH3↑
③氯化锌 ZnO+2HCl ZnCl2+H2O ZnCl2+2H2O===Zn(OH)Cl+2HCl ZnCl2+H2O=H2[ZnCl2(OH)2] FeO+H2[ZnCl2(OH)2]==Fe[ZnCl2(OH)]2+H2O Zn+CuCl2=ZnCl2+Cu
ZnCl2+H2O ZnCl2+2H2O===Zn(OH)Cl+2HCl ZnCl2+H2O=H2[ZnCl2(OH)2] FeO+H2[ZnCl2(OH)2]==Fe[ZnCl2(OH)]2+H2O Zn+CuCl2=ZnCl2+Cu
④硫化锌 2ZnO+2S==2ZnS+O2 Zn2++(NH4)2S==ZnS+2NH4+ ZnSO4+BaS==ZnS+BaSO4 Zn2++H2S==ZnS+2H+
⑤锌的配合物(a)[Zn(NH3)4]2+、(b)[Zn(CN)4]2-
钙的单质及化合物:
①单质钙:活泼金属
②氧化钙:俗称生石灰,白色块状固体;与水反应放出大量热,块状固体变成粉末状CaO+H2O==Ca(OH)2
③氢氧化钙:俗称熟石灰,常用来检验二氧化碳气体Ca(OH)2+CO2==CaCO3↓+H2O
④碳酸钙:俗称石灰石,白色固体,不溶于水,常用的建筑材料,实验室常用其和稀盐酸反应制取二氧化碳CaCO3+2HCl==CaCl2+CO2↑+H2O
银的单质及化合物:
①物理性质:银是一种化学元素,化学符号Ag,原子序数47,是一种银白色的贵金属。银性质稳定,质软富有延展性。导热,导电率高,不易受酸碱的腐蚀
②化学性质:银的特征氧化数为+1,其化学性质比铜差,常温下,甚至加热时也不与水和空气中的氧作用。但当空气中含有硫化氢时,银的表面会失去银白色的光泽,这是因为银和空气中的H2S化合成黑色Ag2S的缘故。其化学反应方程式为: 4Ag+H2S+O2=2Ag2S+2H2O
银不能与稀盐酸或稀硫酸反应放出氢气,但银能溶解在硝酸或热的浓硫酸中:2Ag+2H2SO4(浓) Ag2SO4+SO2↑+2H2O
Ag2SO4+SO2↑+2H2O
银在常温下与卤素反应很慢,在加热的条件下即可生成卤化物:
2Ag+F2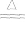 2AgF暗棕色
2AgF暗棕色
2Ag+Cl2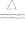 2AgCl白色
2AgCl白色
2Ag+Br2 2AgBr淡黄色
2AgBr淡黄色
2Ag+I2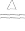 2AgI黄色
2AgI黄色
银对硫有很强的亲合势,加热时可以与硫直接化合成Ag2S:2Ag+S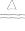 Ag2S
Ag2S
银易溶于硝酸和热的浓硫酸,微溶于热的稀硫酸而不溶于冷的稀硫酸。盐酸和王水只能使银表面发生氯化,而生成氯化银薄膜。
银具有很好的耐碱性能,不与碱金属氢氧化物和碱金属碳酸盐发生作用。
①化学式:SO2
②分子结构:SO2是由极性键形成的极性分子,因此易溶于水,其晶体为分子晶体。
二氧化硫的物理性质和化学性质:
1.物理性质:
SO2是无色、有刺激性气味的有毒气体,密度比空气大,易溶于水(常温常压下,1体积水大约溶解40体积的SO2),易液化(沸点-10℃)。
2.化学性质
(1)具有酸性氧化物的通性
①将SO2通入紫色石蕊试液中,试液变红。
②能与碱性氧化物、碱及某些盐反应。如:
(2)还原性 

(3)弱氧化性 
(4)漂白性(不能漂白酸碱指示剂) 能和某些有色物质化合生成无色物质,生成的无色物质不稳定,易分解而恢复原色,因此,SO2的漂白并不彻底。在中学化学常见试剂中,能用SO2漂白的只有品红溶液,品红溶液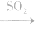 无色溶液
无色溶液 恢复原色。
恢复原色。
SO2与一些物质反应的实验现象:


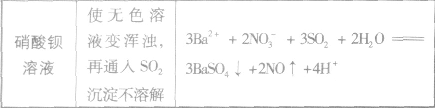
SO2与强碱反应后固体成分的确定:
SO2与强碱(如NaOH)溶液发生反应后的固体成分取决于二者的用量。遇到类似的问题,可以采用数轴分析法讨论。设SO2的物质的量为n(SO2),NaOH物质的量为n(NaOH),数轴代表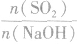 ,如下数轴所示:
,如下数轴所示: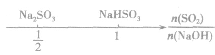
分析数轴可得:
(1)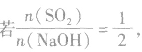 则固体物质为Na2SO3,
则固体物质为Na2SO3,
(2)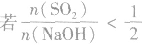 ,则固体物质为NaOH 和Na2SO3.
,则固体物质为NaOH 和Na2SO3.
(3)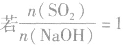 ,则同体物质为NaHSO3
,则同体物质为NaHSO3
(4)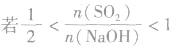 ,则固体物质为Na2SO3和NaHSO3,
,则固体物质为Na2SO3和NaHSO3,
(5)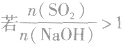 ,则固体物质为NaHSO3。
,则固体物质为NaHSO3。
二氧化硫的制备:
工业制法:

实验室制法:
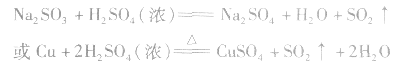
(1)收集:向上排空气法。
(2)检验:品红溶液。SO2是中学阶段学到的唯一种既能使品红褪色,加热后又能使其恢复原色的气体。
(3)尾气处理:用NaOH溶液吸收。
二氧化硫的用途:
工业上用二氧化硫漂白纸浆、毛、丝、草编制品等。此外,二氧化硫还可用于杀菌消毒,可以用作防腐剂。
二氧化硫对环境的污染及治理:

碳:
①元素符号:C
②原子结构示意图: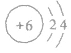
③电子式: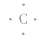
④周期表中位置:第二周期ⅣA族
⑤含量与存在:在地壳中的含量为0.087%,在自然界中既有游离态,又有化合态
⑥同素异形体:金刚石、石墨、C60、活性炭
碳(活性炭):
①金刚石:纯净的金刚石是无色透明、正八面体形状的固体,硬度大,熔点高,不导电,不溶于水
石墨:深灰色的鳞片状固体,硬度小,质软,有滑腻感,熔点高,具有导电性
活性炭:黑色粉末状或颗粒状的无定形碳,疏松多孔,有吸附性
②碳的化学性质:
a.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
b.可燃性:氧气充足的条件下:C+O2 CO2 氧气不充分的条件下:2C+O2
CO2 氧气不充分的条件下:2C+O2 2CO
2CO
c.还原性:
木炭还原氧化铜:C+2CuO 2Cu+CO2↑
2Cu+CO2↑
焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑
3Fe+2CO2↑
木炭与二氧化碳的反应:C+CO2 CO
CO
二氧化碳:
①物理性质:常温下,二氧化碳是一种无色无味的气体,密度比空气大,能溶于水。固态的二氧化碳叫做干冰。
②化学性质:
a.一般情况下,二氧化碳不能燃烧,也不支持燃烧,不供给呼吸,因此当我们进入干枯的深井,深洞或久未开启的菜窖时,应先做一个灯火实验,以防止二氧化碳浓度过高而造成危险
b.二氧化碳和水反应生成碳酸,使紫色石蕊试液变红:CO2+H2O===H2CO3,碳酸不稳定,很容易分解成水和二氧化碳,所以红色石蕊试液又变回紫色:H2CO3===H2O+CO2↑
c.二氧化碳和石灰水反应:Ca(OH)2+CO2====CaCO3↓+H2O
d.二氧化碳可促进植物的光合作用:6CO2+6H2O C6H12O6+6O2
C6H12O6+6O2
③用途:
a.二氧化碳不支持燃烧,不能燃烧,比空气重,可用于灭火
b.干冰升华时吸收大量的热,可用它做制冷剂或人工降雨
c.工业制纯碱和尿素,是一种重要的化工原料 d.植物光合作用,绿色植物吸收太阳能,利用二氧化碳和水,合成有机物放出氧气。
一氧化碳:
①物理性质:通常状况下,是一种没有颜色,气味的气体,比空气略轻难溶于水。
②化学性质
a.可燃性:2CO+O2 2CO2
2CO2
b.还原性:一氧化碳还原氧化铜:CO+CuO Cu+CO2 一氧化碳还原氧化铁:3CO+Fe2O3
Cu+CO2 一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO2 一氧化碳还原四氧化三铁:4CO+Fe3O4
2Fe+3CO2 一氧化碳还原四氧化三铁:4CO+Fe3O4 3Fe+4CO2
3Fe+4CO2
c.毒性:一氧化碳能与人体血液中的血红蛋白结合,使血红蛋白失去运输氧气的能力,造成机体缺氧。冬天用煤火取暖,如排气不良,就会发生煤气中毒,就CO中毒。CO重要来源是汽车尾气和煤,石油等含碳燃料的不完全燃烧。
③用途:用作燃料,冶炼金属。 ④碳酸:弱酸,不稳定,易分解H2CO3==CO2↑+H2O
碳酸盐:
1.正盐与酸式盐的比较
| 正盐 | 酸式盐 | |
| 水溶性 | 除K、Na、铵的碳酸盐易溶于水外,其余都难溶于水 | 都溶于水 |
| 热稳定性 | 较稳定 ①K2CO3、Na2CO3等碱金属的正盐受热难分解 ②CaCO3、(NH4)2CO3 等受热易分解 |
受热易分解 2NaHCO3  Na2CO3+ H2O+CO2↑ Na2CO3+ H2O+CO2↑Ca(HCO3)2  CaCO3+H2O+CO2↑ CaCO3+H2O+CO2↑ |
| 与酸反应 | CO32-+2H+== CO2↑+H2O CaCO3+2H+=Ca2+ +H2O+CO2↑ |
HCO3-+H+==H2O+ CO2↑(相同条件下,NaHCO3与酸反应放出CO2的速率比Na2CO3快) |
| 与碱反应 | Na2CO3+Ca(OH)2 ==CaCO3↓+2NaOH | NaHCO3+NaOH==Na2CO3+H2O Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O |
| 转化关系 |  | |
(1)在水中的溶解性:一般地,相同温度下,难溶性正盐的溶解度小于其酸式盐,可(易)溶性正盐的溶解度大于其酸式盐。如CaCO3,难溶于水,Ca(HCO3)2易溶于水;Na2CO3易溶于水,NaHCO3的溶解度比 Na2CO3的小。
(2)与酸或碱反应:强酸的酸式盐只与碱反应而不与酸反应;弱酸的酸式盐与足量强碱反应生成正盐,与足量强酸反应生成弱酸。
(3)热稳定性:一般地,热稳定性的大小顺序为正盐>酸式盐(盐的阳离子相同,成盐的酸相同)。
3.碳酸钙在自然界中存在广泛,是岩石的主要成分之一。不溶于水,但溶于酸。大理石、石灰石的主要成分是CaCO3,它们既是重要的化工原料,又是重要的建筑材料。其用途图示如下:
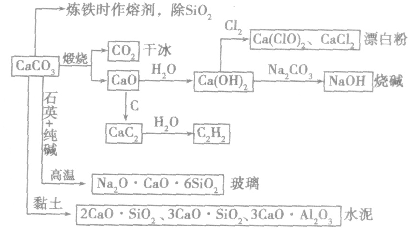
CO2气体与溶液的反应规律:
1.向某溶液中不断通入CO2气体至过量时,现象是“先产生白色沉淀,后沉淀逐渐溶解”
(1)向澄清石灰水中不断通入CO2气体的反应为:
Ca(OH)2+CO2==CaCO3↓+H2O
CaCO3+CO3+H3O==Ca(HCO3)2
(2)向氧氧化钡溶液中不断通入CO2气体的反应为:
Ba(OH)2+CO2==BaCO3↓+H2O
BaCO3+CO2+H2O==Ba(HCO3)2
(3)向漂白粉溶液中不断通入CO2气体的反应为:
Ca(ClO)2+CO2+H2O==CaCO3↓+2HClO
CaCO3+CO2+H2O==Ca(HCO3)2
2.向某溶液中不断通入CO2气体至过量时,现象为“产生白色沉淀或浑浊,沉淀或浑浊不消失”
(1)在NaAlO2溶液中不断通入CO2气体至过量时,反应为:
2AlO2-+CO2(少量)+3H2O==2Al(OH)3↓ +CO32-
2AlO2-+CO2(过量)+2H2O==Al(OH)3↓ +HCO3-
(2)向Na2SiO3溶液中不断通入CO2气体至过量时,反应为:
SiO32-+CO2+H2O==H2SiO3↓+CO32-
SiO32-+2CO2+2H2O==H2SiO3↓+2HCO3-
(3)向饱和Na2CO3溶液中不断通入CO2气体,反应为:
2Na++CO32-+CO2+H2O==2NaHCO3↓
3.CO2与NaOH溶液反应后,溶液中溶质的判断将CO2气体逐渐通入NaOH溶液中,先后发生化学反应:
①CO2+2NaOH==Na2CO3+H2O
②CO2+Na2CO3+H2O==2NaHCO3
向一定量的NaOH溶液中通入CO2气体后,溶液中溶质的成分要根据NaOH与CO2的物质的量之比进行讨论。
当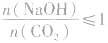 时,发生反应①和②,溶液中的溶质为NaHCO3;
时,发生反应①和②,溶液中的溶质为NaHCO3;
当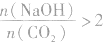 时,发生反应①,溶液中的溶质为 Na2CO3和NaOH;
时,发生反应①,溶液中的溶质为 Na2CO3和NaOH;
当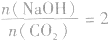 时,发生反应①,溶液中的溶质为Na2CO3;
时,发生反应①,溶液中的溶质为Na2CO3;
当 时,发生反应①和②,溶液中为Na2CO3和NaHCO3
时,发生反应①和②,溶液中为Na2CO3和NaHCO3
碳酸氢盐与碱反应的规律及CO32- HCO3-的鉴别方法:
1.酸式盐与碱反应时的产物要根据相对用量判断
如Ca(HCO3)2溶液中滴加NaOH溶液:
Ca(HCO3)2+NaOH==CaCO3↓+NaHCO3+ H2O(NaOH少量)
Ca(HCO2)2+2NaOH==CaCO3↓+Na2CO3+ 2H2O(NaOH过量)
2.CO32-和HCO3-的鉴别
(1)利用正盐和酸式盐的溶解性可区别CO32-和HCO3-,如分别和BaCl2溶液反应,生成的BaCO3不溶,生成的Ba(HCO3)2易溶;
(2)利用与H+反应产生CO2的快慢检验CO32-或HCO3-
碳族元素:
1.在元素周期表中的位置及结构碳旌死素位于第ⅣA族,包括碳(C)、硅(Si)、锗(Ge)、锡(Sn)、铅(Pb)五种元素。最外层皆有4个电子,这种结构不易得电子也不易失电子,易形成共价键,难形成离子键。
2.主要化合价碳族元素的化合价主要有+2和+4,C、Si、Ge、Sn的+4价化合物较稳定,而Pb的+2价化合物较稳定。
3.氢化物、最高价氧化物及其对应的水化物
氢化物:
最高价氧化物:RO2;
最高价氧化物对应的水化物为H2RO3、 H4RO4或R(OH)4
4.碳族元素的金属性与非金属性的递变规律由C至Pb,核电荷数逐渐增多,原子半径逐渐增大,原子核对最外层电子的吸引能力逐渐减小,失电子能力逐渐增强,得电子能力逐渐减弱,非金属性逐渐减弱,金属性逐渐增强。由碳族元素形成的单质中,碳、硅为非金属,但硅有金属光泽;锗、锡、铅为金属。
与“下列叙述正确的是[ ]A.Li在氧气中燃烧主要生成Li2O2B.将SO2通...”考查相似的试题有:
- 下列说法中,正确的是( )A.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用B.钢铁设备与外加直流电源的正极相连可以防...
- Al、Fe、Cu都是重要的金属元素。下列说法正确的是A.三者对应的氧化物均能溶于水B.三者的单质放置在空气中均只生成氧化物C....
- 下列用途主要体现铝的物理性质的是:①家用铝锅 ②盛浓硝酸的容器 ③制导线 ④焊接钢轨 ⑤包装铝箔 ⑥炼钢的脱氧剂 ⑦做防锈油漆A.①...
- 不能用Cl2跟金属单质直接化合制取的物质是 A. AlCl3B. FeCl3C.CuCl2D. FeCl2
- 下列实验“操作和现象”与“结论”对应关系不正确的是[ ]A.AB.BC.CD.D
- 下列说法正确的是( )A.硫粉在过量的氧气中燃烧可以生成SO3B.可以用澄清石灰水鉴别CO2和SO2C.将少量CO2通入BaCl2溶液能生...
- 工业制CuSO4时,不是直接用铜与浓硫酸在加热条件下反应,而是将铜丝浸入稀硫酸中,再不断由容器下部吹入细小的空气泡,这样做...
- SO2是一种重要的化工原料,也是一种环境污染物。(1)SO2可用于工业制Br2过程中吸收潮湿空气中的Br2,反应的离子方程式是 。...
- 近年来,有科学家提出硅是“21世纪的能源”“未来的石油”的观点。下列关于硅的说法中不正确的是A.硅是一种亲氧元素,在自然界中...
- 2006年8月4日,青海格尔木一市民在昆仑山河道发现一块重约46吨的巨石,疑似玉石,实属罕见。经测定其化学成分为Mg3Ca2Al2Si8O...