本试题 “实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回烧瓶内),加热回...” 主要考查您对有机物的合成
乙酸乙酯的制备
设计实验方案及探究实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 有机物的合成
- 乙酸乙酯的制备
- 设计实验方案及探究实验
有机合成过程主要包括两个方面,
其一是碳原子骨架的变化,例如碳链的增长和缩短、链状和环状的互相转化;
其二是官能团的引入和消除、官能团的衍变等变化。
解答有机物的合成相关题目的方法:
考查有机合成实质是根据有机物的性质,进行必要的官能团反应,从而达到考查官能团性质的目的。因此,要想熟练解答此类问题,须掌握如下知识:
(1)官能团的引入:
在有机化学中,卤代烃可谓烃及烃的衍生物的桥梁,只要能得到卤代烃,就可能得到诸如含有羟基、醛
基、羧基、酯基等官能团的物质。此外,由于卤代烃可以和醇类相互转化,因此在有机合成中,如果能引入羟
基,也和引入卤原子的效果一样,其他有机物都可以信手拈来。同时引入羟基和引入双键往往是改变碳原子骨
架的终南捷径,因此官能团的引入着重总结羟基、卤原子、双键的引入。
①引入羟基(-OH)
A. 醇羟基的引入:烯烃与水加成、卤代烃水解、醛(酮)与氢气的加成、酯的水解等。
B. 酚羟基的引入:酚钠盐过渡中通入CO2,
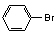 的碱性水解等。
的碱性水解等。 C. 羧羟基的引入:醛氧化为酸(被新制Cu(OH)2悬浊液或银氨溶液氧化)、酯的水解等。
②引入卤原子:烃与卤素取代、不饱和烃与HX或X2加成、醇与HX取代等。
③引入双键:某些醇或卤代烃的消去引入C=C键、醇的氧化引入C=O键等。
(2)官能团的消除:
①通过加成消除不饱和键。
②通过消去、氧化或酯化等消除羟基(-OH)
③通过加成或氧化等消除醛基(-CHO)
(3)官能团间的衍变: 可根据合成需要(或题目中所给衍变途径的信息),进行有机物官能团的衍变,以使中间物向产物递进。常见方式有以下三种:
①利用官能团的衍生关系进行衍变:如以丙烯为例,看官能团之间的转化:

上述转化中,包含了双键、卤代烃、醇、醛、羧酸、酯高分子化合物等形式的关系,领会这些关系,基本可
以把常见的有机合成问题解决。
②通过某种化学途径使一个官能团变为两个,如
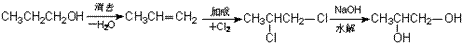
③通过某种手段,改变官能团的位置:如:
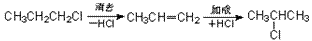
(4)碳骨架的变化:
①碳链增长:若题目中碳链增长,课本中目前的知识有:酯化反应、氨基缩合反应、不饱和结构与HCN的加
成反应、不饱和化合物间的聚合,此外常由信息形式给出,例如羟醛缩合反应、卤代烃与金属钠反应等。
例如:

②碳链变短:碳链变短的形式有烃的裂化裂解,某些烃(如烯烃、苯的同系物)的氧化、羧酸及盐的脱羧反应等。
例如:
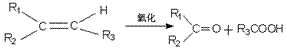
③链状变环状:不饱和有机物之间的加成,同一分子中或不同分子中两个官能团互相反应结合成环状结构。
例如,-OH与-OH间的脱水、羧基和羟基之间的反应、氨基和羧基之间的反应等。
④环状变链状:酯及多肽的水解、环烯的氧化等。当然,掌握上述相关知识后,还要分析要合成的有机物的结构,对比官能团与所给原料的官能团的异同,展开联想,理清衍变关系。同时深入理解并充分运用新信息要注意新信息与所要求合成的物质间的联系,找出
其结合点或共同性质,有时根据需要还应从已知信息中通过对比、分析、联想,开发出新的信息并加以利用。
(1)实验目的:
掌握用醇和羧酸制备酯的方法。
(2)试剂:
乙醇、冰醋酸、浓硫酸、饱和碳酸钠水溶液、饱和食盐水、饱和氯化钙、无水硫酸镁(或无水硫酸钠) 2~3g (用于干燥乙酸乙酯)
(3)反应原理:
主反应:
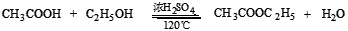
副反应:
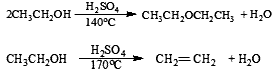
(4)反应装置图:
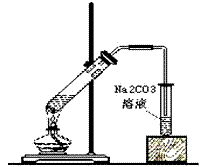
(5)操作步骤
①在一个大试管里注入乙醇2mL,再慢慢加入0.5mL浓硫酸、2mL乙酸,连接好制备乙酸乙酯的装置。
②用小火加热试管里的混合物。把产生的蒸气经导管通到3mL饱和碳酸钠溶液的上方约2mm~3mm处,注意观察盛碳酸钠溶液的试管的变化,待有透明的油状液体浮在液面上,取下盛有碳酸钠溶液的试管,并停止加热。振荡盛有碳酸钠溶液的试管,静置,待溶液分层后,观察上层液体,并闻它的气味。
③加热混合物一段时间后,可看到有气体放出,在盛碳酸钠溶液的试管里有油状物。
(6)注意事项:
1、酯化反应所用仪器必须无水,包括量取乙醇和冰醋酸的量筒也要干燥。
2、加热之前一定将反应混合物混合均匀,否则容易炭化。
3、分液漏斗的正确使用和维护。。
4、用10%碳酸钠水溶液洗涤有机相时有二氧化碳产生,注意及时给分液漏斗放气,以免气体冲开分液漏斗的塞子而损失产品。
5、正确进行蒸馏操作,温度计的位置影响流出温度,温度计水银球的上沿与蒸馏头下沿一平。
6、有机相干燥要彻底,不要把干燥剂转移到蒸馏烧瓶中。
7、反应和蒸馏时不要忘记加沸石。
8、用CaCl2溶液洗之前,一定要先用饱和NaCl溶液洗,否则会产生沉淀,给分液带来困难。
化学实验方案的设计:
1.概念:化学实验方案的设计是在实施化学实验之前.根据化学实验的目的和要求,运用相关的化学知识和技能,对实验的仪器、装置和方法所进行的一种规划。
2.实验方案设计的基本要求
(1)科学性:实验原理、实验操作程序和方法必须科学合理。
(2)安全性:尽量避免使用有毒药品和进行有一定危险性的实验操作,保护人身安全,保护仪器。
(3)可行性:实验所选用的药品、仪器、设备和方法等在中学现有条件下能满足要求。
(4)简约性:方案简单易行,尽可能采用简单的实验装置,较少的实验步骤和药品。还应遵循完成实验所用时间较短,副反应少,效果好等基本要求。
(5)经济性:综合考虑原料的用量和价格。
3.化学实验设计的基本内容一个相对完整的化学实验方案一般包括下述内容:
(1)实验名称;
(2)实验目的;
(3)实验原理;
(4)实验用品(药品、仪器、装置、设备)及规格;
(5)实验装置图、实验步骤和操作方法;
(6)实验注意事项;
(7)实验现象的记录及结果处理;
(8)问题与讨论。
4.化学实验方案设计的基本思路 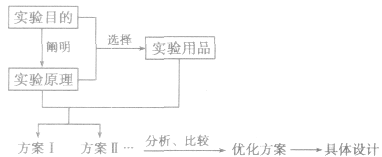
(1)明确目的、原理首先必须认真审题,明确实验的目的,弄清题目有哪些新的信息,结合已学过的知识,通过类比、迁移、分析,从而明确实验原理。
(2)选择仪器、药品根据实验的目的和原理,以及反应物和生成物的性质、反应条件(如反应物和生成物的状态、能否腐蚀仪器、反应是否需要加热及温度是否需要控制在一定的范围内等),合理选择化学仪器和药品。
(3)设汁装置、步骤根据实验目的和原理,以及所选用的仪器和药品,设计出合理的实验装置和实验操作步骤。学生应具备识别和绘制典型的实验仪器装置图的能力,实验步骤应既完整又简明。
(4)记录现象、数据根据观察,全面而准确地记录实验过程中的现象和数据。
(5)分析得出结论根据实验观察到的现象和记录的数据,通过分析、计算、图表、推理等,得出正确的结论。
化学实验方案设计的分类:
1.物质性质实验方案的设计研究物质性质的基本方法:观察法、实验法、分类法、比较法等。研究物质性质的基本程序:观察外观性质一预测物质性质一实验和观察一解释及结论。图示如下:
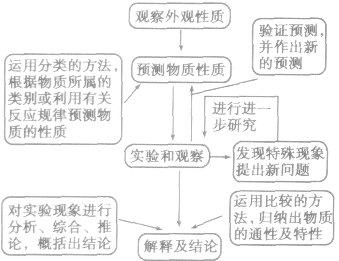
在进行性质实验方案的设计时,要充分了解物质的结构、性质、用途与制法之间的相互关系,要根据物质的结构特点,设计化学实验方案来探究或验证物质所具有的一些性质:
2.物质制备实验方案的设计
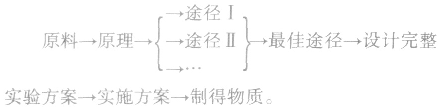
制备实验方案的设计,应遵循以下原则
(1)条件合适,操作简便;
(2)原理正确,步骤简单;
(3)原料丰富,价格低廉;
(4)产物纯净,污染物少。制备实验方案的设计,主要涉及原料、基本化学反应原理,实验程序和仪器、设备。核心是原料,由原料可确定反应原理,推导出实验步骤及所用仪器。
3.物质检验实验方案的设计

通过特定的反应现象,推断被检验物质是否存在。在对物质进行检验或鉴别时,一般的原则是:
①给出n 种物质进行鉴别,一般只需检验n一1种即可;
②物理和化学方法可并用,一般先用物理方法(如物质的颜色、气味、水溶性等),再用化学方法;
③设计的实验步骤越简单越好,实验现象越明显越好;
④有干扰离子存在时,应先排除干扰,以免得出错误的结论;
⑤进行检验的一般步骤为:观察外表一一加热固体(确定是否有结晶水)——配成溶液——观察外观一一加入试剂——观察现象——得出结论。
化学实验方案的评价:
对几个实验方案的正确与错误、严密与不严密、准确与不准确作出判断,要考虑是否合理、有无干扰现象、经济上是否合算和对环境有无污染等。
1.从可行性方面对实验方案作出评价科学性和可行性是设计实验方案的两条重要原则,在对实验方案进行评价时,要分析实验方案是否科学可行,实验方案是否遵循化学理论和实验方法的要求,在实际操作时能否做到可控易行。评价时,可从以下4个方面分析:
(1)实验原理是否正确、可行;
(2)实验操作是否安全、合理;
(3)实验步骤是否简单、方便;
(4)实验现象是否明显。
2.从“绿色化学”视角对实验方案作出评价 “绿色化学”要求设计安全的、对环境友好的合成线路,降低化学工业生产过程对人类健康和环境的危害,减少废弃物的产生和排放。据此,对化学实验过程或方案从以下4个方面进行综合评价:
(1)反应原料是否易得、安全、无毒;
(2)反应速率是否适巾;
(3)原料利用率以及合成物质的产率是否较高;
(4)合成过程中是否造成环境污染。
3.从安全性方面对实验方案作出评价从安全角度常考虑的主要因素如下:
(1)净化、吸收气体及熄灭酒精灯时要防止液体倒吸;
(2)使用某些易燃易爆品进行实验时要防爆炸(如 H2还原CuO应先通H2可燃性气体点燃前先验纯等);
(3)防氧化(如H2还原CuO后要“先灭灯再停氢”,白磷切割宜在水中进行等);
(4)防吸水(如实验取用、制取易吸水、潮解、水解的物质时宜采取必要措施,以保证达到实验目的);
(5)冷凝回流(有些反应中,为减少易挥发液体反应物的损耗和充分利用原料,需在反应装置上加装冷凝回流装置,如长玻璃管、竖装的干燥管及冷凝管等);
(6)易挥发液体产物(导出时可为蒸气)的及时冷却;
(7)仪器拆卸的科学性与安全性(可从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑);
(8)其他(如实验操作顺序、试剂加入顺序等)。
与“实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫...”考查相似的试题有:
- 甲苯是一种重要的化工原料。某化学实验小组从甲苯经一系列反应合成了化合物C。已知:(1)R-Br+MgR-MgBr(2)请完成下列各题:(1)...
- 盐酸利多卡因(F)葡萄糖注射液抗心律失常,可用于急性心肌梗死后室性早搏和室性心动过速。合成路线如下(1)B在核磁共振氢谱上...
- (10分) (1)某研究性学习小组对“钠在空气中燃烧的产物”进行了探究。其实验过程是:取一小块钠在空气中加热片刻后与一定量的水...
- (8分)(2011·西宁模拟)甲醛是世界卫生组织(WHO)确认的致癌物质和致畸物质之一。我国规定:室内甲醛含量不得超过0.08mg·m-3。...
- 下列实验设计能完成或实验结论合理的是( )A.证明一瓶红棕色气体是溴蒸气还是二氧化氮,可用湿润的碘化钾—淀粉试纸检验,观...
- 某化学兴趣小组为探索工业废料的再利用,在实验室中用含有铝、铁、铜的合金制取氯化铝溶液、绿矾晶体和胆矾晶体.其实验方案...
- 为了探究铁与氯气在一定条件下反应后的固体中铁元素的价态,化学兴趣小组的甲、乙、丙三同学分别进行了如下实验。(1)甲取少许...
- 食醋分为酿造醋和配制醋两种。国家标准规定酿造食醋总酸含量不得低于3.5 g/100 mL。(1)某研究小组利用滴定分析法测定某品牌食...
- (12分)同学们课外探究酸的性质活动中将以下8个实验分为三组进行(如下图所示)。(1)这8个实验是如何分组的?请写出各组的试...
- 在加热条件下,浓H2SO4可与食盐制取浓HCl、浓HCl可与KMnO4制取Cl2,选用下图所示装置(含有所盛放的试剂)设计实验。(1)写...