本试题 “化学与我们的生活密切相关.请回答以下生活中的几个问题:(1)活性炭能做冰箱除味剂是因为活性炭具有______;(2)“墙内开花墙外香”是因为微观上______;(3...” 主要考查您对灭火的原理和方法
构成物质的微粒(分子、原子、离子)
生石灰的性质和用途
碳的性质
中和反应及在实际中的应用
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 灭火的原理和方法
- 构成物质的微粒(分子、原子、离子)
- 生石灰的性质和用途
- 碳的性质
- 中和反应及在实际中的应用
灭火的原理:
破坏燃烧的条件,即可达到灭火的目。
①清除可燃物或使可燃物与其他物品隔离;②隔绝氧气(或空气);③使可燃物的温度降到着火点以下。破坏燃烧的三个条件中任何一个即可达到灭火的目的。
灭火原理的实验探究:
灭火方法:
①将可燃物撤离燃烧区.与火源隔离.如液化气、煤气起火,首先要及时关闭阀门,以断绝可燃物的来源;扑灭森林火灾,可用设置隔离带的方法使森林中的树木与可燃烧区隔离
②将燃着的可燃物与空气隔离,如厨房油锅起火,盖上锅盖就能灭火;二氧化碳灭火器能火火的原因之一是灭火器喷出的大量二氧化碳在燃烧物表面形成一层二氧化碳气体层,使燃烧物与在空气隔绝,达到灭火的目的
③用大量的冷却剂(如水、干冰等)冷却可燃物,使温度降低到可燃物的着火点以下,如建筑物起火时,用高压水枪灭火等。
易错点:
灭火时降低温度不是降低着火点,着火点是物质的固有属性,一般情况下不能改变。
几种常见灭火器的灭火原理和适用范围:
泡沫灭火器的灭火原理:
1. 泡沫灭火器的灭火原理:
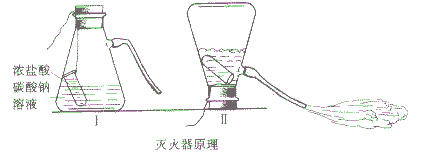
现象:当把吸滤瓶倒置后,浓HCl与Na2CO3溶液剧烈反应,产生大量CO2气体夹带着水从导管喷出。
方程式:Na2CO3+HCl==2NaCl+H2O+CO2↑(泡沫灭火原理)
2. 实际使用的泡沫灭火器,常用硫酸铝来代替盐酸(或硫酸),用碳酸氢钠来代替碳酸钠,为了产生泡沫,常放入甘草或皂角等原来制取液体。把泡沫灭火器倒转时,两种药液相互混合,发生如下反应:Al2(SO4)2+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
大量的二氧化碳跟发泡剂形成泡沫,从喷嘴中喷射出来,覆盖在燃烧物上,使燃烧物隔绝空气和降低温度,达到灭火的目的。但是,因为泡沫中含有水分,不宜用于扑救遇水发生燃烧或爆炸的物质(如钾、钠、电石等)引起的火灾;对于电器火灾,要在切断电源后才能使用泡沫灭火器。
破坏燃烧的条件,即可达到灭火的目。
①清除可燃物或使可燃物与其他物品隔离;②隔绝氧气(或空气);③使可燃物的温度降到着火点以下。破坏燃烧的三个条件中任何一个即可达到灭火的目的。
灭火原理的实验探究:
| 实验方案 | 现象 | 分析 |
点燃三支蜡烛,在其中一支蜡烛上扣一只烧杯.将另两支蜡烛放在烧杯中,然后向其中只烧杯中加适量碳酸钠和稀盐酸如下图: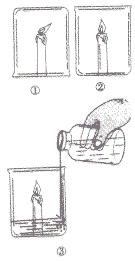 |
①在倒扣烧杯中的蜡烛熄灭 ②正放在烧杯中的蜡烛正常燃烧 ③加入适量碳酸钠和稀盐酸的烧杯中的蜡烛很快熄灭 |
①在倒扣烧杯中的蜡烛因钮气不足而熄灭 ②正放存烧杯中的蜡烛与氧气接触,温度保持在蜡烛的着火点以上,因此能正常燃烧 ⑧稀盐酸与碳酸钠迅速反应产生大量的二氧化碳气体,二氧化碳既不燃烧也不支持燃烧,所以蜡烛很快熄灭。 |
灭火方法:
①将可燃物撤离燃烧区.与火源隔离.如液化气、煤气起火,首先要及时关闭阀门,以断绝可燃物的来源;扑灭森林火灾,可用设置隔离带的方法使森林中的树木与可燃烧区隔离
②将燃着的可燃物与空气隔离,如厨房油锅起火,盖上锅盖就能灭火;二氧化碳灭火器能火火的原因之一是灭火器喷出的大量二氧化碳在燃烧物表面形成一层二氧化碳气体层,使燃烧物与在空气隔绝,达到灭火的目的
③用大量的冷却剂(如水、干冰等)冷却可燃物,使温度降低到可燃物的着火点以下,如建筑物起火时,用高压水枪灭火等。
易错点:
灭火时降低温度不是降低着火点,着火点是物质的固有属性,一般情况下不能改变。
几种常见灭火器的灭火原理和适用范围:
| 灭火器 | 灭火原理 | 适用范围 |
| 泡沫灭火器 | 灭火时.能喷射出大量二氧化碳及泡沫,它们能黏附在可燃物上,使可燃物与空气隔绝,达到灭火的目的 | 可用来扑灭木材、棉布等燃烧引起的灭火 |
| 利用压缩的二氧化碳吹出干粉(主要含有碳酸氧钠)来灭火 | 具有流动性好,喷射率高、不腐蚀容器和不易变质等优良性能,除可用来扑灭一般失火外,还可用来扑灭油、气等燃烧引起的失火 | |
| 在加压时将液态二氧化碳压缩在小钢瓶中,灭火时再将其喷出,有降温和隔绝空气的作用 | 火火时不会因留下任何痕迹而使物体损坏.因此可用来扑灭图书、档案、贵重设备、精密仪器等处的失火.使用时,手一定要先握在钢瓶的木柄上,否则.会把手冻伤。 |
泡沫灭火器的灭火原理:
1. 泡沫灭火器的灭火原理:

现象:当把吸滤瓶倒置后,浓HCl与Na2CO3溶液剧烈反应,产生大量CO2气体夹带着水从导管喷出。
方程式:Na2CO3+HCl==2NaCl+H2O+CO2↑(泡沫灭火原理)
2. 实际使用的泡沫灭火器,常用硫酸铝来代替盐酸(或硫酸),用碳酸氢钠来代替碳酸钠,为了产生泡沫,常放入甘草或皂角等原来制取液体。把泡沫灭火器倒转时,两种药液相互混合,发生如下反应:Al2(SO4)2+6NaHCO3==3Na2SO4+2Al(OH)3↓+6CO2↑
大量的二氧化碳跟发泡剂形成泡沫,从喷嘴中喷射出来,覆盖在燃烧物上,使燃烧物隔绝空气和降低温度,达到灭火的目的。但是,因为泡沫中含有水分,不宜用于扑救遇水发生燃烧或爆炸的物质(如钾、钠、电石等)引起的火灾;对于电器火灾,要在切断电源后才能使用泡沫灭火器。
构成物质的微粒:
分子、原子、离子是构成物质的基本微粒。
分子,原子,离子的比较:
分子和原子的比较:
原子与离子的比较:
分子、原子、离子是构成物质的基本微粒。
分子,原子,离子的比较:
| 分子 | 原子 | 离子 | |
| 概念 | 保持物质化学性质的最小粒子 | 是化学变化中的最小粒子 | 带电的原子或原子团 |
| 表示方法 | 用化学式表示. 如H2,He | 用元素符号表示,如H,Fe | 用离子符号表示,如Na+、NO3- |
| 微粒的运动 | 物理变化是分子运动的结果,如:水的蒸发 | 化学变化是原子运动的结果. 如:水的电解 | 离子运动的结果可能是物理变化。也可能是化学变化,如:NaCl的溶解是物理变化, NaCl与AgNO3反应是化学变化 |
| 化学计量数与符号的关系 | 化学式、元素符号、离子符号前加上化学计量数,如2H,2H2,3Na+,只表示原子、分子、离了的“个数”,不表示元素和物质 | ||
| 联系 |  | ||
分子和原子的比较:
| 原子 | 分子 | |
| 定义 | 化学变化中的最小粒子 | 保持物质(由分子直接构成的物质)化学性质的最小粒子 |
| 相同点 | ①都是构成物质的基本粒子,有些物质是由分子构成的.有些物质是由原子直接构成的; ②都很小,但者阶一定的体积和质量; ③都在不断地运动; ④微粒子间都有间隔; ⑤都能保持物质的化学性质 | |
| 区别 | 化学变化中不能再分 | 化学变化中可以再分 |
| 如:在电解水实验中,水分子可以分成氢原子和氧原子,而氢原子和氧原子不可以再分,只是重新组合成氢分子、氧分子 | ||
| 同种原子具有相同的质子数 | 同种分子化学性质相同 | |
| 联系 | 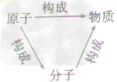 | |
原子与离子的比较:
| 原子 | 离子 | |
| 概念 | 化学变化中最小粒子 | 带电荷的原子或原子团 |
| 电性 | 呈电中性,不带电 | 带电: 阳离子带正电 阴离子带负电 |
| 表示方法 | 用元素符号表示;Na 表示钠原子,2Na表示2个钠原子 | 在元素符号右上角先写电荷数,后标出电性 (+、-):Na+表示钠离子,2Na+表示2个钠离子 |
| 数量关系 | 核内质子数=核外电子数 | 阳离子:核内质子数> 核外电子数 阴离子:核内质子数< 核外电子数 |
| 相似点 | 都是构成物质的一种粒子 | |
| 转化 |  | |
生石灰:
凡是以碳酸钙为主要成分的天然岩石,如石灰岩、白垩、白云质石灰岩等,都可用来生产石灰。 主要成分:氧化钙(CaO)。
物理性质:
一般呈块状,纯的为白色,含有杂质时为淡灰色或淡黄色。
化学性质:
在空气中吸收水和二氧化碳。氧化钙与水作用生成氢氧化钙,并放出热量。化学反应方程式为:CaO+H2O==Ca(OH)2
产品用途
1.可作填充剂,例如:用作环氧胶黏剂的填充剂;
2.用作分析试剂,气体分析时用作二氧化碳吸收剂,光谱分析试剂,高纯试剂用于半导体生产中的外延、扩散工序,实验室氨气的干燥及醇类脱l水等;
3.用作原料,可制造电石、纯碱、漂白粉等,也用于制革、废水净化,氢氧化钙及各种钙化合物;
4.可用作建筑材料、冶金助熔剂,水泥速凝剂,荧光粉的助熔剂。
5.用作植物油脱色剂,药物载体,土壤改良剂和钙肥;
6.还可用于耐火材料、干燥剂;
7.可配制农机1、2号胶和水下环氧胶黏剂,还用作与2402树脂预反应的反应剂;
8.用于酸性废水处理及污泥调质;
9.还可用作锅炉停用保护剂,利用石灰的吸湿能力,使锅炉水汽系统的金属表面保持干燥,防止腐蚀,适用于低压、中压、小容量汽包锅炉的长期停用保护;
注意事项:
1、使用操作过程时间越短越好,放置在包装容器内的适当处,起到密封吸湿的作用。
2、存放在干燥库房中,防潮,避免与酸类物接触。
3、运输过程中避免受潮,小心轻放,以防止包装破损而影响产品质量。
4、禁止食用,万一入口,用水漱口立即求医。(切记不能饮水,生石灰是碱性氧化物遇水会腐蚀!)
与熟石灰,石灰乳的区别:
1. 与熟石灰
①石灰有生石灰和熟石灰之分。生石灰的主要成分是氧化钙(CaO),白色固体耐火难溶。将(CaO)含量高的石灰岩在通风的石灰窑中锻烧至900℃以上即得。是有吸水性,可用作干燥剂,我国民间常用以防止杂物回潮。与水反应(同时放出大量的热),或吸收潮湿空气中的水分,即成熟石灰[氢氧化钙Ca(OH)2,又称“消石灰”。熟石灰在一升水中溶解1.56克(20℃),它的饱和溶液称为“石灰水”,呈碱性,在空气中吸收二氧化碳而成碳酸钙沉淀。
②与熟石灰的转化与硬化
生石灰(CaO)与水反应生成氢氧化钙的过程,称为石灰的熟化或消化。反应生成的产物氢氧化钙称为熟石灰或消石灰。
石灰熟化时放出大量的热,体积增大1—2.0倍。煅烧良好、氧化钙含量高的石灰熟化较快,放热量和体积增大也较多。工地上熟化石灰常用两种方法:消石灰浆法和消石灰粉法。
生石灰熟化后形成的石灰浆中,石灰粒子形成氢氧化钙胶体结构,颗粒极细(粒径约为1μm),比表面积很大(达10~30m2/g),其表面吸附一层较厚的水膜,可吸附大量的水,因而有较强保持水分的能力,即保水性好。将它掺入水泥砂浆中,配成混合砂浆,可显著提高砂浆的和易性。
石灰依靠干燥结晶以及碳化作用而硬化,由于空气中的二氧化碳含量低,且碳化后形成的碳酸钙硬壳阻止二氧化碳向内部渗透,也妨碍水分向外蒸发,因而硬化缓慢,硬化后的强度也不高,1:3的石灰砂浆28d的抗压强度只有0.2~0.5MPa。在处于潮湿环境时,石灰中的水分不蒸发,二氧化碳也无法渗入,硬化将停止;加上氢氧化钙微溶于水,已硬化的石灰遇水还会溶解溃散。因此,石灰不宜在长期潮湿和受水浸泡的环境中使用。
石灰在硬化过程中,要蒸发掉大量的水分,引起体积显著收缩,易出现干缩裂缝。所以,石灰不宜单独使用,一般要掺人砂、纸筋、麻刀等材料,以减少收缩,增加抗拉强度,并能节约石灰。 石灰具有较强的碱性,在常温下,能与玻璃态的活性氧化硅或活性氧化铝反应,生成有水硬性的产物,产生胶结。因此,石灰还是建筑材料工业中重要的原材料。
2. 与石灰乳
石灰乳一般是在氧化钙中加水生成的,因为氢氧化钙溶解度不是很大,所以往往生成的是氢氧化钙的悬浊液(即水溶液中还存在着没有溶解的氢氧化钙),这就是石灰乳
石灰乳是石灰浆用水稀释后的混浊液。 指石灰加入过量的水(约为石灰质量的2.5-3倍)后得到的浆体。
凡是以碳酸钙为主要成分的天然岩石,如石灰岩、白垩、白云质石灰岩等,都可用来生产石灰。 主要成分:氧化钙(CaO)。
物理性质:
一般呈块状,纯的为白色,含有杂质时为淡灰色或淡黄色。
化学性质:
在空气中吸收水和二氧化碳。氧化钙与水作用生成氢氧化钙,并放出热量。化学反应方程式为:CaO+H2O==Ca(OH)2
产品用途
1.可作填充剂,例如:用作环氧胶黏剂的填充剂;
2.用作分析试剂,气体分析时用作二氧化碳吸收剂,光谱分析试剂,高纯试剂用于半导体生产中的外延、扩散工序,实验室氨气的干燥及醇类脱l水等;
3.用作原料,可制造电石、纯碱、漂白粉等,也用于制革、废水净化,氢氧化钙及各种钙化合物;
4.可用作建筑材料、冶金助熔剂,水泥速凝剂,荧光粉的助熔剂。
5.用作植物油脱色剂,药物载体,土壤改良剂和钙肥;
6.还可用于耐火材料、干燥剂;
7.可配制农机1、2号胶和水下环氧胶黏剂,还用作与2402树脂预反应的反应剂;
8.用于酸性废水处理及污泥调质;
9.还可用作锅炉停用保护剂,利用石灰的吸湿能力,使锅炉水汽系统的金属表面保持干燥,防止腐蚀,适用于低压、中压、小容量汽包锅炉的长期停用保护;
注意事项:
1、使用操作过程时间越短越好,放置在包装容器内的适当处,起到密封吸湿的作用。
2、存放在干燥库房中,防潮,避免与酸类物接触。
3、运输过程中避免受潮,小心轻放,以防止包装破损而影响产品质量。
4、禁止食用,万一入口,用水漱口立即求医。(切记不能饮水,生石灰是碱性氧化物遇水会腐蚀!)
与熟石灰,石灰乳的区别:
1. 与熟石灰
①石灰有生石灰和熟石灰之分。生石灰的主要成分是氧化钙(CaO),白色固体耐火难溶。将(CaO)含量高的石灰岩在通风的石灰窑中锻烧至900℃以上即得。是有吸水性,可用作干燥剂,我国民间常用以防止杂物回潮。与水反应(同时放出大量的热),或吸收潮湿空气中的水分,即成熟石灰[氢氧化钙Ca(OH)2,又称“消石灰”。熟石灰在一升水中溶解1.56克(20℃),它的饱和溶液称为“石灰水”,呈碱性,在空气中吸收二氧化碳而成碳酸钙沉淀。
②与熟石灰的转化与硬化
生石灰(CaO)与水反应生成氢氧化钙的过程,称为石灰的熟化或消化。反应生成的产物氢氧化钙称为熟石灰或消石灰。
石灰熟化时放出大量的热,体积增大1—2.0倍。煅烧良好、氧化钙含量高的石灰熟化较快,放热量和体积增大也较多。工地上熟化石灰常用两种方法:消石灰浆法和消石灰粉法。
生石灰熟化后形成的石灰浆中,石灰粒子形成氢氧化钙胶体结构,颗粒极细(粒径约为1μm),比表面积很大(达10~30m2/g),其表面吸附一层较厚的水膜,可吸附大量的水,因而有较强保持水分的能力,即保水性好。将它掺入水泥砂浆中,配成混合砂浆,可显著提高砂浆的和易性。
石灰依靠干燥结晶以及碳化作用而硬化,由于空气中的二氧化碳含量低,且碳化后形成的碳酸钙硬壳阻止二氧化碳向内部渗透,也妨碍水分向外蒸发,因而硬化缓慢,硬化后的强度也不高,1:3的石灰砂浆28d的抗压强度只有0.2~0.5MPa。在处于潮湿环境时,石灰中的水分不蒸发,二氧化碳也无法渗入,硬化将停止;加上氢氧化钙微溶于水,已硬化的石灰遇水还会溶解溃散。因此,石灰不宜在长期潮湿和受水浸泡的环境中使用。
石灰在硬化过程中,要蒸发掉大量的水分,引起体积显著收缩,易出现干缩裂缝。所以,石灰不宜单独使用,一般要掺人砂、纸筋、麻刀等材料,以减少收缩,增加抗拉强度,并能节约石灰。 石灰具有较强的碱性,在常温下,能与玻璃态的活性氧化硅或活性氧化铝反应,生成有水硬性的产物,产生胶结。因此,石灰还是建筑材料工业中重要的原材料。
2. 与石灰乳
石灰乳一般是在氧化钙中加水生成的,因为氢氧化钙溶解度不是很大,所以往往生成的是氢氧化钙的悬浊液(即水溶液中还存在着没有溶解的氢氧化钙),这就是石灰乳
石灰乳是石灰浆用水稀释后的混浊液。 指石灰加入过量的水(约为石灰质量的2.5-3倍)后得到的浆体。
概述:
碳是一种非金属元素,位于元素周期表的第二周期IVA族。拉丁语为Carbonium,意为“煤,木炭”。汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音。碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本。碳是生铁、熟铁和钢的成分之一。碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子。生物体内大多数分子都含有碳元素。
碳的存在形式:
碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等。单质碳的物理和化学性质取决于它的晶体结构。高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等。
碳的化学性质:
1.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
2.可燃性:
氧气充足的条件下:C+O2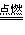 CO2
CO2
氧气不充分的条件下:2C+O2 2CO
2CO
3.还原性:
木炭还原氧化铜:C+2CuO 2Cu+CO2↑
2Cu+CO2↑
焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
焦炭还原四氧化三铁:2C+Fe3O4 3Fe+2CO2↑
3Fe+2CO2↑
木炭与二氧化碳的反应:C+CO2 CO
CO
碳”与“炭”的区别:
“碳”是一种核电荷数为6的非金属元素,而“炭” 一般是指由石墨的微小晶体和少量杂质组成的混合物,如木炭、焦炭、活性炭、炭黑等。在说明碳元素时,用“碳”表示,如碳单质、二氧化碳、碳酸等;在说明含石墨的无定形碳时,用“炭”表示,如木炭、焦炭等。
碳燃烧生成物的判断:
氧气量充足时,碳充分燃烧:C+O2 CO2
CO2
氧气量不充足时,碳不充分燃烧:2C+O2 2CO
2CO
mg碳与ng氧气反应:
①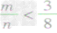 时,生成物只有CO,且O2有剩余;
时,生成物只有CO,且O2有剩余;
②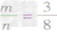 时,恰好完全反应生成CO2;
时,恰好完全反应生成CO2;
③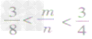 时,生成物既有CO2,也有CO;
时,生成物既有CO2,也有CO;
④ 时,恰好完全反应生成CO;
时,恰好完全反应生成CO;
⑤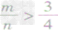 时,生成物只有CO,且C有剩余。
时,生成物只有CO,且C有剩余。
碳单质及其化合物间的转化:
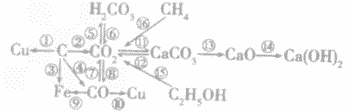
(1)C+2CuO 2Cu+CO2↑
2Cu+CO2↑
(2)C+O2 CO2
CO2
(3)3C+2Fe2O3 4Fe+3CO2↑
4Fe+3CO2↑
(4)2C+O2 2CO
2CO
(5)CO2 + H2O===H2CO3
(6)H2CO3==CO2 + H2O
(7)2CO + O2 2CO2
2CO2
(8)C+CO2 2CO
2CO
(9)3CO + Fe2O3 2Fe + 3CO2
2Fe + 3CO2
(10)CO+ 2CuO 2Cu + CO2
2Cu + CO2
(11)Ca(OH)2 + CO2====CaCO3↓+ H2O
(12)CaCO3+2HCl==CaCl2+CO2↑+H2O
(13)CaCO3 CaO+CO2
CaO+CO2
(14)CaO+H2O==Ca(OH)2
(15)C2H5OH+3O2 2CO2+3H2O
2CO2+3H2O
(16)CH4+O2 CO2+2H2O
CO2+2H2O
碳是一种非金属元素,位于元素周期表的第二周期IVA族。拉丁语为Carbonium,意为“煤,木炭”。汉字“碳”字由木炭的“炭”字加石字旁构成,从“炭”字音。碳是一种很常见的元素,它以多种形式广泛存在于大气和地壳之中。碳单质很早就被人认识和利用,碳的一系列化合物——有机物更是生命的根本。碳是生铁、熟铁和钢的成分之一。碳能在化学上自我结合而形成大量化合物,在生物上和商业上是重要的分子。生物体内大多数分子都含有碳元素。
碳的存在形式:
碳的存在形式是多种多样的,有晶态单质碳如金刚石、石墨;有无定形碳如煤;有复杂的有机化合物如动植物等;碳酸盐如大理石等。单质碳的物理和化学性质取决于它的晶体结构。高硬度的金刚石和柔软滑腻的石墨晶体结构不同,各有各的外观、密度、熔点等。
碳的化学性质:
1.稳定性:在常温下碳的化学性质稳定,点燃或高温的条件下能发生化学反应
2.可燃性:
氧气充足的条件下:C+O2
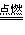 CO2
CO2 氧气不充分的条件下:2C+O2
 2CO
2CO 3.还原性:
木炭还原氧化铜:C+2CuO
 2Cu+CO2↑
2Cu+CO2↑ 焦炭还原氧化铁:3C+2Fe2O3
 4Fe+3CO2↑
4Fe+3CO2↑ 焦炭还原四氧化三铁:2C+Fe3O4
 3Fe+2CO2↑
3Fe+2CO2↑ 木炭与二氧化碳的反应:C+CO2
 CO
CO 碳”与“炭”的区别:
“碳”是一种核电荷数为6的非金属元素,而“炭” 一般是指由石墨的微小晶体和少量杂质组成的混合物,如木炭、焦炭、活性炭、炭黑等。在说明碳元素时,用“碳”表示,如碳单质、二氧化碳、碳酸等;在说明含石墨的无定形碳时,用“炭”表示,如木炭、焦炭等。
碳燃烧生成物的判断:
氧气量充足时,碳充分燃烧:C+O2
 CO2
CO2 氧气量不充足时,碳不充分燃烧:2C+O2
 2CO
2CO mg碳与ng氧气反应:
①
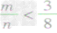 时,生成物只有CO,且O2有剩余;
时,生成物只有CO,且O2有剩余;②
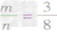 时,恰好完全反应生成CO2;
时,恰好完全反应生成CO2; ③
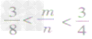 时,生成物既有CO2,也有CO;
时,生成物既有CO2,也有CO;④
 时,恰好完全反应生成CO;
时,恰好完全反应生成CO; ⑤
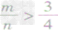 时,生成物只有CO,且C有剩余。
时,生成物只有CO,且C有剩余。 碳单质及其化合物间的转化:

(1)C+2CuO
 2Cu+CO2↑
2Cu+CO2↑ (2)C+O2
 CO2
CO2(3)3C+2Fe2O3
 4Fe+3CO2↑
4Fe+3CO2↑ (4)2C+O2
 2CO
2CO (5)CO2 + H2O===H2CO3
(6)H2CO3==CO2 + H2O
(7)2CO + O2
 2CO2
2CO2 (8)C+CO2
 2CO
2CO(9)3CO + Fe2O3
 2Fe + 3CO2
2Fe + 3CO2 (10)CO+ 2CuO
 2Cu + CO2
2Cu + CO2 (11)Ca(OH)2 + CO2====CaCO3↓+ H2O
(12)CaCO3+2HCl==CaCl2+CO2↑+H2O
(13)CaCO3
 CaO+CO2
CaO+CO2 (14)CaO+H2O==Ca(OH)2
(15)C2H5OH+3O2
 2CO2+3H2O
2CO2+3H2O(16)CH4+O2
 CO2+2H2O
CO2+2H2O中和反应:
(1)定义:酸跟碱作用生成盐和水的反应,叫做中和反应。
(2)实质:酸中的氢离子与碱中的氢氧根离子作用生成水的过程。
概念理解:
①中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应。如Fe2O3+6HCl==2FeCl3+3H2O不是中和反应
②中和反应一定是复分解反应,但复分解反应不一定是中和反应。二者的关系是复分解反应包含了中和反应。
探究中和反应是否发生的方法:
酸与碱作用生成盐和水的反应叫中和反应,中和反应一般情况下没有明显的外观现象【H2SO4+ Ba(OH)2==BaSO4↓+2H2O除外】。
探究酸碱发生中和反应的方法有以下几种(以HCl和NaOH反应为例):
1. 指示剂法。先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
2. pH试纸法。先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时多次测定混合溶液的pH。如果测得pH逐渐变小且小于7,则证明 NaOH溶液与稀盐酸发生了化学反应。
3. 热量变化法。化学反应通常伴随着能量的变化.所以可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。
中和反应的应用:
①改变土壤的酸碱性根据土壤情况,可以利用中和反应,在土壤中加人适量酸性或碱性物质,调节土壤的酸碱性,以利于植物生长。如:近年来由于空气污染造成的酸雨,导致一些地方的土壤显酸性,不利于农作物生长,人们通常向土壤中撒适量熟石灰中和其酸性。
②处理工厂的废水工厂里排出的废水有一些显酸性或碱性,直接排放会对水体和环境造成污染。通常在排出的废水中加入适量的碱性或酸性物质中和。如:废水中含有硫酸可向其中加人适从熟石灰,反应的化学方程式为:H2SO4+Ca(OH)2==CaSO4+2H2O。
③用于医药人体胃酸(主要成分是盐酸)过多,会造成消化不良,甚至会产生胃病,通常服用呈碱性的物质来消除症状,如氢氧化铝,反应的化学方程式为:3HCl+Al(OH)3== AlCl3+3H2O。被蚊虫叮咬(蚊虫能分泌出蚁酸)后,可在患处涂上显碱胜的物质,如:NH3·H2O。
(1)定义:酸跟碱作用生成盐和水的反应,叫做中和反应。
(2)实质:酸中的氢离子与碱中的氢氧根离子作用生成水的过程。
概念理解:
①中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应。如Fe2O3+6HCl==2FeCl3+3H2O不是中和反应
②中和反应一定是复分解反应,但复分解反应不一定是中和反应。二者的关系是复分解反应包含了中和反应。
探究中和反应是否发生的方法:
酸与碱作用生成盐和水的反应叫中和反应,中和反应一般情况下没有明显的外观现象【H2SO4+ Ba(OH)2==BaSO4↓+2H2O除外】。
探究酸碱发生中和反应的方法有以下几种(以HCl和NaOH反应为例):
1. 指示剂法。先在NaOH溶液中滴加几滴酚酞溶液,溶液显红色,然后再滴加盐酸,观察到红色逐渐消失,则证明NaOH溶液与稀盐酸发生了化学反应。
2. pH试纸法。先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时多次测定混合溶液的pH。如果测得pH逐渐变小且小于7,则证明 NaOH溶液与稀盐酸发生了化学反应。
3. 热量变化法。化学反应通常伴随着能量的变化.所以可借助反应前后的温度变化来判断反应的发生。如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应。
中和反应的应用:
①改变土壤的酸碱性根据土壤情况,可以利用中和反应,在土壤中加人适量酸性或碱性物质,调节土壤的酸碱性,以利于植物生长。如:近年来由于空气污染造成的酸雨,导致一些地方的土壤显酸性,不利于农作物生长,人们通常向土壤中撒适量熟石灰中和其酸性。
②处理工厂的废水工厂里排出的废水有一些显酸性或碱性,直接排放会对水体和环境造成污染。通常在排出的废水中加入适量的碱性或酸性物质中和。如:废水中含有硫酸可向其中加人适从熟石灰,反应的化学方程式为:H2SO4+Ca(OH)2==CaSO4+2H2O。
③用于医药人体胃酸(主要成分是盐酸)过多,会造成消化不良,甚至会产生胃病,通常服用呈碱性的物质来消除症状,如氢氧化铝,反应的化学方程式为:3HCl+Al(OH)3== AlCl3+3H2O。被蚊虫叮咬(蚊虫能分泌出蚁酸)后,可在患处涂上显碱胜的物质,如:NH3·H2O。
发现相似题
与“化学与我们的生活密切相关.请回答以下生活中的几个问题:(1...”考查相似的试题有:
- 很多地区以“铁”酱油为食物载体,逐步开展补铁工程.这里的铁指的是( )A.分子B.原子C.元素D.单质
- 在缉毒行动中,训练有素的缉毒犬可以准确嗅出毒品的事实说明( )A.分子是不断运动的B.分子是由原子构成的C.分子的体积很...
- 若用和表示不同元素的原子,原子的不同组合可以构成不同的分子.能用下图示意的化学反应是( )A.2H2O2MnO22H2O+O2↑B.2HgO...
- 在“宏观”、“微观”、“符号”三者之间建立联系是化学学科 特有的思维方式.(1)符号“Fe3+”的名称是_________(2)锰酸钾中所含...
- 从分子的角度分析,下列解释错误的是( )A.热胀冷缩--分子的大小随温度的改变而改变B.好酒不怕巷子深--分子在不断地运动C...
- 下列能保持氢气化学性质的是A.HB.H+C.H2D.2H
- 如图所示,锥形瓶内盛有物质Y,分液漏斗内盛有液体X,U型管内盛有红墨水(便于观察).开始时a、b处于同一水平线,当把X滴人...
- 下面是小青同学对部分化学知识的归纳,其中有错误的一组是( )A.安全知识B.化学与健康①厨房煤气管漏气关闭阀门并开窗通风②...
- 近年来,科学家们发现,除金刚石、石墨外,还有一些新的以单质形式存在的碳。其中,发现较早并在研究中取得重要进展的是C60分...
- 同学们在化学复习课上,积极交流自已的学习体会。以下是四位同学的发言,你认为其中不正确的是[ ]A.氧气是一种化学性质较活...