本试题 “下列说法中错误的是[ ]A.金属晶体的四种堆积模型中,六方最密堆积和面心立方最密堆积的空间利用率最高B.通过手性合成的方法,可以只得到一种或者主要只得到...” 主要考查您对手性(手性碳原子)
原子晶体
分子晶体
金属晶体
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 手性(手性碳原子)
- 原子晶体
- 分子晶体
- 金属晶体
手性碳原子、手性异构体与手性分子:
1.手性碳原子
连接四个不同原子或基团的碳原子,称为手性碳原子,常用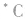 表示。如下图所示。
表示。如下图所示。
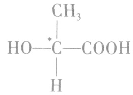
2.手性异构体
具有完全相同的组成和原子排列的一对分子,如同左手与右手一样互为镜像,但在三维空间里不能重叠,这对分子互称为手性异构体。
3.手性分子
有手性异构体的分子叫做手性分子。
4.分子是否表现手性的判断
具有手性的有机物,是因为其含有手性碳原子。所以,判断一种有机物是否具有手性异构体,就看其是否含有连有四个不同的原子或基团的碳原子。
相邻原子间以共价键相结合而形成空间网状结构的晶体,熔沸点高,导热性、延展性不良,导电性差,硬度大。如:金刚石、石英。
晶体的基本类型与性质:
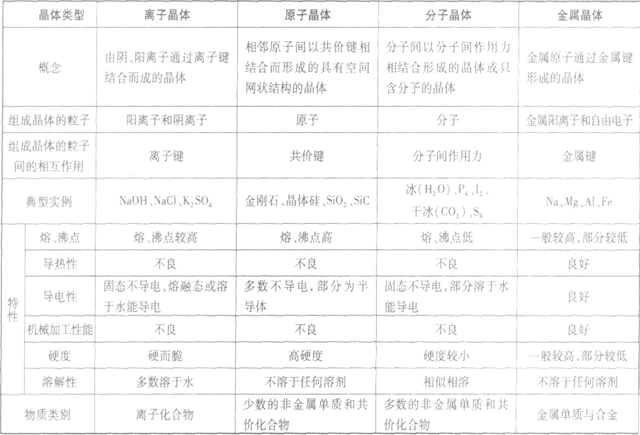
晶体熔、沸点高低的比较规律:
(1)不同类型晶体的熔、沸点高低规律:一般,原子晶体>离子晶体>分子晶体。金属晶体的熔、沸点有的很高,如钨、铂等;有的则很低,如汞、铯等。
(2)同种类型晶体,晶体内粒子间的作用力越大,熔、沸点越高。
①分子晶体:分子间作用力越大,物质的熔、沸点越高,反之越低。
a.组成和结构相似的分子,相对分子质量越大,范德华力越大,熔、沸点越高。如沸点:O2>N2、HI>HBI>HCl(含氢键的除外)。
b.相对分子质量相等或相近的分子,极性分子的范德华力大,熔、沸点高。如沸点:CO>N2。
c.含有氢键的分子熔、沸点比较高。如沸点:H2O >H2Te>H2Se>H2S,HF>HCl,NH3>PH3。
d.在烷烃的同分异构体中,一般来说,支链越多,熔、沸点越低。如沸点:正戊烷>异戊烷>新戊烷。芳香烃及其衍生物苯环上的同分异构体熔、沸点大小一般按照“邻位>问位>对位”的顺序。
e.在高级脂肪酸形成的油脂中,油的熔、沸点比脂肪低,烃基部分的不饱和程度越大(碳碳双键越多),熔、沸点越低,如:
(C17H35COO)3C3H5>(C17H33COO)3C3H5
硬脂酸甘油酯 油酸甘油酯
②原子晶体:要比较共价键的强弱。一般来说,原子半径越小,键长越短,键能越大,共价键越牢固,晶体的熔、沸点越高.如熔点:金刚石(C—C)>金刚砂 (Si—C)>晶体硅(Si—Si)>锗(Ge—Ge)。
③离子晶体:要比较离子键的强弱。一般来说,阴、阳离子电荷数越多,离子半径越小,离子键越强,熔、沸点越高,如熔点:MgO>NaCl,KF>KCl>KBr> KI。离子晶体的晶格能越大,其熔、沸点越高。
④金属晶体:要比较金属键的强弱。金属晶体中金属原子的价电子数越多,原子半径越小,金属阳离子与自由电子间的静电作用越强,金属键越强,熔、沸点越高,反之越低,如熔点:Na<Mg<Al。
(3)元素周期表中ⅦA族卤素的单质(分子晶体) 的熔、沸点随原子序数递增而升高;笫IA族碱金属元素的单质(金属晶体)的熔、沸点随原子序数的递增而降低。如熔、沸点:Li>Na>K>Rb>Cs。
注意:上述总结的是一般规律,不能绝对化。在具体比较晶体的熔、沸点高低时,应先弄清晶体的类型,然后根据不同类型晶体进行判断,但应注意具体问题具体分析。如MgO为离子晶体,[大]为离子半径小且离子电荷多,离子键较强,其熔点(2852℃)要高于部分原子晶体,如SiO2(1710℃)。
分子之间通过分子间作用力结合形成的晶体,熔沸点低,导热性、延展性不良,导电性差,硬度较小。如:干冰、固态氖。
晶体的基本类型与性质:

晶体结构模型:
| 晶体 | 晶体结构模型 |
| 氯化铯晶体 |  |
| 氯化钠晶体 | 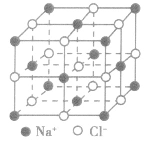 |
| 氟化钙晶体 |  |
| 二氧化碳晶体 | 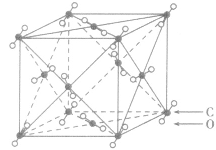 |
| 金刚石晶体 |  |
| SiO2晶体 | 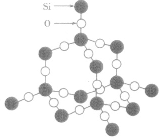 |
| 石墨晶体 (混合晶体) | 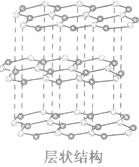 |
晶体中的几个不一定:
(1)由非金属元素构成的晶体不一定为分子品体。如NH4Cl。
(2)具有导电性的晶体不一定是金属晶体。如Si、石墨。
(3)离子晶体不一定只含离子键。如NaOH、 FeS2、Na2O2。
(4)由氢化物构成的晶体不一定是分子晶体。如NaH。
(5)金属与非金属元素构成的晶体不一定是离子晶体。如AlCl3为分子晶体。
(6)原子晶体不一定为绝缘体。如Si。
(7)溶于水能导电的晶体不一定是离子晶体。如HCl。
(8)离子晶体的熔点不一定低于原子晶体。如 MgO的熔点为2852℃,而SiO2的熔点为1710℃。
(9)金属晶体的熔点不一定低于原子晶体。如w 的熔点达34lO℃。
(10)金属晶体的熔点不一定高于分子晶体。如 Hg常温下呈液态,而硫、白磷常温下呈同态.
(11)金属晶体的硬度不一定小于原子晶体。如Cr 的硬度为9,仅次于金刚石。
(12)金属晶体的硬度不一定大于分子晶体。如 Na的硬度只有0.4,可用小刀切割。
(13)晶体巾有阳离子不一定有阴离子。如构成金
通过金属离子与自由电子间的较强作用(金属键)形成的单质晶体,熔沸点(除Hg外)高,导热性、延展性良好,易导电,硬度一般较大。
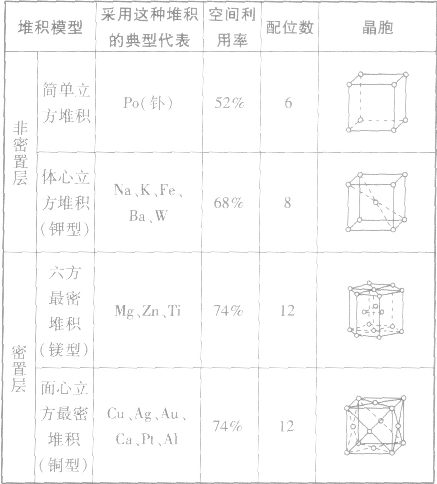
如:金属单质金属晶体原子堆积模型:
(1)简单立方堆积 (2)体心立方堆积 (3)六方最密堆积和面心立方最密堆积
晶体的基本类型与性质:
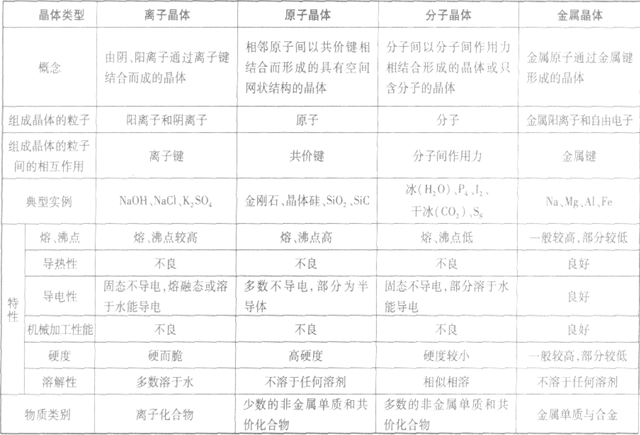
金属晶体的原子堆积模型:
与“下列说法中错误的是[ ]A.金属晶体的四种堆积模型中,六方最...”考查相似的试题有:
- (8分)选择以下物质填写下列空白:A.氢氧化钠B.氧化镁C.HeD.二氧化硅E.氯化铵 F.碘晶体 G.二氧化硫 H.钾(1)晶体中...
- (12分)镍(Ni)可形成多种配合物,且各种配合物有广泛的用途。(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂...
- 下列晶体中属于原子晶体的是( )A.干冰B.食盐C.金刚石D.氖
- 氮化硅(Si3N4)是一种新型的耐高温耐磨材料,在工业上有广泛用途,它属于( )A.原子晶体B.分子晶体C.金属晶体D.离子晶体
- 在下列有关晶体的叙述中错误的是[ ]A.离子晶体中,一定存在离子键B.原子晶体中,只存在共价键C.金属晶体的熔、沸点均很高D.分...
- [化学——选修物质结构与性质](15分)乙炔是有机合成工业的一种原料。工业上曾用与水反应生成乙炔。(1)将乙炔通入溶液生成...
- 某物质的晶体中含A、B、C三种元素,其排列方式如图所示(其中前后两面心上的B原子未能画出),晶体中A、B、C的中原子个数之比依...
- 我国前科学院院长卢嘉锡与法裔加拿大科学家Gignere巧妙地利用尿素 (H2NCONH2)和H2O2形成加合物H2NCONH2·H2O2,不但使H2O2稳定...
- 纳米材料的表面粒子的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形...
- (1)BN是一种新型的无机材料,由于属等电子体物质,其结构和性质具有极大的相似性,则可推知,在BN的两种晶型中,一种是类似__...