本试题 “下列说法不正确的是[ ]A.在食品保鲜袋中放置硫酸亚铁和硅胶可以防止食品氧化变质及受潮B.金属元素的原子只有还原性,其阳离子只有氧化性C.玻璃、水泥、陶...” 主要考查您对氧化剂、还原剂
单质铝
玻璃、陶瓷、水泥
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化剂、还原剂
- 单质铝
- 玻璃、陶瓷、水泥
(1)定义:得到电子(或电子对偏向)的物质,在反应时所含元素的化合价降低。
(2)常见的氧化剂:
①活泼非金属单质:如 Cl2、Br2、O2等。
②某些高价氧化物,如SO3、MnO2等。
③氧化性含氧酸,如 浓H2SO4、HNO3、HClO等
④元素(如Mn、Cl、Fe等)处于高化合价时的盐,如KMnO4、K2Cr2O7、KClO3、FeCl3等。
⑤过氧化物,如Na2O2、H2O2等。
⑥某些金属阳离子:如Ag+、Fe3+等
还原剂:
(1)定义:失去电子(或电子对偏离)的物质,在反应时所含元素的化合价升高。
(2)常见的还原剂:
①活泼金属单质:如 Na、A1、Zn、Fe等。
②低价态的金属阳离子:如Fe2+等;
③某些非金属单质:如 H2、C等。
④元素(如C、S等)处于低价时的氧化物,如CO、NO、SO2等。
⑤元素(如Cl、S等)处于低化合价时的氢化物:如 H2S、HCl、HI、NH3等 。
⑥元素(如S、Fe等)处于低化合价时的盐或酸,如Na2SO3、H2SO3、H2C2O4、FeSO4等。
常见的氧化剂及对应的还原产物:
|
氧化剂 |
还原产物 |
| Cl2、ClO- | Cl- |
| KMnO4(H+)、MnO2 | Mn2+ |
| HNO3 | NOx、N2、NH4+ |
| 浓H2SO4 | SO2 |
| Ag+、Fe3+ | Ag、Fe2+ |
| H2O2 | H2O |
常见的还原剂及对应的氧化产物:
|
还原剂 |
氧化产物 |
|
Na、K等金属单质 |
Na+、K+ |
|
某些非金属C、S |
CO2、SO2 |
|
非金属的氢化物CH4、H2S、NH3等 |
CO2、S/SO2、NO |
|
某些低价态的氧化物CO、SO2 |
CO2、SO3 |
|
某些低价态的酸或盐H2SO3、Na2SO3等 |
SO42- |
|
某些低价态的阳离子Fe2+ |
Fe3+ |
|
H2O2 |
O2 |
易错易混点:
(1)金属单质只具有还原性,金属最高价阳离子只具有氧化性,处于中间价态的物质既有氧化性,又有还原性;
(2)非金属单质常作氧化剂,某些非金属单质也是较强的还原性物质,比如H2、C等等
(3)元素化合价的变化:
①元素最低价只有还原性,最高价只有氧化性,中间价态既有氧化性又有还原性
②同一元素在反应中化合价发生变化,只能接近不能交叉。
例如: 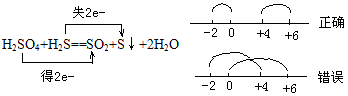
铝的主要性质:
- 物理性质:
铝是银白色,具有金属光泽的固体,硬度较小,具有良好的导电性、导热性和延展性。 - 化学性质:
活泼金属,具有较强的还原性;常温下铝在浓硫酸和浓硝酸中发生钝化;既可以与酸反应又可以与碱反应。
(1)与氧气反应: (纯氧中发出耀眼的白光)
(纯氧中发出耀眼的白光)
(2)与Cl2 、S 、N2反应: (Al2S3在溶液中完全双水解)
(Al2S3在溶液中完全双水解)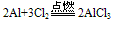
 (AlN与水反应生成Al(OH)3和NH3↑)
(AlN与水反应生成Al(OH)3和NH3↑)
(3)与水反应: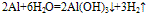
(4)与酸反应: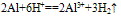
(5)与碱的反应:
(6)铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe - 铝的用途
纯铝制作导线,铝合金用于制造飞机、汽车、生活用品等。
铝的特殊性质:
铝既能与酸反应,也能与强碱反应。
铝与酸反应:铝与浓硫酸在常温下发生钝化,2Al+6HCl==2AlCl3+3H2↑
铝与碱反应:2Al+2NaOH+2H2O==2NaAlO2+3H2↑
铝热反应:
铝热法是一种利用铝的还原性获得高熔点金属单质的方法。此种反应被称为铝热反应。
可简单认为是铝与某些金属氧化物(如Fe2O3、Fe3O4、Cr2O3、V2O5等)或非金属氧化物(如SiO2等)在高热条件下发生的反应。
铝热反应常用于冶炼高熔点的金属,并且它是一个放热反应,
其中镁条为引燃剂,氯酸钾为助燃剂。
其装置如下图所示: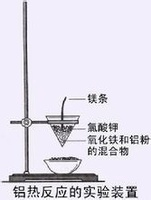
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,然后便可得到Al为8,Fe为9。
镁铝的化学性质比较:
| 单质 | 镁 | 铝 |
| 与非金属反应 | 2Mg+O2=(点燃)=2MgO (发出耀眼白光) Mg+Cl2=(点燃)=MgCl2 3Mg+N2=(点燃)=Mg3N2 |
4Al+3O2=(加热)=2Al2O3 2Al+3Cl2=(加热)=2AlCl3 2Al+3S=(加热)=Al2S3 |
| 与沸水反应 | Mg+2H2O=(加热)=Mg(OH)2+H2↑ | 不反应 |
| 与酸反应 | Mg+2H+==Mg2++H2↑ 与稀硝酸反应生成Mg(NO3)2、NOx(或者N2、NH4NO3)、H2O |
2Al+6H+==2Al3++3H2↑ 在冷的浓硝酸或浓硫酸中钝化 |
| 与氧化物反应 | 2Mg+CO2=(点燃)=2MgO+C (剧烈燃烧,生成白色粉末和黑色固体) |
2Al+Fe2O3=(高温)=2Fe+Al2O3(铝热反应) |
| 与盐溶液反应 | Mg+2NH4++2H2O==Mg2++2NH3·H2O+H2↑ Mg+Cu2+==Mg2++Cu |
2Al+3Hg2+=2Al3++3Hg |
| 与强碱反应 | 不反应 | 2Al+2OH-+2H2O==2AlO2-+3H2↑ |
铝热反应配平技巧:
取反应物和生成物中氧化物中两边氧的最小公倍数,即可快速配平,如8Al+3Fe3O4=4Al2O3+9Fe中,可取Fe3O4和Al2O3中氧的最小公倍数12,则Fe3O4前应为3Al2O3前应为4,底下便可得到Al为8,Fe为9。
铝与酸、碱反应的计算技巧:
铝与酸、碱反应的实质都是 ,
, ,所以根据得失电子守恒可知:
,所以根据得失电子守恒可知: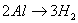 ,利用此关系可以方便地进行有关计算。
,利用此关系可以方便地进行有关计算。
铝与酸或碱溶液反应生成H2的量的计算:
Al是我们中学阶段学习的唯一既与H+反应也与OH-反应的金属,它与酸、碱反应既有相同点,也有不同点。
相同点:Al均被氧化成+3价,所以1molAl不论与H+还是与OH-反应均生成3gH2。
不同点:1molAl与H+反应消耗3molH+,而与OH-反应只消耗1molOH-,所以含有等物质的量的NaOH溶液和HCl溶液分别与足量的铝反应时生成的氢气的物质的量之比为3∶1。

“铝三角”关系:
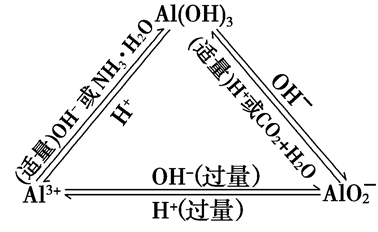
Al3++3OH-===Al(OH)3↓
Al(OH)3+OH-===AlO2-+2H2O
Al3++4OH-===AlO2-+2H2O
AlO2-+2H2O+CO2===Al(OH)3↓+HCO3-
AlO2-+H++H2O===Al(OH)3↓
AlO2-+4H+===Al3++2H2O
钝化:
铝、铁在常温下与浓硫酸发生钝化,钝化不是不反应,而是被氧化成一层致密的氧化物薄膜,恰恰说明金属的活泼性。
传统无机非金属材料:
| 硅酸盐产品 | 水泥 | 玻璃 | 陶瓷 |
| 主要设备 | 水泥回转窑 | 玻璃熔炉 | |
| 原料 | 石灰石、石膏和黏土 | 纯碱、石灰石、石英 | 黏土 |
| 反应原理 | 复杂的物理,化学变化 | Na2CO3+SiO2 Na2SiO3+CO2↑ Na2SiO3+CO2↑CaCO3+SiO2  CaSiO3+CO2↑ CaSiO3+CO2↑ |
复杂的物理,化学变化 |
| 主要成分 | 2CaO·SiO2 3CaO·SiO2 3CaO·Al2O3 |
Na2O·CaO·6SiO2 | |
| 特性 | 水硬性 | 非晶体、无固定熔点,在一定温度范围内软化可制成各种形状 | 抗氧化、抗酸碱腐蚀、耐高温、绝缘 |
| 共同特点 | ①都用含硅的物质作原料 ②反应条件都是高温 ③都发生复杂的物理、化学变化 ④冷却后都生成成分复杂的硅酸盐 | ||
几种玻璃的特性和用途:
| 种类 | 特性 | 用途 |
| 普通玻璃 | 熔点较低 | 窗玻璃、玻璃瓶等 |
| 石英玻璃 | 膨胀系数小、耐酸碱、强度大、滤光 | 化学仪器;高压水银灯、紫外灯的灯壳等 |
| 光学玻璃 | 透光性能好、有折光和色散性 | 眼镜片;照相机、显微镜、望远镜用凹凸透镜等光学仪器 |
| 玻璃纤维 | 耐踌蚀、不怕烧、不导电、不吸水、隔热、吸声、防虫蛀 | 太空飞行员的衣服等 |
| 钢化玻璃 | 耐高温、耐腐蚀、强度大、质轻、抗震裂等 | 运动器材;汽车、火车窗玻璃等 |
| 有色玻璃 | 加入金属氧化物 红色:Cu2O 蓝色:Co2O3 |
工艺品、窗玻璃等 |
无机非金属材料:
1.无机非金属材料的分类:

2.无机非金属材料的定义:
最初,无机非金属材料主要是指硅酸盐材料,所以,硅酸盐材料也称为传统无机非金属材料。随着科学和生产技术的发展,以及人们生活的需要,一些具有特殊结构、特殊功能的新材料被相继研制出来,如半导体材料、超硬耐高温材料、发光材料等,我们称这些材料为新型无机非金属材料。
与“下列说法不正确的是[ ]A.在食品保鲜袋中放置硫酸亚铁和硅胶...”考查相似的试题有:
- 以下说法正确的是[ ]A.物质所含元素化合价升高的反应叫还原反应B.在氧化还原反应中,失去电子的元素化合价降低C.物质中某...
- 下列反应中,氧化剂与还原剂物质的量关系为1︰2的是[ ]A、O3+2KI+H2O2=KOH+I2+O2B、2CH3COOH+Cu(ClO)2=2HClO+Ca(CH3COO)2C...
- 某反应体系中的物质有: NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O。⑴请将Au2O3之外的反应物与生成物分别填入以下空格内并配...
- (1)有一种叫做钾长石(K2Al2Si6O16),其化学式为写成氧化物的形式为______________(2)反应3Cu+8HNO3== 3Cu(NO3)2+2NO↑+4...
- 下列说法中正确的是( )A.铝是地壳中含量最多的金属元素B.地球上的金属元素都是以化合态形式存在于自然界中C.所有金属都具...
- 下列有关说法不正确的是[ ]A.铝制品比铁制品在空气中更容易被腐蚀B.实验室用铜片与稀硝酸反应产生的气体可用排水法收集C....
- 某古墓出土的重要文物有字画、玉带、银钵、铁猪及铁牛等。其中金属制品中保存较好的可能是( )A.银钵B.玉带C.字画D.铁牛
- (1)请写出加入NaOH溶液的体积由V2→V3时,所发生的化学反应方程式:___________________ _ _______,并由此计算合金中铝的质...
- 下列变化不可能通过一步反应直接完成的是A.Al(OH)3→ Al2O3B.Al2O3→ Al(OH)3C.Al → AlO2-D.Al3+→ Al(OH)3
- 下列物质属于硅酸盐材料的是[ ]A.碳纤维B.石灰石C.普通水泥D.石英玻璃