本试题 “在下列分子中,有的是组成蛋白质的氨基酸,有的不是。请认真分析后回答:(1)以上5种化合物中属于组成蛋白质的氨基酸有____________,这些氨基酸分子在结构上...” 主要考查您对实验:检测生物组织中的糖类、脂肪和蛋白质
氨基酸
蛋白质的结构
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 实验:检测生物组织中的糖类、脂肪和蛋白质
- 氨基酸
- 蛋白质的结构
生物组织中糖类、脂肪和蛋白质的检测方法:
1、检测原理:
生物组织中某些有机化合物能与某些化学试剂产生特定的颜色反应。
(1)糖类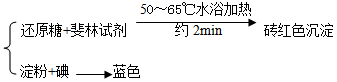
(2)脂肪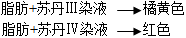
(3)蛋白质
2、检测步骤
(1)还原糖的检测与观察: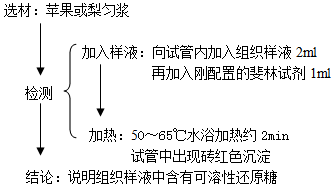
(2)脂肪的检测:
方法一:花生种子匀浆+3滴苏丹Ⅲ染液→橘黄色
方法二: 
(3)蛋白质的检测:
(4)淀粉的检测与观察: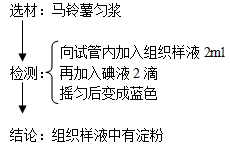
斐林试剂与双缩脲试剂的比较:
| 斐林试剂 | 双缩脲试剂 | |
| 鉴定成分 | 还原糖 | 蛋白质 |
| 鉴定原理 | 还原糖中的醛基(-CHO)在加热条件下能将Cu(OH)2中的Cu2+还原成Cu+,从而生成砖红色的Cu.0沉淀 | 双缩脲(H2NOC-NH-CONH2)在碱性溶液中能与Cuz+结合生成紫色络合物,蛋白质分子中含有与双缩脲结构相似的肽键 |
| 试剂浓度 | 甲液:质量浓度为0.1g/mL的NaOH溶液;乙液:质量浓度为0.05g/mL的CuSO4溶液 | A液:质量浓度为0.1g/mL的NaOH溶液;B液:质量浓度为0.01g/mL的CuSO4溶液 |
| 使用方法 | 甲液、乙液混合均匀后,再加入样液 | 先加A液造成碱性环境,再滴加B液 |
| 使用条件 | 加热 | 不加热 |
| 实验现象 | 浅蓝色一棕色—砖红色 | 紫色 |
知识点拨:
(1)在还原糖的鉴定实验中,最理想的实验材料是含还原糖量较高的生物组织(或器官),而且组织颜色较浅,或近于白色的苹果、梨等材料。另外,由于甘蔗、甜菜中含有的蔗糖是非还原糖,不宜选用。
(2)在脂肪的鉴定实验中,实验材料最好选择富含脂肪的种子。
(3)在蛋白质的鉴定实验中,最好选用富含蛋白质的生物组织,植物材料常用的是大豆,动物材料常用的是稀释的鸡蛋清。
注意事项:
还原糖的检测和观察:
①还原糖有葡萄糖,果糖,麦芽糖;
②甲乙液必须等量混合均匀后再加入样液中,现配现用;
③必须用水浴加热
脂肪的鉴定:
①切片要薄,如厚薄不均就会导致观察时有的地方清晰,有的地方模糊。
②酒精的作用是:洗去浮色
③需使用显微镜观察
④使用不同的染色剂染色时间不同
蛋白质的鉴定:
①先加A液1ml,再加B液4滴
②鉴定前,留出一部分组织样液,以便对比
氨基酸及其种类:
1.氨基酸的组成元素:C、H、O、N,有的含有S。
2.氨基酸的结构通式:

3.氨基酸的结构特点
(1)氨基和羧基的数目:每个氨基酸都至少含有一个氨基和一个羧基,R基中也可能含有氨基或羧基。
(2)连接位点:构成蛋白质的氨基酸都有一个-NH2和一个-COOH连在同一个碳原子上,此特点为判断某化合物是否是构成蛋白质的氨基酸的依据。
氨基酸的分类及特性:
氨基酸分为必须氨基酸和非必须氨基酸
1、必需氨基酸(essentialaminoacid):指人体(或其它脊椎动物)不能合成或合成速度远不适应机体的需要,必需由食物蛋白供给,这些氨基酸称为必需氨基酸。成人必需氨基酸的需要量约为蛋白质需要量的20%~37%。
共有8种其作用分别是:
赖氨酸:促进大脑发育,是肝及胆的组成成分,能促进脂肪代谢,调节松果腺、乳腺、黄体及卵巢,防止细胞退化;
色氨酸:促进胃液及胰液的产生;
苯丙氨酸:参与消除肾及膀胱功能的损耗;
蛋氨酸(甲硫氨酸):参与组成血红蛋白、组织与血清,有促进脾脏、胰脏及淋巴的功能;
苏氨酸:有转变某些氨基酸达到平衡的功能;
异亮氨酸:参与胸腺、脾脏及脑下腺的调节以及代谢;
脑下腺属总司令部作用于甲状腺、性腺;
亮氨酸:作用平衡异亮氨酸;缬氨酸:作用于黄体、乳腺及卵巢。
2、半必需氨基酸和条件必需氨基酸:
精氨酸:精氨酸与脱氧胆酸制成的复合制剂(明诺芬)是主治梅毒、病毒性黄疸等病的有效药物。
组氨酸:可作为生化试剂和药剂,还可用于治疗心脏病,贫血,风湿性关节炎等的药物。人体虽能够合成精氨酸和组氨酸,但通常不能满足正常的需要,因此,又被称为半必需氨基酸或条件必需氨基酸,在幼儿生长期这两种是必需氨基酸。人体对必需氨基酸的需要量随着年龄的增加而下降,成人比婴儿显著下降。(近年很多资料和教科书将组氨酸划入成人必需氨基酸)
3、非必需氨基酸(nonessentialaminoacid):
指人(或其它脊椎动物)自己能由简单的前体合成,不需要从食物中获得的氨基酸。例如甘氨酸、丙氨酸等氨基酸。
思维拓展:
1、自然界中氨基酸的种类约100种,其中在生物体中组成蛋白质的氨基酸约有20种(8种必需氨基酸),但并非生物体内每一种蛋白质都一定含有20种氨基酸。
2、8种必需氨基酸可用谐音记忆“一(异亮氨酸)家(甲硫氨酸)人来(赖氨酸)写(缬氨酸)两(亮氨酸)三(色氨酸)本(苯丙氨酸)书(苏氨酸)”。
3、儿童必需氨基酸比成人多一种,为组氨酸。
蛋白质结构的形成及多样性:
1、蛋白质的结构层次:

2、蛋白质种类多样性的原因:
(1)氨基酸的原因:
①氨基酸的种类不同。
②氨基酸的数目成百上千。
③氨基酸的排列顺序千变万化。
(2)肽链的原因:
肽链的盘曲、折叠方式及其形成的空间结构千差万别。
知识点拨:
1、脱去的水分子中的氢来自氨基和羧基,氧来自羧基。
2、肽键的写法有以下几种,这三种都是正确的。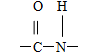 或-CO-NH-或-NH-CO-
或-CO-NH-或-NH-CO-
3、多肽中具体有几个氨基或几个羧基,应关注R基中是否有氨基或羧基。
4、若形成的多肽链是环状:氨基酸数=肽键数=失去水分子数。
5、在蛋白质分子量的计算中若通过图示或其他形式告知蛋白质分子中含有二硫键时,要考虑脱去氢的质量,每形成一个二硫键,脱去2个H。
注:1、氨基酸平均相对分子质量为a。
2、蛋白质中游离氨基或羧基数的计算
(1)至少含有的游离氨基或羧基数=肽链数
(2)游离氨基或羧基数=肽链数+R基中含有的氨基或羧基数
3、蛋白质中含有N、O原子数的计算 (1)N原子数=肽键数+肽链数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽键数+2×肽链数+R基上的O原子数=各氨基酸中O原子总数一脱去水分子数。
4、巧记氨基酸结构通式让学生把自己身体想象成一个氨基酸分子:中央C原子、头-H原子、右手——氨基(-NH2)左手——羧基(-COOH)、脚-R基(-R)
5、巧记脱水缩合过程 首先由两个人手拉手,一个人出左手拉住另一个人的右手,脱去一分子水,形成二肽。然后再加上一个人,又脱去一分子水,形成三肽,以此类推,形成多肽。
1、蛋白质的结构层次:

2、蛋白质种类多样性的原因:
(1)氨基酸的原因:
①氨基酸的种类不同。
②氨基酸的数目成百上千。
③氨基酸的排列顺序千变万化。
(2)肽链的原因:
肽链的盘曲、折叠方式及其形成的空间结构千差万别。
知识点拨:
1、脱去的水分子中的氢来自氨基和羧基,氧来自羧基。
2、肽键的写法有以下几种,这三种都是正确的。
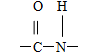 或-CO-NH-或-NH-CO-
或-CO-NH-或-NH-CO- 3、多肽中具体有几个氨基或几个羧基,应关注R基中是否有氨基或羧基。
4、若形成的多肽链是环状:氨基酸数=肽键数=失去水分子数。
5、在蛋白质分子量的计算中若通过图示或其他形式告知蛋白质分子中含有二硫键时,要考虑脱去氢的质量,每形成一个二硫键,脱去2个H。
知识拓展:
氨基酸形成多肽过程中的相关计算
1、蛋白质分子量、氨基酸数、肽链数、肽键数和脱去水分子数的关系
(1)肽键数=脱去水分子数=氨基酸数一肽链数;
(2)蛋白质分子量=氨基酸数目x氨基酸平均相对分子质量一脱去水分子数×18。
| 肽链数目 | 酸数氨基 | 脱去水分子数 | 多肽链分子量 | 氨基数目 | 羧基数目 | |
| 1条 | m | m-1 | m-1 | am-18(m-1) | 至少1个 | 至少1个 |
| 2条 | m | m-n | m-n | am-18(m-n) | 至少n个 | 至少1个 |
2、蛋白质中游离氨基或羧基数的计算
(1)至少含有的游离氨基或羧基数=肽链数
(2)游离氨基或羧基数=肽链数+R基中含有的氨基或羧基数
3、蛋白质中含有N、O原子数的计算 (1)N原子数=肽键数+肽链数+R基上的N原子数=各氨基酸中N原子总数。
(2)O原子数=肽键数+2×肽链数+R基上的O原子数=各氨基酸中O原子总数一脱去水分子数。
4、巧记氨基酸结构通式让学生把自己身体想象成一个氨基酸分子:中央C原子、头-H原子、右手——氨基(-NH2)左手——羧基(-COOH)、脚-R基(-R)
5、巧记脱水缩合过程 首先由两个人手拉手,一个人出左手拉住另一个人的右手,脱去一分子水,形成二肽。然后再加上一个人,又脱去一分子水,形成三肽,以此类推,形成多肽。
发现相似题
与“在下列分子中,有的是组成蛋白质的氨基酸,有的不是。请认真...”考查相似的试题有:
- 某实验小组为了验证乙烯的生理作用,进行了下列实验:某种番茄成熟时呈红色,取A、B两箱尚未成熟的番茄(绿色),A箱用一定量的...
- 以洋葱为实验材料,可以完成的实验是[ ]A.鳞片叶表皮细胞呈紫色,可用于光合色素的提取和分离实验B.根尖细胞分裂旺盛,前期...
- 在下列四个试管中分别加入一些物质,甲试管:新鲜乳酸奶;乙试管:甘氨酸溶液;丙试管:豆浆和蛋白酶;丁试管:鸡血液中的红...
- 假设你去某饲料研究所进行课外实践活动,需要完成以下任务:(1)选用恰当的试剂检测某样品中是否含有蛋白质。提供的试剂有:①...
- 肽:_____________________________________________。
- 全世界每年有成百上千人由于误吃毒蘑菇而死亡,鹅膏蕈碱就是一种毒菇的毒素,它是一种环状八肽。若20种氨基酸的平均分子量为1...
- 某蛋白质的分子式为C63H103O65N17S2,他最多可含有几个肽键[ ]A.16B.17C.18D.19
- 组成蛋白质的基本单位是[ ]A.氨基B.羧基C.核苷酸D.氨基酸
- 胰岛素是一种含由51个氨基酸缩合成的,具有两条肽链的蛋白质,对它的描述,不正确的是[ ]A.合成的场所是核糖体B.具有复杂的...
- “世界水日”的主题是“清洁用水,健康世界”。下列关于水的叙述不正确的是[ ]A.探索外星空间是否存在生命的过程中,科学家把寻...