本试题 “(16分)化学反应的能量变化、速率、限度是化学研究的重要内容。(1)有关研究需要得到C3H8(g) = 3C(石墨,s) + 4H2(g)的ΔH,但测定实验难进行。设计下图可计算...” 主要考查您对化学反应速率的定义、公式
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 化学反应速率的定义、公式
化学反应速率:
1.定义:化学反应速率是用来衡量化学反应进行的快慢程度的物理量。
2.表示方法:在容积不变的反应器中,通常用单位时间内反应物浓度的减少或生成物浓度的增加来表示。即: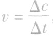
3.单位:mol·L-1·s-1或mol·L-1·min-1等。
4.注意:
(1)化学反应速率是指一段时间内的平均速率,而不是瞬时速率;通常前一段时间的平均反应速率要快于后一段时间的平均反应速率,反应速率均取正值,即v>0。
(2)在一定温度下,固体和纯液体物质单位体积的物质的量保持不变,即物质的量浓度为常数,因此在表示化学反应速率时,不代入固体或纯液体物质的浓度。浓度是指气体或溶液的浓度。
(3)同一个化学反应在相同的条件下、在同一段时间内,用不同物质表示反应速率时,数值可能相同也可能不同,但表达的意义都相同,即反应的快慢程度是一样的。
(4)在同一反应巾用不同的物质来表示反应速率时,其数值之比等于化学方程式中各物质的化学计量数之比.
如化学反应: ,
,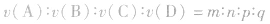 ,所以
,所以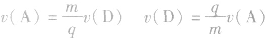
发现相似题
与“(16分)化学反应的能量变化、速率、限度是化学研究的重要内容...”考查相似的试题有:
- 已知反应A2(g)+2B2(g)2AB(g)的△H<0,下列说法正确的是A.升高温度,正向反应速率增加,逆向反应速率减小B.升高温度有...
- 在一密闭容器中充入一定量的N2和H2,经测定反应开始后的2s内氢气的平均速率:ν(H2)=0.45mol/(L-s),则2s末NH3的浓度为( ...
- 下列说法中正确的是 A.已知:2H2O(l)= 2H2(g)+O2(g);△H1>0H2O(l)=H2(g)+1/2 O2(g);△H2>0则△H1>△H2B.在合成氨...
- 500℃、20Mpa时,将H2和N2置于一容积为2L的密闭容器中发生反应。反应过程中H2、N2和NH3物质的量变化如图所示,下列说法正确的...
- 已知在某密闭容器中发生反应 4NH3+5O2=4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则下列关系正确的是A...
- 下列说法正确的是( )A.化学反应速率通常用单位时间内反应物或生成物的质量变化来表示B.用不同物质的浓度变化表示同一时间...
- 某一化学反应中反应物B的物质的量浓度在5s内从4.0mol•L-1变成1.0mol•L-1,在这5s内B的化学反应速率为( )A.3mol•L-1•s-1B....
- 在密闭容器中发生可逆反应4NH3+5O24NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是 ( )A.v(O2)="0.01" mol·L-1·s-1B...
- 下列关于化学反应速率的说法中,正确的是[ ]A.化学反应速率通常表示在一定时间内任何一种反应物物质的量的减少或任何一种生...
- NaHSO3溶液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,根据I2析出所需时间可以求得NaHSO3的反应速率。将...