本试题 “下列实验操作正确的是( )A.测定某浓度盐酸的pH时,先将pH试纸用蒸馏水湿润B.蒸馏时,将温度计的水银球插入蒸馏烧瓶中液面以下C.分液时,分液漏斗中下层...” 主要考查您对蒸馏
萃取
分液
酸碱中和滴定
pH值的测定
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 蒸馏
- 萃取
- 分液
- 酸碱中和滴定
- pH值的测定
蒸馏:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 蒸馏 | 分离沸点不同的液体混合物 | 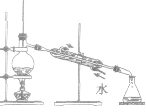 |
制无水乙醇(加生石灰)、硝酸的浓缩[加浓硫酸或 Mg(NO3)2] | ①温度计水银球在蒸馏烧瓶支管口处 ②加沸石(碎瓷片) ③注意冷凝管水流方向应下进上出 ④不可蒸干 |
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 萃取 | 分离两种互溶的液体 |  |
CCl4把溴水中的Br2萃取出来 |
①萃取后再进行分液操作 ②对萃取剂的要求:与原溶剂互不混溶,不反应;溶质在其中的溶解度比在原溶剂中大;溶质不与萃取剂反应 ③萃取后得到的仍是溶液,一般要通过分馏等方法进一步分离 |
分液:
| 名称 | 用途 | 装置 | 举例 | 注意事项 |
| 分液 | 分离两种不相混溶的液体(密度不同) | 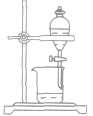 |
水、苯的分离 | 下层液体从下口放出,上层液体从上口倒出 |
酸碱中和滴定:
用已知物质的量浓度的酸(或碱)来测 定未知物质的量浓度的碱(或酸)的方法叫做酸碱中和滴定。
(1)原理:对于一元酸和一元碱发生的中和反应,C酸V酸=C碱V碱 或:C未知V未知=C标准V标准,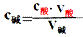
(2)仪器:a.酸式滴定管 b.碱式滴定管c.铁架台d.滴定管夹e.锥形瓶 f.烧杯g.胶头滴管等
(3)装置图: 
(4)操作步骤:
洗涤、检漏、水洗、润洗、装液、去泡、调液面记录、放待测液、加指示剂、滴定、记录、
计算、误差分析
(5)数据处理依据:
c(NaOH)=c(HCl)V(HCl)/V(NaOH)
(6)误差分析:
①仪器润洗不当:
a.盛标准液的滴定管用蒸馏水洗后未用标准液润洗;
b.盛待测液滴定(移液)管用蒸馏水洗后未用待测液润洗;
c.锥形瓶用蒸馏水洗后再用待测液润洗;
②读数方法有误:
a.滴定前仰视,滴定后俯视;
b.滴定前俯视,滴定后仰视;
c.天平或量筒的使用读数方法错误;
③操作出现问题:
a.盛标准液的滴定管漏液;
b.盛待测液的滴定管滴前尖嘴部分有气泡,终了无气泡
(或前无后有);
c.振荡锥形瓶时,不小心有待测液溅出;
d.滴定过程中,将标准液滴到锥形瓶外;
中和滴定中的误差分析:
中和滴定是一个要求较高的定量实验,每一个不当的或错误的操作都会引起误差。
对于一元酸与一元碱,由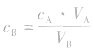 可知,
可知,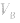 是准 确量取的体积,
是准 确量取的体积, 是标准溶液的浓度,它们均为定值,所以
是标准溶液的浓度,它们均为定值,所以 的大小取决于
的大小取决于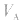 的大小,
的大小,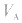 大则
大则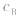 大,
大,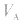 小则
小则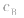 小。
小。
以标准酸溶液滴定末知浓度的碱溶液(酚酞作指示剂)为例,常见的不正确操作对实验结果的影响见下表: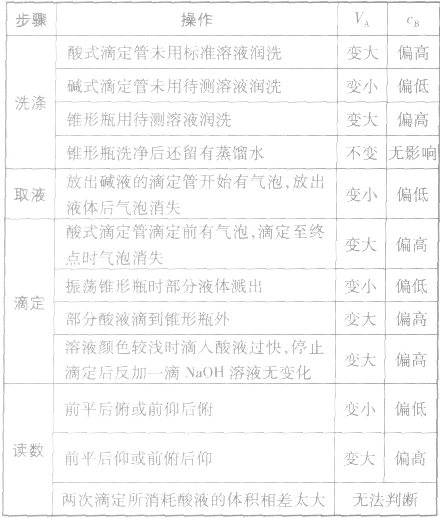
中和滴定应注意的问题:
1.中和滴定中指示剂的使用与选择
(1)用量不能太多,常用2~3滴,冈指示剂本身也是有机弱酸或有机弱碱,若用量太多,会使中和滴定中需要的酸或碱的量增多或减少。
(2)指示剂的选择:中和滴定时一般选用的指示剂有酚酞和甲基橙。石蕊试液由于颜色变化不明显,不易辨别,在滴定过程中不宜使用。
(3)酸、碱恰好完全反应时,终点溶液的pH应在指示剂的变色范围内,如强酸溶液滴定弱碱溶液应选用甲基橙作指示剂;强碱溶液滴定弱酸溶液应选用酚酞作指示剂。
(4)指示剂的变色:最好由浅到深,这样对比明显。如用强碱滴定强酸用酚酞作指示剂较好,当酚酞从无色变为粉红色(或浅红色)且半分钟内不褪色时即达到滴定终点。
2.欲减小实验误差的三点做法
(1)半分钟:振荡,半分钟内颜色不褪去,即为滴定终点。
(2)l一2min:滴定停止后,必须等待l~2min,让附着在滴定管内壁的溶液流下后,再进行读数。
(3)重复:同一实验,要做两到三次,两次滴定所用标准溶液的体积的差值不能超过0.02mL,再取平均值。
pH的测定:
1.酸碱指示剂法:只能粗略测定溶液的pH范围
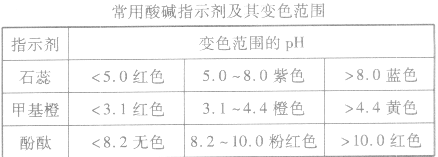
2.pH试纸法:用洁净的玻璃棒蘸取待测溶液点在一小片pH试纸(干燥的)的中部,变色后与标准比色卡对照,读出溶液的pH(粗略的整数值)。
3.pH计法(酸度计):能精确测定溶液的pH(精确到小数点后两位)。
与“下列实验操作正确的是( )A.测定某浓度盐酸的pH时,先将pH...”考查相似的试题有:
- 下列实验操作正确的是( ) 编号 实验 操作 A 实验室用自来水制备蒸馏水 将自来水倒入烧杯中,小心给烧杯加热 B 配制一定浓度...
- 下列物质与水混合静置,不出现分层的是( )A.CCl4B.C6H6C.C2H5OHD.CHCl3
- 下列各组混合物中,能用分液漏斗进行分离的是( ) A.水和四氯化碳 B.碘和四氯化碳 C.乙醇和水 D.汽油和植物油
- 某化学课外小组用海带为原料制取少量碘水.现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液.其实验操作可分为如下几步...
- 下列实验中,合理的是( )A.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出B.用100mL量筒量取5.2mL盐酸C.用...
- 下列实验操作错误的是( )A.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口B.分液时,分液漏斗中下层液体从下口放出,上层液...
- 欲萃取碘水中的I2,不能作为萃取剂的是( )A.酒精B.苯C.CCl4D.汽油
- 下列说法正确的是( )A.NaHCO3溶液加热蒸干后所得固体的成分是Na2CO3B.配制FeCl3溶液时,将FeCl3固体溶解在硫酸中,然后再...
- 有一支50mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体全部放出,盛入量筒内,所得液体体积一定是( ) A.a mL B...
- 用标准盐酸滴定未知浓度的NaOH溶液,下列各操作中,不会引起实验误差的是( )A.用蒸馏水冼净滴定管后,装入标准盐酸进行滴...