本试题 “三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物.探究过程如下:查阅资料:Cu2O是一...” 主要考查您对氧化亚铁
氧化铁
四氧化三铁
氢氧化亚铁
氢氧化铁
单质铜
氧化亚铜
氧化铜
氢氧化铜
设计实验方案及探究实验
等考点的理解。关于这些考点您可以点击下面的选项卡查看详细档案。
- 氧化亚铁
- 氧化铁
- 四氧化三铁
- 氢氧化亚铁
- 氢氧化铁
- 单质铜
- 氧化亚铜
- 氧化铜
- 氢氧化铜
- 设计实验方案及探究实验
氧化亚铁:
(1)色态:黑色粉末
(2)溶解性:不溶于水,不与水反应,溶于盐酸、稀硫酸生成亚铁盐。
(3)稳定性:不稳定,在空气中加热时迅速被氧化成四氧化三铁
(4)氧化性:(高温下)被CO、H2、Al、C、Si等还原
(5)还原性:在空气中加热氧化为Fe3O4
氧化亚铁:
(1)色态:黑色粉末
(2)溶解性:不溶于水,不与水反应,溶于盐酸、稀硫酸生成亚铁盐。
(3)稳定性:不稳定,在空气中加热时迅速被氧化成四氧化三铁
(4)氧化性:(高温下)被CO、H2、Al、C、Si等还原
(5)还原性:在空气中加热氧化为Fe3O4
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
氧化亚铁的化学性质:
- 铝热反应:2Al+3FeO=(高温)=Al2O3+3Fe
- 与非氧化性酸反应:FeO+2H+==Fe2++H2O
- 与氧化性酸反应:3FeO+10H++NO3-==3Fe3++NO↑+5H2O
氧化铁:
化学式Fe2O3,溶于盐酸,为红棕色粉末。其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中,可做催化剂,玻璃、宝石、金属的抛光剂,可用作炼铁原料。
(1)色态:红色粉末,俗称铁锈(铁红)
(2)溶解性:溶于盐酸、稀硫酸生成+3价铁盐;难溶于水,不与水反应。
(3)氧化性:高温下被CO、H2、Al、C、Si等还原
氧化铁的化学性质:
- 铝热反应:2Al+Fe2O3=(高温)=Al2O3+2Fe
- 与强酸反应:Fe2O3+6H+==2Fe3++3H2O
- 与还原性酸(HI)反应:Fe2O3+6H++2I-==2Fe2++3H2O+I2
铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
四氧化三铁:
又称磁性氧化铁,具有磁性的黑色晶体,不溶于水,具有优良的导电性。
四氧化三铁的性质:
(1)色态:具有磁性的黑色晶体
(2)别名:磁性氧化铁、氧化铁黑、磁铁、磁石、吸铁石、偏铁酸亚铁
(3)矿物:磁铁矿
(4)溶解性:不溶于水,与酸反应生成+2、+3铁盐
(5)稳定性:稳定
(6)还原性:在高温下,易氧化成三氧化二铁。4Fe3O4+O2 6Fe2O3
6Fe2O3
(7)氧化性:在高温下可与还原剂H2、CO、Al、C等反应。 


铁的氧化物:
| 化学式 | FeO | Fe2O3 | Fe3O4 |
| 俗称 | —— | 铁红 | 磁性氧化铁 |
| 色态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 铁的价态 | +2 | +3 | +2、+3 |
| 水溶性 | 不溶 | 不溶 | 不溶 |
| 与酸反应 | FeO+2H+==Fe2++H2O | Fe2O3+6H+==2Fe3++3H2O | Fe3O4+8H+==Fe2++2Fe3++4H2O |
| 用途 | 玻璃色料 | 油漆、颜料 | 做颜料和抛光剂 |
| 氧化性 | 高温时都能与C、CO、H2反应,被还原生成Fe单质 | ||
氢氧化亚铁:
化学式为Fe(OH)2,白色固体,难溶于水,碱性较弱,可与常见酸反应;在空气中易被氧化,白色→灰绿色→红褐色。反应方程式如下:
(1)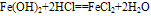
(2)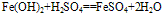
(3)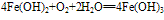
氢氧化亚铁的性质:
氢氧化亚铁极易被氧化,水中的溶解氧就可以把它氧化。
4Fe(OH)2+O2+2H2O=4Fe(OH)3
4Fe(OH)2+O2=△=2Fe2O3+4H2O
铁的氢氧化物:
| Fe(OH)2 | Fe(OH)3 | |
| 色态 | 白色固体 | 红褐色固体 |
| 与盐酸反应 | Fe(OH)2+2H+==Fe2++2H2O | Fe(OH)3+3H+==Fe3++3H2O |
| 热稳定性 | 在空气中加热迅速生成Fe3O4 | 2Fe(OH)3=(加热)=Fe2O3+3H2O |
| 二者的关系 | 在空气中Fe(OH)2能够非常迅速地被氧化成Fe(OH)3,现象是:白色迅速变成灰绿色,最后变成红褐色。反应方程式为:4Fe(OH)2+O2+2H2O===4Fe(OH)3 | |
氢氧化亚铁的制备:
因Fe(OH)2在空气中易被氧化,4Fe(OH)2+O2+2H2O===4Fe(OH)3,故Fe(OH)2在水中不能稳定存在,在实验室制取Fe(OH)2时,一定要用新制的亚铁盐和先加热驱赶掉O2的NaOH溶液,且滴管末端要插入试管内的液面以下,再滴加NaOH溶液,也可以在反应液面上滴加植物油或苯等物质进行液封,以减少Fe(OH)2与O2的接触。关于Fe(OH)2制备的方法很多,核心问题有两点,一是溶液中溶解的氧必须除去,二是反应过程必须与O2隔绝。
1、操作方法:在试管里注入少量新制备的硫酸亚铁溶液,再向其中滴入几滴煤油,用胶头滴管吸取氢氧化钠溶液,将滴管尖端插入试管里溶液液面下,逐滴滴入氢氧化钠溶液,观察现象。另外,为使氢氧化亚铁的制备成功,先将硫酸亚铁溶液加热,除去溶解的氧气。
实验现象:滴入溶液到硫酸亚铁溶液中有白色絮状沉淀生成。白色沉淀放置一段时间,振荡后迅速变成灰绿色,最后变成红褐色。
注:白色沉淀:Fe(OH)2;灰绿色沉淀:Fe(OH)2和Fe(OH)3的混合物;红褐色沉淀:Fe(OH)3
方法的改进:可在液面上滴加苯或者油进行液封,可有效防止氧的溶解。
【典例】 Ⅰ.用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述FeSO4溶液时还需要加入________。
(2)除去蒸馏水中溶解的O2常采用________的方法。
(3)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的理由是__________________________________________________________ ________________________________________________________
Ⅱ.在如图所示的装置中,用NaOH溶液、铁屑、稀H2SO4等试剂制备。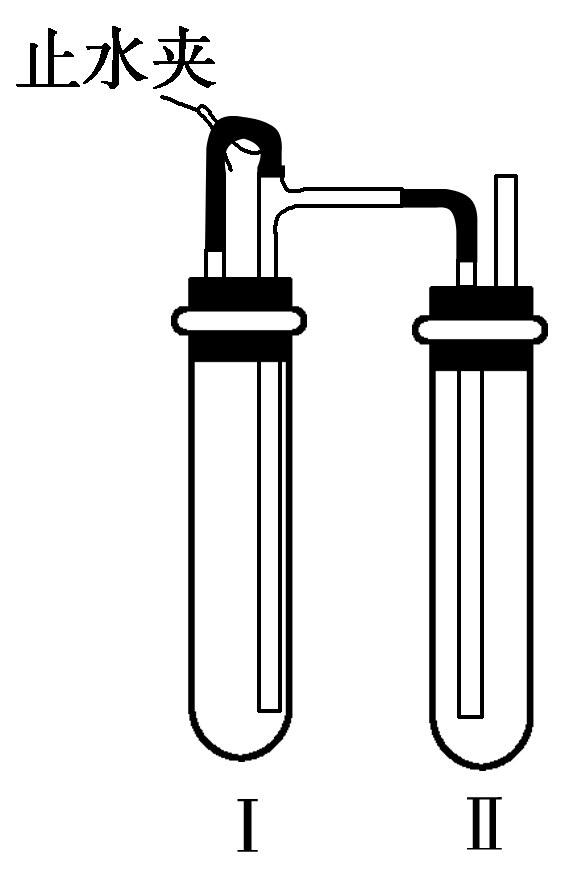
(1)在试管Ⅰ中加入的试剂是________。
(2)在试管Ⅱ中加入的试剂是________。
(3)为了制得Fe(OH)2白色沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是_____________________________。
(4)这样生成的Fe(OH)2沉淀能较长时间保持白色,理由是_________________________________________________________________。
【答案】:Ⅰ.(1)稀H2SO4、铁屑 (2)煮沸 (3)避免生成的Fe(OH)2沉淀接触O2而被氧化 Ⅱ.(1)稀H2SO4和铁屑 (2)NaOH溶液 (3)检验试管Ⅱ出口处排出的H2的纯度,当排出的H2已经纯净时再夹紧止水夹 (4)试管Ⅰ中反应生成的H2充满了试管Ⅰ和试管Ⅱ,故外界O2不易进入
2、电化学制备
【典例】 由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀。若用下图所法实验装置可制得纯净的Fe(OH)2沉淀。两极材料分别为石墨和铁。
①a电极材料为_______,其电极反应式为_______________。
②电解液d可以是_______,则白色沉淀在电极上生成;也可以是_______,则白色沉淀在两极之间的溶液中生成。
A.纯水 B.NaCl溶液 C.NaOH溶液 D.CuCl2溶液
③液体c为苯,其作用是______________,在加入苯之前,对d溶液进行加热处理的目的是___________。
④为了在短时间内看到白色沉淀,可以采取的措施是____________________。
A.改用稀硫酸做电解液 B.适当增大电源电压 C.适当缩小两电极间距离 D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为___________。
【答案】:①Fe;Fe-2e-=Fe2+ ②C;B ③隔绝空气防止Fe(OH)2被空气氧化;排尽溶液中的氧气,防止生成的Fe(OH)2在溶液中氧化 ④B、C ⑤白色沉淀迅速变成灰绿色,最后变成红褐色
氢氧化铁:
红褐色固体,难溶于水,易与酸反应;加热可分解生成氧化铁。反应方程式如下:
(1)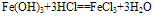
(2)
(3)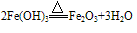
氢氧化铁胶体的制备:
操作步骤:将烧杯中的蒸馏水加热至沸腾,向沸水中滴加5~6滴饱和FeCl3溶液,继续煮沸至呈红褐色为止。
离子方程式:Fe3++3H2O=(加热)=Fe(OH)3(胶体)+3H+
铁的氢氧化物:
| Fe(OH)2 | Fe(OH)3 | |
| 色态 | 白色固体 | 红褐色固体 |
| 与盐酸反应 | Fe(OH)2+2H+==Fe2++2H2O | Fe(OH)3+3H+==Fe3++3H2O |
| 热稳定性 | 在空气中加热迅速生成Fe3O4 | 2Fe(OH)3=(加热)=Fe2O3+3H2O |
| 二者的关系 | 在空气中Fe(OH)2能够非常迅速地被氧化成Fe(OH)3,现象是:白色迅速变成灰绿色,最后变成红褐色。反应方程式为:4Fe(OH)2+O2+2H2O===4Fe(OH)3 | |
铜元素:
在元素周期表中的位置:铜的原子序数29,位于周期表中第四周期,第IB族。
(1)物理性质:有金属光泽,紫红色固体,密度较大,导电导热性能很好,具有很好的延展性,铜属于重金属、有色金属、常见金属,不能被磁铁吸引。
(2)化学性质: 铜常见的化合价为+1价和+2价
①在加热条件下,铜可与多种非金属单质反应。一般来说,遇到氧化性较弱的非金属,铜显较低化合价;遇到氧化性较强的非金属,铜显较高化合价。例如:与强氧化剂反应(如Cl2 Br2等)生成+2价铜的化合物。如:
Cu+Cl2 CuCl2 2Cu+O2
CuCl2 2Cu+O2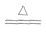 2CuO
2CuO
②铜与酸反应:铜只能被氧化性酸中的中心元素氧化。例如: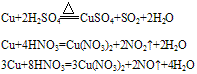
③铜与盐溶液反应:
Cu+2AgCl CuCl2+2Ag
CuCl2+2Ag
铜与铁的对比:
从金属活性顺序表:K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au可知,金属铁的金属活性比铜强,所以单质Fe可以从Cu的溶液中还原出单质来,例如: Fe+CuCl2 FeCl2+Cu
FeCl2+Cu
即Fe的还原性强于Cu
铜与浓硫酸和稀硫酸的反应:
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
2Cu+O2+2H2SO4(稀) 2CuSO4+2H2O
2CuSO4+2H2O
注意:从金属活性顺序表:K Ca Na Mg Al Zn Fe Sn Pb (H)Cu Hg Ag Pt Au 可知,铜不能与稀硫酸发生反应,但是在有氧气和加热的条件下可以反应
铜与铜的化合物之间的转换图: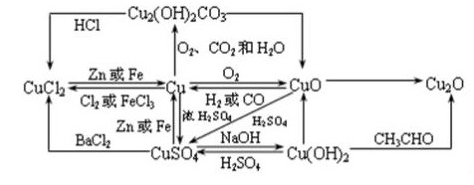
铜的制备和精炼:
(1)工业炼铜法:CuO+CO Cu+CO2
Cu+CO2
(2)湿法炼铜:Fe+CuSO4 FeSO4+Cu
FeSO4+Cu
(3)高温炼铜:工业上用高温冶炼黄铜矿的方法获得铜(粗铜):
2CuFeS2+4O2 Cu2S+3SO2+2FeO(炉渣)
Cu2S+3SO2+2FeO(炉渣)
2Cu2S+3O2 2Cu2O+2SO2
2Cu2O+2SO2
2Cu2O+Cu2S 6Cu+SO2↑
6Cu+SO2↑
备注:粗铜中铜的的含量为99.5%-99.7%,主要含有Ag、Zn、Au等杂质,粗铜通过电解精炼可得到纯度达99.95%-99.98%的铜,原理为用粗铜作阳极,失去电子变为Cu2+,用纯铜棒作阴极即可得精铜。
氧化亚铜:
氧化亚铜为红色或砖红色八面立方晶系结晶性粉末。相对密度6.0,熔点1235℃。在1800℃失去氧。不溶于水和醇,溶于盐酸、氯化铵、氨水,微溶于硝酸。
氧化亚铜的化学性质:
(1)溶于盐酸生成白色氯化亚铜结晶粉末。遇稀硫酸和稀硝酸生成铜盐。在空气中会迅速变蓝。能溶于浓碱、三氯化铁等溶液中。在湿空气中逐渐氧化成黑色氧化铜。
(2)不溶于水及有机溶剂,但可溶于浓氨溶液形成无色配合物[Cu(NH3)2]+,其在空气中被氧化为蓝色的[Cu(NH3)4(H2O)2]2+。氢卤酸反应,因生成络合物,不岐化成二价铜和铜,氧化亚铜氧化亚铜可溶于盐酸生成H[CuCl2](氯化亚铜的配合物),也可溶于硫酸及硝酸分别形成硫酸铜及硝酸铜。
知识点拨:
在酸性溶液中岐化为二价铜,说明在溶液中,二价铜离子的稳定性大于一价铜离子,例如氧化亚铜和硫酸反应,生成硫酸铜和铜。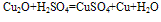
知识扩展:
氧化亚铜有剧毒,氧化亚铜粉尘在空气中含量达到0.22~14mg/m3时,工作1~2h后会引起急性中毒,表现为头痛、无力、咽和结膜发红、恶心、肌肉痛、有时呕吐和腹泻、疲乏、体温升高。一天以后体温可恢复正常,但仍无力,头痛,眩晕,脉数加快,淋巴细胞增多。氧化亚铜的慢性中毒表现为:接触铜化合物的工人的局部皮肤、头发及眼结膜有时变成浅黄色或黑绿色,齿龈上有暗红色或绛红色边。对皮肤有刺激作用,粉尘刺激眼睛,并引起角膜溃疡。对急性中毒者用一定浓度的K4[Fe(CN)6]溶液洗胃,服牛奶等措施。空气中最高容许浓度为0.1mg/m3。可戴口罩、防尘眼镜,穿防护工作服,工作后要洗淋浴。
氧化铜:
(1)物理性质:氧化铜是不溶于水的黑色固体(粉末),能溶于烯酸中,主要用于制造人造丝、陶瓷、釉、电池、杀虫剂,也用于制氢,做催化剂使用。
(2)化学性质:①氧化铜有金属氧化物的性质,常温下能与烯酸反应:CuO+2H+ Cu2++H2O
Cu2++H2O
②氧化铜具有氧化性,加热条件下可以与还原剂发生氧化还原反应:H2+CuO Cu+H2O
Cu+H2O
③氧化铜在高温下可发生分解反应:4CuO 2Cu2O+O2↑
2Cu2O+O2↑
(3)冶炼:一般通过加热分解Cu(OH)2的方式得到CuO,化学方程式为:Cu(OH)2 CuO+H2O
CuO+H2O
注意: 溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
氧化铜的特性:
| 气味 | 无味 |
| 颜色 | 黑色或者棕黑色 |
| 外观 | 无定形或结晶性粉末 |
| 性状 | 稍有吸湿性 |
| 相对质量 | 79.55 |
| 溶解性(水) | 不可溶 |
| 溶解度 | 不溶于水和乙醇,溶于酸、氯化铵及氰化钾溶液,氨溶液中缓慢溶解 |
| 稳定性 | 稳定 |
| 储存 | 密封干燥保存 |
| 用途 | 做有机反应的催化剂,制作人造丝和其他铜化合物等 |
氧化铜和氢氧化铜的性质比较:
名称
氧化铜
氢氧化铜
化学式
CuO
Cu(OH)2
物理性质
不溶水的黑色固体(粉末)
不溶于水的蓝色固体
化学性质
CuO+2H+
 Cu2++H2O
Cu2++H2O
CuO+H2 Cu+H2O
Cu+H2O
CuO+CO Cu+CO2
Cu+CO2Cu(OH)2+2H+  Cu2++2H2O
Cu2++2H2O
Cu(OH)2 CuO+H2O
CuO+H2O
Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
制法
Cu(OH)2
 CuO+H2O
CuO+H2OCu2++2OH-  Cu(OH)2↓
Cu(OH)2↓
例题:铜在自然界存在于多种矿石中,如:黄铜矿(CuFeS2)、斑铜矿(Cu5FeS4)、辉铜矿(Cu2S)、孔雀石(CuCO3·Cu(OH)2
请回答下列问题:
(1)、上表所列铜化合物中,铜的质量百分含量最高的是__Cu2S
)、工业上以黄铜矿为原料。采用火法熔炼工艺生产铜。改工艺的中间过程会发生反应:
2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
6Cu+SO2↑,反应的氧化剂是Cu2S和Cu2O
(3)、二氧化硫尾气直接排放到大气中造成环境污染的后果是形成酸雨,会对植物和建筑物等造成严重危害;该尾气可得到有价值的化学品,写出其中1中酸和1中盐的名称硫酸、硫酸钠。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需要进一步采用电解法精制。请简述粗铜电解得到精铜的大批量:以硫酸铜-硫酸溶液为电解质。电解时,粗铜(阳极)中的铜以及比铜活泼的金属失去电子进入溶液,不如铜活泼的金属沉入电解槽形成“阳极泥”;溶液中的Cu2+得到电子沉积在纯铜(阴极)上。
氧化铜与铜化合物之间的转换图:
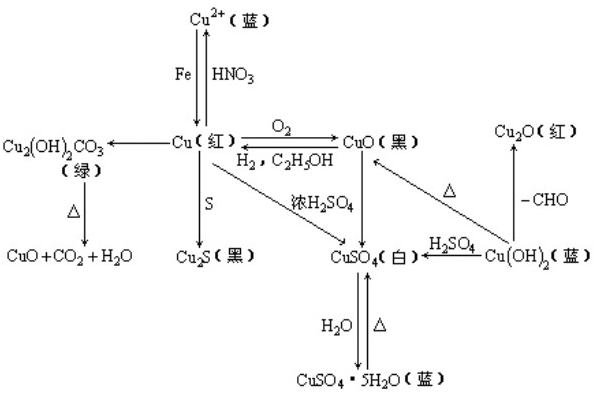
需要记住这些单质、化合物的颜色和状态,可以做为实验题的切入点。
知识扩展:
溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判断依据。Cu2+与碱发生反应生成蓝色沉淀Cu(OH)2,其溶于氨水形成蓝色溶液。
反应方程为:CuCl2+2NaOH Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O
Cu(OH)2↓+2NaCl;Cu(OH)2+4NH3·H2O Cu(NH3)4(OH)2+4H2O
Cu(NH3)4(OH)2+4H2O
氢氧化铜:
化学式Cu(OH)2,淡蓝色粉末状晶体,密度3.368g/cm3。难溶于水。受热易分解为氧化铜和水。微显两性,既溶于酸又溶于氨水和浓碱溶液。
氢氧化铜的物理性质和化学性质:
1.物理性质:不溶于水的蓝色固体
2.化学性质:Cu(OH)2+2H+==Cu2++2H2O;Cu(OH)2 CuO+H2O;Cu(OH)2+4NH3·H2O==Cu(NH3)4(OH)2+4H2O
CuO+H2O;Cu(OH)2+4NH3·H2O==Cu(NH3)4(OH)2+4H2O
知识点拨:
溶液中的Cu2+常为蓝色(浓CuCl2溶液呈绿色,稀CuCl2溶液呈蓝色),其颜色可作为Cu2+的判定依据。Cu2+与碱反应生成蓝色沉淀Cu(OH)2, Cu(OH)2溶于氨水形成深蓝色溶液。
化学实验方案的设计:
1.概念:化学实验方案的设计是在实施化学实验之前.根据化学实验的目的和要求,运用相关的化学知识和技能,对实验的仪器、装置和方法所进行的一种规划。
2.实验方案设计的基本要求
(1)科学性:实验原理、实验操作程序和方法必须科学合理。
(2)安全性:尽量避免使用有毒药品和进行有一定危险性的实验操作,保护人身安全,保护仪器。
(3)可行性:实验所选用的药品、仪器、设备和方法等在中学现有条件下能满足要求。
(4)简约性:方案简单易行,尽可能采用简单的实验装置,较少的实验步骤和药品。还应遵循完成实验所用时间较短,副反应少,效果好等基本要求。
(5)经济性:综合考虑原料的用量和价格。
3.化学实验设计的基本内容一个相对完整的化学实验方案一般包括下述内容:
(1)实验名称;
(2)实验目的;
(3)实验原理;
(4)实验用品(药品、仪器、装置、设备)及规格;
(5)实验装置图、实验步骤和操作方法;
(6)实验注意事项;
(7)实验现象的记录及结果处理;
(8)问题与讨论。
4.化学实验方案设计的基本思路 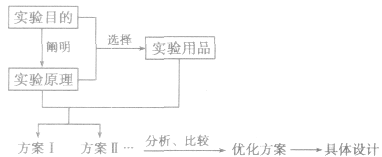
(1)明确目的、原理首先必须认真审题,明确实验的目的,弄清题目有哪些新的信息,结合已学过的知识,通过类比、迁移、分析,从而明确实验原理。
(2)选择仪器、药品根据实验的目的和原理,以及反应物和生成物的性质、反应条件(如反应物和生成物的状态、能否腐蚀仪器、反应是否需要加热及温度是否需要控制在一定的范围内等),合理选择化学仪器和药品。
(3)设汁装置、步骤根据实验目的和原理,以及所选用的仪器和药品,设计出合理的实验装置和实验操作步骤。学生应具备识别和绘制典型的实验仪器装置图的能力,实验步骤应既完整又简明。
(4)记录现象、数据根据观察,全面而准确地记录实验过程中的现象和数据。
(5)分析得出结论根据实验观察到的现象和记录的数据,通过分析、计算、图表、推理等,得出正确的结论。
化学实验方案设计的分类:
1.物质性质实验方案的设计研究物质性质的基本方法:观察法、实验法、分类法、比较法等。研究物质性质的基本程序:观察外观性质一预测物质性质一实验和观察一解释及结论。图示如下:
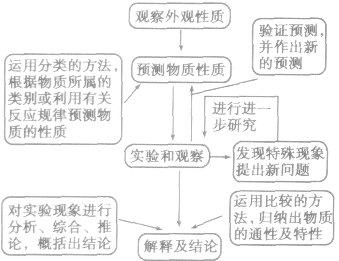
在进行性质实验方案的设计时,要充分了解物质的结构、性质、用途与制法之间的相互关系,要根据物质的结构特点,设计化学实验方案来探究或验证物质所具有的一些性质:
2.物质制备实验方案的设计
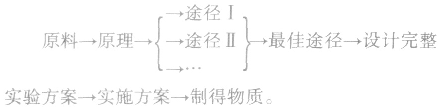
制备实验方案的设计,应遵循以下原则
(1)条件合适,操作简便;
(2)原理正确,步骤简单;
(3)原料丰富,价格低廉;
(4)产物纯净,污染物少。制备实验方案的设计,主要涉及原料、基本化学反应原理,实验程序和仪器、设备。核心是原料,由原料可确定反应原理,推导出实验步骤及所用仪器。
3.物质检验实验方案的设计

通过特定的反应现象,推断被检验物质是否存在。在对物质进行检验或鉴别时,一般的原则是:
①给出n 种物质进行鉴别,一般只需检验n一1种即可;
②物理和化学方法可并用,一般先用物理方法(如物质的颜色、气味、水溶性等),再用化学方法;
③设计的实验步骤越简单越好,实验现象越明显越好;
④有干扰离子存在时,应先排除干扰,以免得出错误的结论;
⑤进行检验的一般步骤为:观察外表一一加热固体(确定是否有结晶水)——配成溶液——观察外观一一加入试剂——观察现象——得出结论。
化学实验方案的评价:
对几个实验方案的正确与错误、严密与不严密、准确与不准确作出判断,要考虑是否合理、有无干扰现象、经济上是否合算和对环境有无污染等。
1.从可行性方面对实验方案作出评价科学性和可行性是设计实验方案的两条重要原则,在对实验方案进行评价时,要分析实验方案是否科学可行,实验方案是否遵循化学理论和实验方法的要求,在实际操作时能否做到可控易行。评价时,可从以下4个方面分析:
(1)实验原理是否正确、可行;
(2)实验操作是否安全、合理;
(3)实验步骤是否简单、方便;
(4)实验现象是否明显。
2.从“绿色化学”视角对实验方案作出评价 “绿色化学”要求设计安全的、对环境友好的合成线路,降低化学工业生产过程对人类健康和环境的危害,减少废弃物的产生和排放。据此,对化学实验过程或方案从以下4个方面进行综合评价:
(1)反应原料是否易得、安全、无毒;
(2)反应速率是否适巾;
(3)原料利用率以及合成物质的产率是否较高;
(4)合成过程中是否造成环境污染。
3.从安全性方面对实验方案作出评价从安全角度常考虑的主要因素如下:
(1)净化、吸收气体及熄灭酒精灯时要防止液体倒吸;
(2)使用某些易燃易爆品进行实验时要防爆炸(如 H2还原CuO应先通H2可燃性气体点燃前先验纯等);
(3)防氧化(如H2还原CuO后要“先灭灯再停氢”,白磷切割宜在水中进行等);
(4)防吸水(如实验取用、制取易吸水、潮解、水解的物质时宜采取必要措施,以保证达到实验目的);
(5)冷凝回流(有些反应中,为减少易挥发液体反应物的损耗和充分利用原料,需在反应装置上加装冷凝回流装置,如长玻璃管、竖装的干燥管及冷凝管等);
(6)易挥发液体产物(导出时可为蒸气)的及时冷却;
(7)仪器拆卸的科学性与安全性(可从防污染、防氧化、防倒吸、防爆炸、防泄漏等角度考虑);
(8)其他(如实验操作顺序、试剂加入顺序等)。
与“三氧化二铁和氧化亚铜都是红色粉末,常用作颜料.某校一化学...”考查相似的试题有:
- 下列各组物质反应后,再滴入KSCN溶液,显红色的是A.过量铁和稀盐酸B.FeCl2溶液和氯水C.过量铁和CuCl2溶液D.过量铁和FeCl3...
- 根据下列框图分析,下列说法正确的是( )A.E3+的氧化性比M2+的氧化性弱B.在反应①中硫酸既表现了酸性、又表现了氧化性C.反应④...
- (14分)铜及其化合物在生产、生活中有广泛的应用。Ⅰ、铜可采用如下方法制备:方法一:火法炼铜:Cu2S + O2 2Cu + SO2方法二...
- A-I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为主族元素的固态...
- 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.请就“三大酸”与金属铜反应的情况,回答下列问题:(1)我们知道,稀盐酸与铜不反...
- (1)烧瓶A中加入碎瓷片,其作用是 ;装置C处烧杯中加冰水的作用是__ ___ _。(2)装置B中发生反应的化学方程式是__ ____;装...
- (15分)铁及其化合物在生活、生产中有广泛应用。请回答下列问题:(1)Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁...
- 下列实验方案合理的是A.鉴别集气瓶中的甲烷和乙烯:分别点燃,观察火焰的颜色及是否有黑烟B.检验酒精中的少量水:向酒精中...
- 只用一种试剂就可区别NaCl、Al2(SO4)3、(NH4)2CO3、Mg(NO3)2四种溶液.这种试剂是( )A.NaOHB.BaCl2C.AgNO3D.HCl
- 图Ⅰ是化学实验室中常用制备、干燥气体的部分仪器装置。某学校同学利用中学常用试剂及仪器设计下列实验。 图Ⅰ(1)图Ⅰ中仪器C...